Clear Sky Science · ru
Взаимодействие митохондриальной биоэнергетики и SASP определяет эффективность сенолитиков при терапии‑индуцированном старении
Почему «уничтожить» «зомби»-раковые клетки так трудно
Многие современные противораковые препараты не убивают все опухолевые клетки сразу. Некоторые клетки уходят в состояние, похожее на лимбо, называемое сенесценцией: они перестают делиться, но остаются живыми, подобно «зомби»-клеткам. Такие терапевтически индуцированные сенесцентные клетки сначала могут приносить пользу, но при длительном сохранении они способны способствовать рецидивам, резистентности и побочным эффектам. Поэтому учёные тестируют сенолитики — препараты, которые селективно убивают сенесцентные клетки. В этой работе задаётся, казалось бы, простой вопрос: почему одни сенесцентные раковые клетки гибнут под действием сенолитиков, а другие упрямо выживают?
Энергетические станции, сохраняющие память о прошлом
В центре исследования — митохондрии, крошечные «электростанции» внутри клеток. Авторы изучали, влияет ли то, как митохондрии «сжигают» разные топлива — например сахара, жиры и аминокислоты — на чувствительность сенесцентных раковых клеток к сенолитикам, направленным против белка выживания BCL‑xL. С помощью высокопроизводительного анализа (MitoPlate S‑1) они функционально «сняли отпечаток» митохондриальной активности в нескольких раковых клеточных линиях до и после индукции сенесценции разными стимулами (днк‑повреждающие препараты, блокаторы митоза, оксидативный стресс или ингибиторы клеточного цикла). Они обнаружили, что терапевтически индуцированная сенесценция не формирует единого универсального митохондриального состояния. Вместо этого каждое лечение оставляло характерный «биоэнергетический отпечаток», меняя широту и интенсивность способов, которыми митохондрии могли использовать различные источники энергии. Критически важно, что эта гибкость накладывалась на уже существующую исходную конфигурацию: митохондриальная установка родительских опухолевых клеток задавала верхний предел — «потолок» — того, какой максимальный сенолитический ответ вообще возможен.
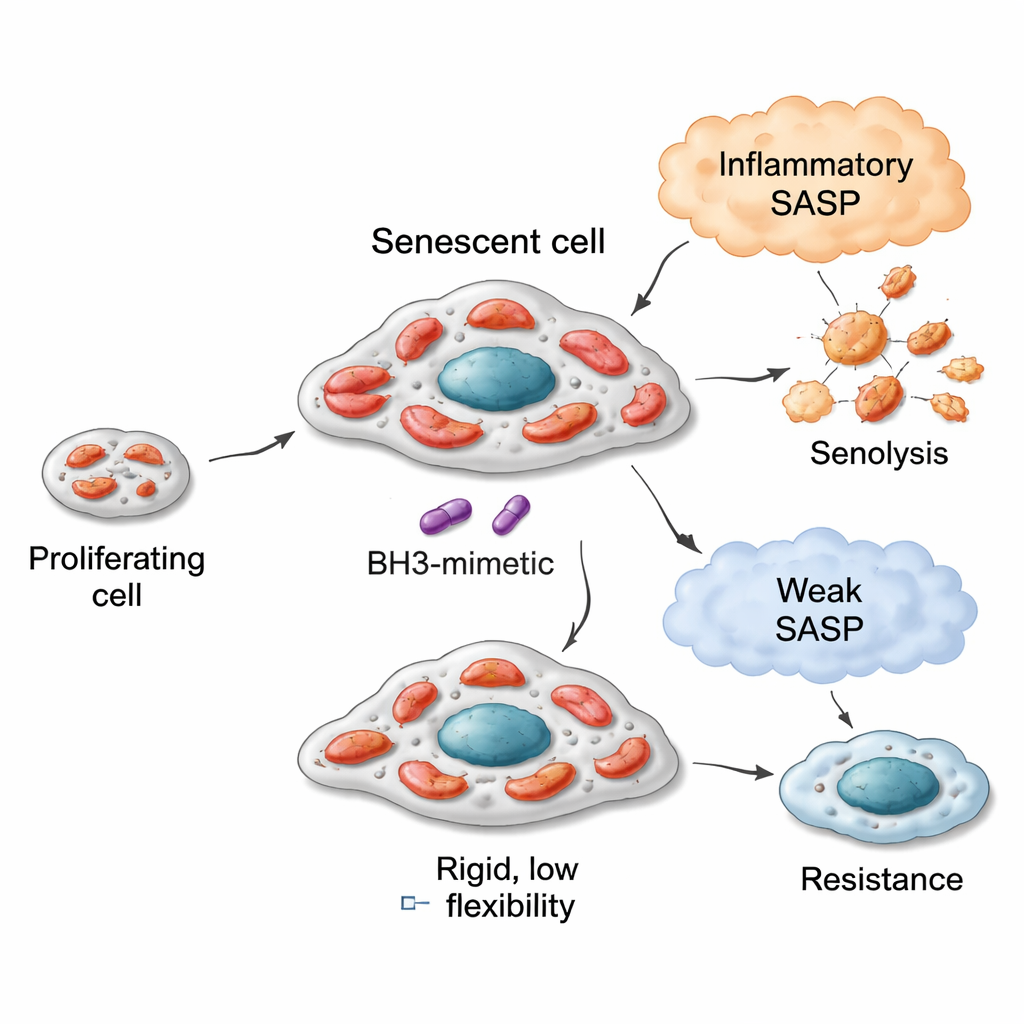
Гибкие «двигатели», разные топлива и чувствительность к сенолитикам
В моделях рака лёгких, молочной и толстой кишки сенесцентные клетки с более гибкими митохондриями — способными окислять более широкий спектр топлив — как правило, оказывались более уязвимыми к сенолитикам, нацеленным на BCL‑xL, таким как навиТоклакс (ABT‑263) и A1331852. Например, клетки рака лёгкого, введённые в сенесценцию препаратом блеомицином, развивали митохондрии, активно использующие множество субстратов, особенно связанных с распадом жирных кислот и определёнными аминокислотными путями. Эти клетки были крайне чувствительны к сенолитикам. Напротив, клетки, выведенные в сенесценцию ингибитором CDK4/6 (пальбоциклибом), продемонстрировали более узкий метаболический репертуар и слабо реагировали на те же сенолитические агенты. Однако эта зависимость имела ограничения: клетки рака молочной железы также могли стать метаболически гибкими после сенесценции, но поскольку их исходные митохондрии были менее «готовы» к апоптозу, их максимальный сенолитический ответ был умеренным. Клетки рака толстой кишки с дефектной апоптотической машиной оставались резистентными независимо от сдвигов в метаболизме. Одна простая мера — насколько хорошо клетки окисляют субстрат сукцинат в исходном состоянии — оказалась служить простым индикатором этой унаследованной митохондриальной способности.
Когда метаболизм «переговаривается» с воспалением
Сенесцентные клетки известны своим SASP — коктейлем секретируемых воспалительных и ростовых факторов, влияющих на соседние ткани. Команда изучила, как митохондриальный метаболизм связан с этой секреторной активностью, используя клетки с репортером miR‑146a, микроРНК, включаемой главным регулятором воспаления NF‑κB. Они обнаружили, что в то время как общие профили SASP в основном определялись типом клетки, только некоторые сенесцентные состояния активировали ось NF‑κB/miR‑146a. Именно эти состояния хорошо отвечали на сенолитики, нацеленные на BCL‑xL. Важно, что эти «положительные по воспалительному SASP» сенесцентные клетки также демонстрировали усиленное использование окисления жирных кислот и транскрипционное повышение выражения генов, переносящих длинноцепочечные жиры в митохондрии. Блокада входа жирных кислот с помощью препарата этомоксир ослабляла активацию miR‑146a, не полностью отменяя саму сенесценцию, что указывает на то, что выбор митохондриального топлива помогает запускать воспалительный, благоприятный для сенолитиков SASP.
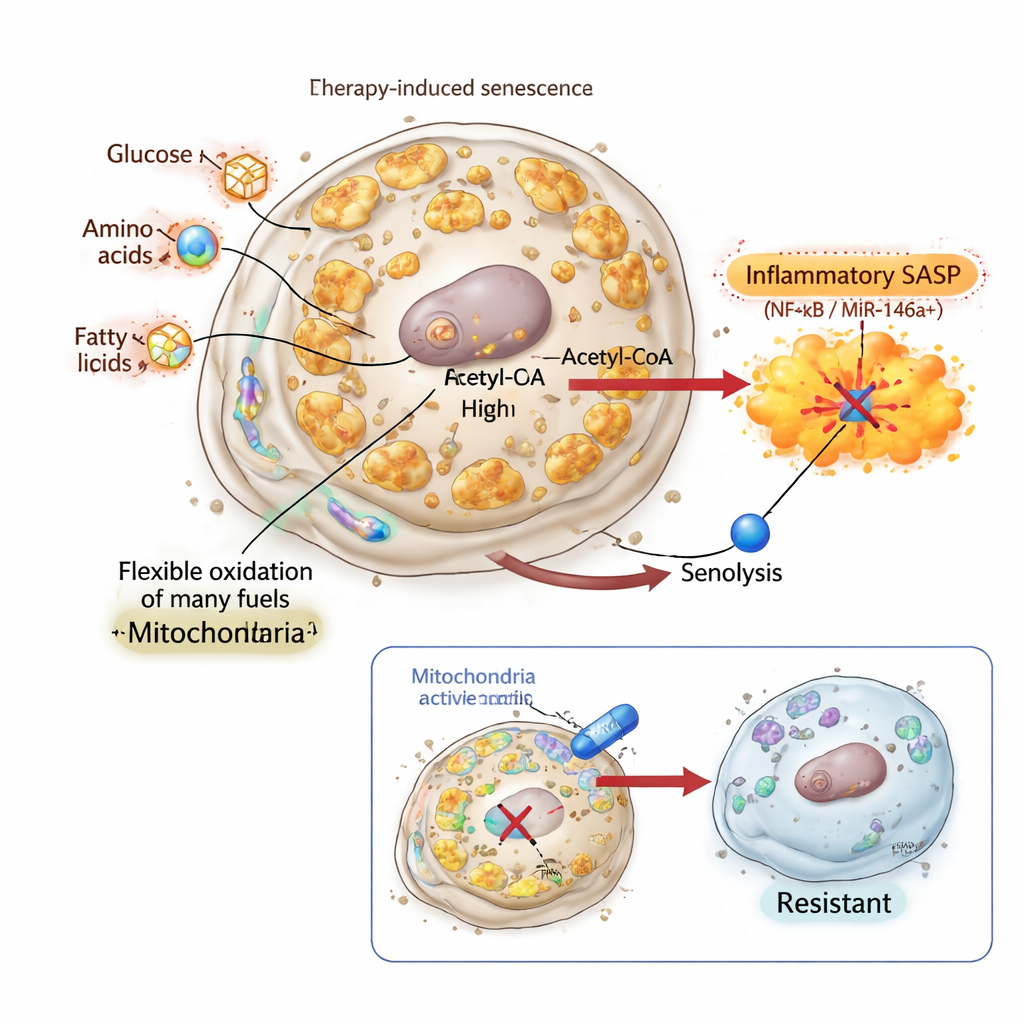
Подавление сигнала и создание неубиваемых сенесцентных клеток
Чтобы проверить, действительно ли воспалительный SASP необходим для сенолитической гибели, исследователи использовали инфлахроме́н, соединение, связывающееся с хроматиновыми белками HMGB1 и HMGB2 и блокирующее их роль в активации генов SASP. В клетках рака лёгких и молочной железы инфлахромен индуцировал классический сенесцентный фенотип: клетки увеличивались, прекращали деление и накапливали маркеры старения. Их митохондриальная масса и биоэнергетическая активность значительно возросли, и профиль использования топлива был явно перестроен. Тем не менее их SASP был притуплён, и репортер miR‑146a оставался в основном неактивным. Поразительно, что эти сенесцентные клетки без SASP были полностью резистентны к сенолитикам, нацеленным на BCL‑xL, несмотря на биоэнергетически активные, перепрограммированные митохондрии и сниженное экспрессирование классического антиапоптотического гена BCL2. Это показало, что одних митохондриальных изменений недостаточно; без митохондриально опосредованного воспалительного ответа «второй удар» сенолитиков не срабатывает.
Что это значит для будущих методов лечения рака
В пересчёте для непрофессионала, вывод исследования таков: уничтожение терапевтически индуцированных «зомби»-раковых клеток управляется многослойной цепью. Во‑первых, исходное состояние и «проводка» митохондрий опухолевой клетки задают предел того, насколько далеко могут зайти сенолитики. Во‑вторых, конкретное лечение, вызывающее сенесценцию, может сместить митохондриальный метаболизм в сторону большей или меньшей гибкости, приближая или отдаляя клетки от порога апоптоза. В‑третьих — и что решает все — сенолитики эффективны только в том случае, если метаболическое перепрограммирование успешно вовлекает воспалительную программу SASP, которая «открывает диалог» с ядром. Без этого воспалительного перекрёстного влияния сенесцентные клетки могут превратиться в тупиковое, лекарственно резистентное состояние. Практически это означает, что будущие терапии можно будет оптимизировать, функционально оценивая и митохондриальную гибкость, и воспалительность SASP в опухолях, а затем подбирая комбинации препаратов, индуцирующих сенесценцию, и сенолитиков так, чтобы «зомби»-клетки были не просто заморожены, но и подготовлены к уничтожению.
Цитирование: Llop-Hernández, À., Verdura, S., López, J. et al. Mitochondrial bioenergetics-SASP crosstalk determines senolytic efficacy in therapy-induced senescence. Cell Death Discov. 12, 103 (2026). https://doi.org/10.1038/s41420-026-02967-6
Ключевые слова: клеточное старение, митохондрии, сенолитики, раковый метаболизм, воспалительный SASP