Clear Sky Science · ru
Подавление SREBP1 вызывает ферроптоз за счёт подавления оси Nrf2‑XCT/GPX4 при раке яичников
Обратить жировую фабрику рака против него самого
Рак яичников часто обнаруживают на поздних стадиях и его бывает очень трудно лечить. В этом исследовании изучается неожиданная уязвимость таких опухолей: их зависимость от синтеза жиров и липидов. Авторы показывают, что выключение ключевого переключателя «жировой фабрики» в раковых клетках не только замедляет их рост, но и запускает особый тип клеточной гибели, а также облегчает иммунной системе атаку на опухоль.
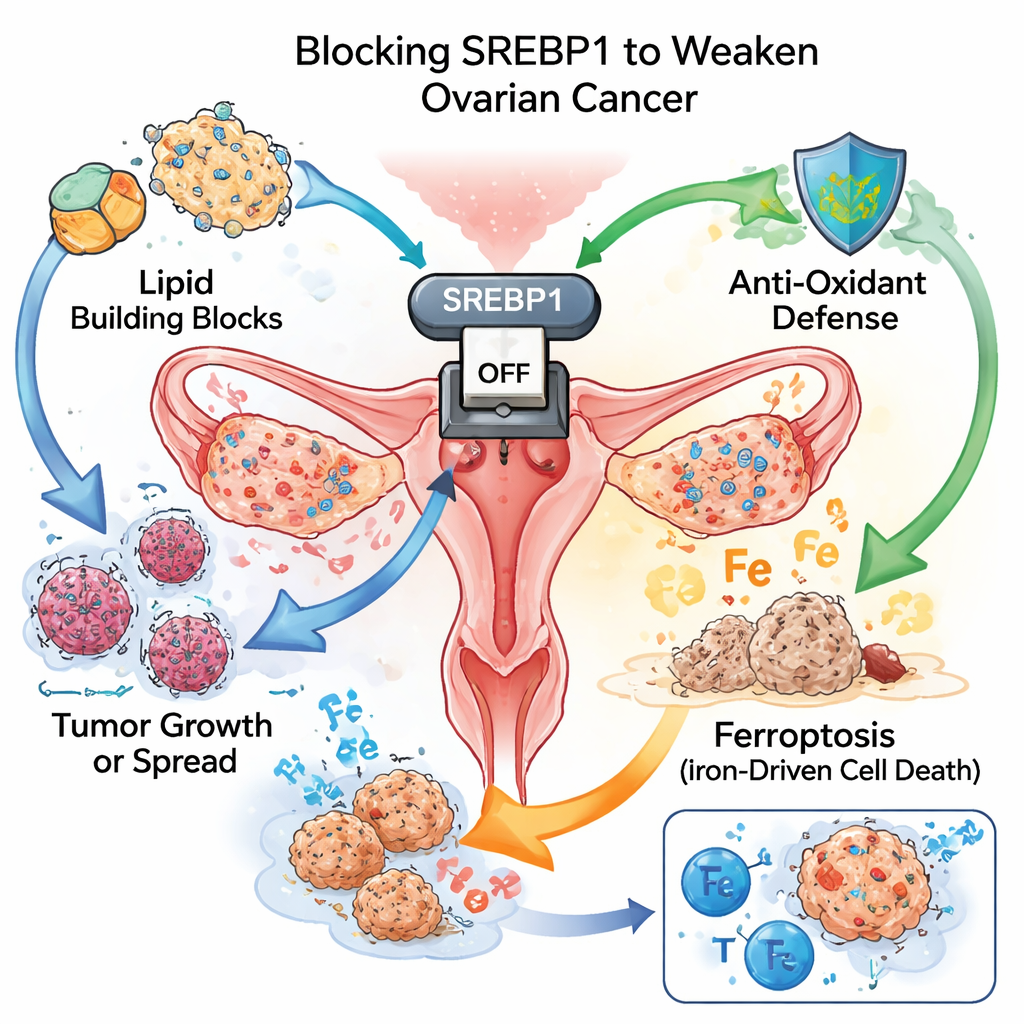
Мастер‑переключатель топлива опухоли
Как быстро растущие сорняки, раковые клетки нуждаются в огромном количестве строительных блоков и энергии. Один из способов удовлетворить эту потребность — перестроить синтез и использование жиров. Команда сосредоточилась на SREBP1 — белке, выполняющем роль мастер‑переключателя липогенеза. В образцах тканей более ста пациентов опухоли яичников имели значительно более высокий уровень SREBP1 по сравнению с прилежащей нормальной тканью. У женщин, чьи опухоли демонстрировали более интенсивную окраску по SREBP1, как правило, наблюдалось более агрессивное течение болезни и более короткая выживаемость, что делает этот белок и двигателем прогрессии, и маркером неблагоприятного прогноза.
Замедление роста и метастазирования путём перекрытия жирового питания
В культурах клеток рака яичников в лаборатории снижение экспрессии SREBP1 резко уменьшало способность клеток к размножению и образованию колоний. Клетки застревали на определённых этапах клеточного цикла и уже не могли эффективно делиться. Учёные также отметили меньше признаков подвижности и инвазии: в тестах «царапина» и Transwell клетки с пониженным уровнем SREBP1 хуже мигрировали, а ключевые маркёры эпителиально‑мезенхимального перехода (EMT) смещались в сторону более «нормального» состояния. Одновременно падали уровни триглицеридов и холестерина, а окрашивание показывало меньше липидных капель внутри клеток, что подтверждает подавление их внутренней жировой машины.
Запуск клеточной гибели на железной основе
Самый яркий эффект подавления SREBP1 — активация ферроптоза, недавно описанного типа клеточной гибели, обусловленного железом и пероксидацией липидов мембран. Только блокатор ферроптоза, а не ингибиторы других путей гибели, смог спасти клетки с выключенным SREBP1, указывая на ферроптоз как основную причину их гибели. Химические анализы показали больше продуктов окисленных жиров, меньше антиоксиданта глутатиона и более высокие уровни реактивных липидных молекул. Два белка, обычно защищающие клетки от ферроптоза — xCT и GPX4 — значительно снижались при нокауте SREBP1, устраняя важный защитный барьер против этого разрушительного процесса.
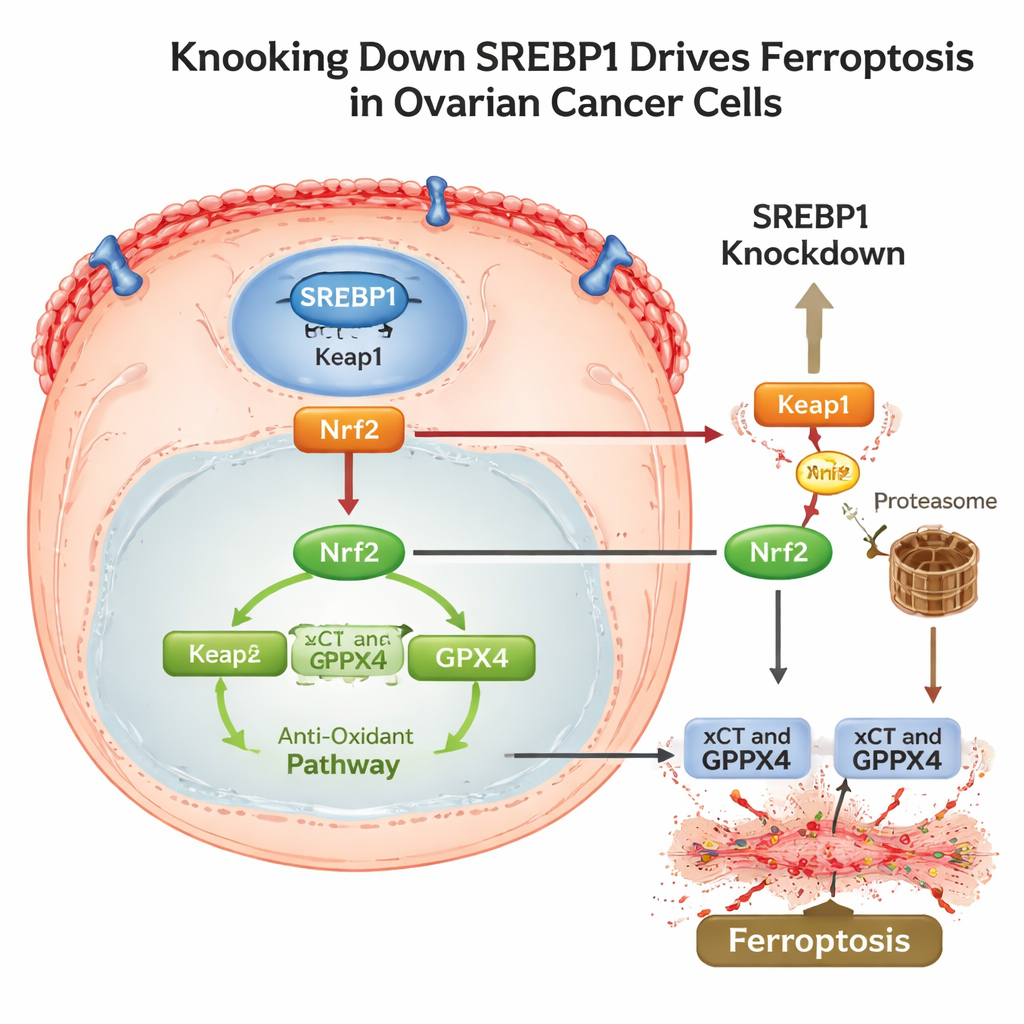
Обезвреживание антиоксидантного щита клетки и приёмов уклонения
Чтобы понять, как SREBP1 связан с этой программой гибели, учёные проследили путь через другой крупный белок ответа на стресс — Nrf2. В норме Nrf2 помогает клеткам выживать, включив транскрипцию генов антиоксидантной защиты, включая xCT и GPX4. Исследование показало, что снижение SREBP1 повышало уровни Keap1 — белка, помечающего Nrf2 для разрушения, что приводило к усиленному распаду Nrf2 и меньшему его поступлению в ядро. По мере падения Nrf2 ослабевали его нисходящие защитные механизмы, и возникал ферроптоз. Важно, что опухоли с высоким уровнем SREBP1 также демонстрировали повышенный уровень PD‑L1 — поверхностного белка, помогающего раковым клеткам скрываться от атакующих T‑лимфоцитов. При подавлении SREBP1 в мышиных моделях опухоли росли медленнее, демонстрировали больше признаков липидного повреждения, меньше Nrf2 и GPX4, а также сниженный PD‑L1 и повышенную иммунную активность.
Почему это важно для будущих методов лечения
Проще говоря, опухоли яичников используют SREBP1 как двусторонний инструмент выживания: он питает их рост, усиливая синтез липидов, и одновременно обеспечивает антиоксидантную защиту и иммунную маскировку. Эта работа показывает, что выключение SREBP1 может лишить опухоль липидов, снять её защиту от железо‑опосредованного повреждения и уменьшить способность уклоняться от иммунной атаки. Всё это делает SREBP1 привлекательной мишенью для новых препаратов и указывает на то, что сочетание ингибиторов SREBP1 с лечением, запускающим ферроптоз или активирующим иммунную систему, может предоставить пациентам более эффективный и продолжительный контроль над заболеванием.
Цитирование: Nie, R., Zhou, H., Chen, L. et al. SREBP1 knockdown triggers ferroptosis by suppressing the Nrf2-XCT/GPX4 axis in ovarian cancer. Cell Death Discov. 12, 101 (2026). https://doi.org/10.1038/s41420-026-02964-9
Ключевые слова: рак яичников, липидный метаболизм, ферроптоз, SREBP1, опухолевая иммунность