Clear Sky Science · ru
PDHA1 повышает устойчивость к ферроптозу у клеток предстательной железы, устойчивых к анойкису, за счёт повышения экспрессии AIFM2
Почему некоторые клетки рака простаты отказываются умирать
Когда раковые клетки отрываются от опухоли и попадают в кровоток, большинство из них должно погибнуть до того, как они достигнут нового органа. Тем не менее опасное меньшинство выживает, перемещается и посевает метастазы, которые часто бывают смертельными. В этом исследовании поставлен ключевой вопрос: что позволяет отдельным клеткам рака простаты сопротивляться форме клеточной гибели, которая обычно наступает при утрате контакта с родной тканью? Выявив спрятанную цепь выживания внутри таких клеток, работа указывает на новые способы блокировать метастазирование у его истоков.
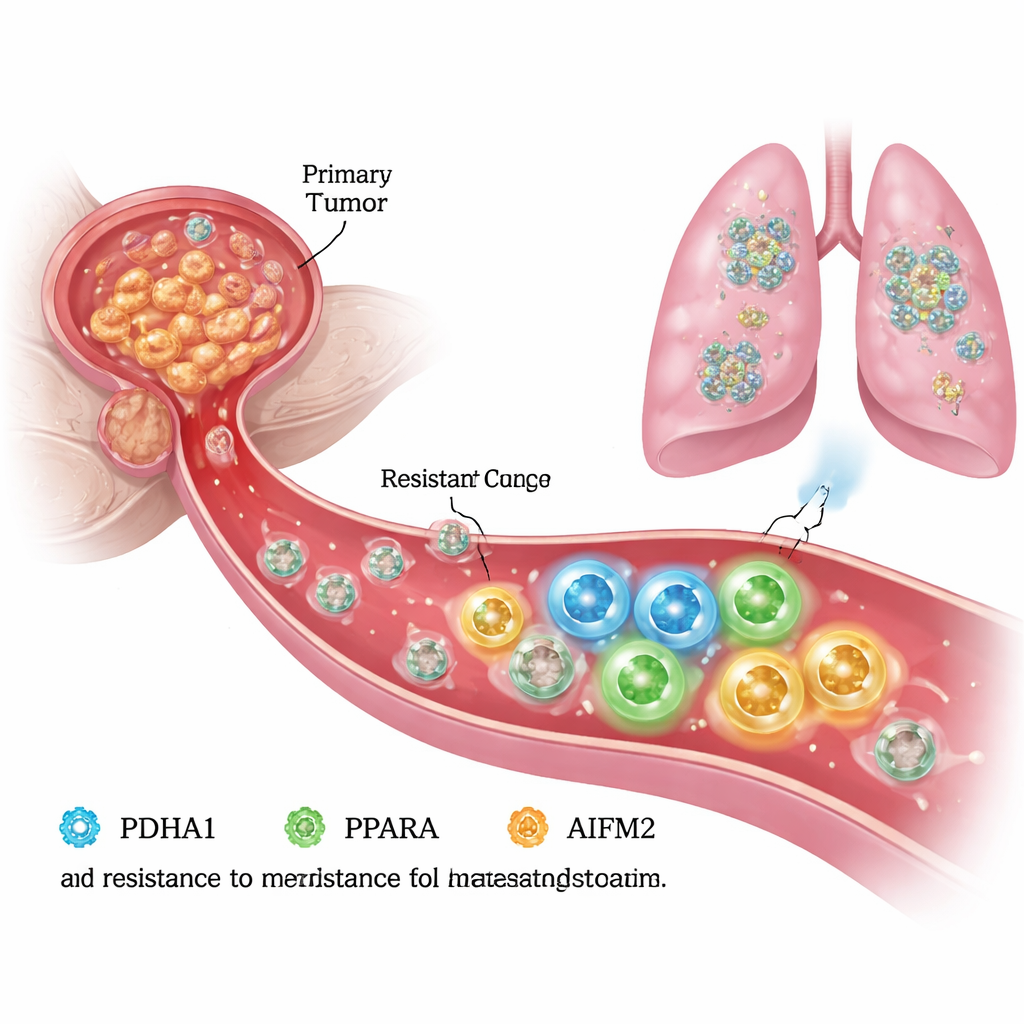
Ускользая от смерти в кровотоке
Чтобы распространяться, клетки рака простаты должны выдержать существование без поддержки окружающей ткани, называемой внеклеточным матриксом. В условиях «отсоединения» здоровые клетки проходят программируемую гибель, называемую анойкисом, и многие раковые клетки также уязвимы к связанному процессу железозависимой гибели — ферроптозу. Авторы получили в лаборатории клетки рака простаты, устойчивые к анойкису, и сравнили их с исходными «родительскими» клетками. Они обнаружили, что устойчивые клетки не только чаще мигрировали и внедрялись, но и лучше выживали при отсоединении, что указывает на перенастройку их внутренней машины, позволяющую избегать ферроптоза и продолжать рост.
Метаболический переключатель с дополнительной функцией
Глубже изучив механизм, группа сосредоточилась на метаболическом ферменте PDHA1, наиболее известном тем, что помогает превращать пировиноградную кислоту, образующуюся при расщеплении сахаров, в ацетил‑КоА в митохондриях, питая производство энергии. В клетках, устойчивых к анойкису, уровни и активность PDHA1 были заметно повышены, а в образцах пациентов обнаруживали больше PDHA1 в первичных опухолях у мужчин, у которых рак простаты метастазировал в лимфатические узлы или отдалённые органы. При снижении PDHA1 устойчивые клетки теряли большую часть способности к миграции, инвазии и выживанию. Удивительно, что значительная часть PDHA1 в этих клетках больше не была ограничена митохондриями; она переместилась в ядро, где ДНК упакована с гистонами, которые могут химически модифицироваться для включения или выключения генов.
Переписывание активности генов для блокировки ферроптоза
В ядре PDHA1, по-видимому, питал локальное производство ацетил‑КоА — ключевого субстрата для ацетилирования гистонов. Авторы показали, что ядерный PDHA1 усиливал конкретную метку — ацетилирование H3K9 — в регуляторной области гена PPARA. Это изменение действовало как ослабление «бобин» хроматина, облегчая включение PPARA. PPARA, в свою очередь, выступал как главный переключатель, увеличивая синтез белка AIFM2 за счёт связывания с его промотором и повышения транскрипции. Таким образом, PDHA1 не воздействовал напрямую на ген AIFM2, а действовал через PPARA, устанавливая многоступенчатый путь от изменённого метаболизма к изменённой регуляции генов.
Построение щита против железозависимого разрушения
AIFM2 известен как внутренний тормоз ферроптоза: он помогает защищать липиды в мембранах клеток от разрушительного окисления. В клетках рака простаты, устойчивых к анойкису, повышение PDHA1 приводило к увеличению уровней AIFM2, тогда как уменьшение PDHA1 снижало их. Функциональные тесты показали, что снижение PDHA1 усиливало признаки ферроптоза — больше реактивных форм кислорода, больше повреждений липидов, пониженный потенциал мембраны митохондрий и характерное усыхание митохондрий — особенно при обработке клеток индуктором ферроптоза эрастином. Переэкспрессия AIFM2 обращала эти эффекты, спасая выживание в культуре и восстанавливая метастазирование в лёгких у мышей, даже при подавлении PDHA1. Это подтвердило, что AIFM2 является критическим нисходящим эффектором в пути PDHA1‑опосредованной устойчивости к ферроптозу.
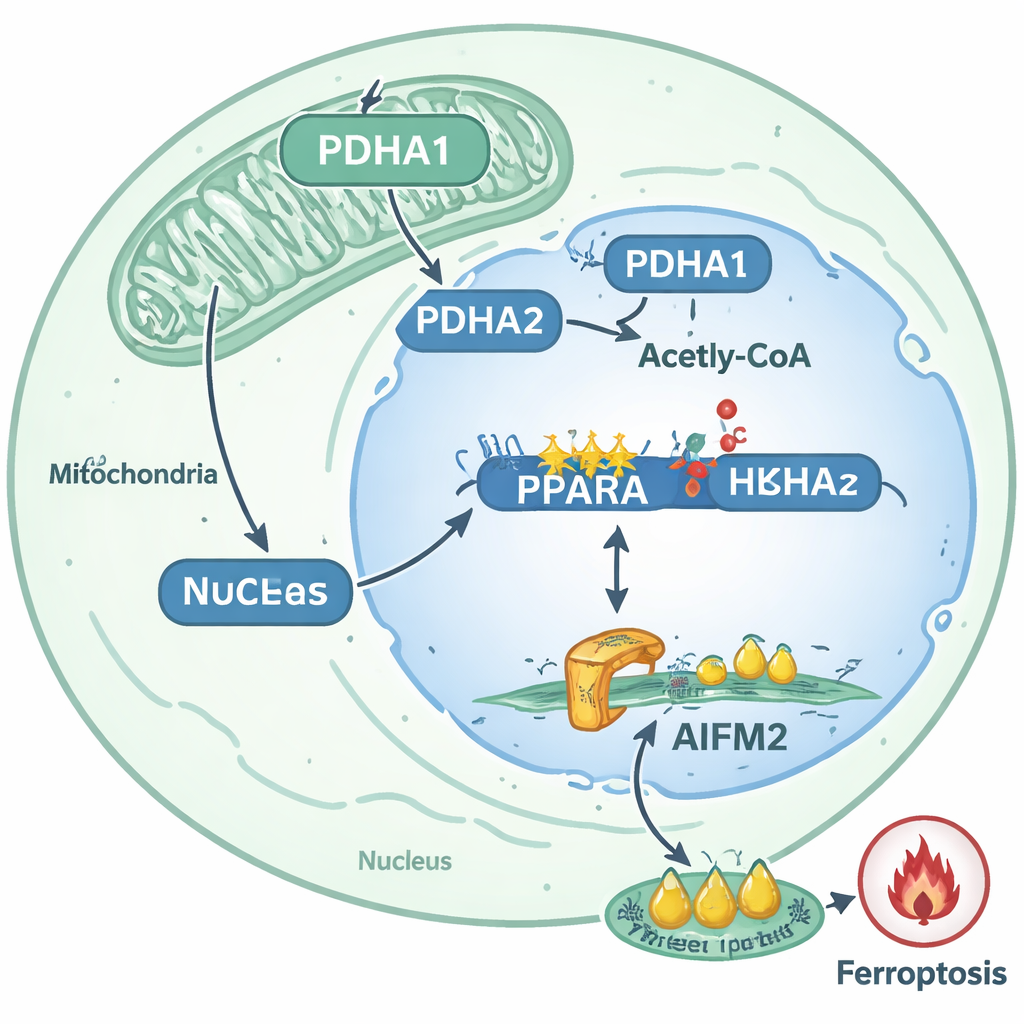
От молекулярной схемы к идеям лечения
Сопоставив эти события, исследование описывает ясный путь, по которому отсоединённые клетки рака простаты становятся труднее убиваемыми: PDHA1 перемещается в ядро, увеличивает ацетилирование гистонов в гене PPARA, усиливает активность PPARA и тем самым повышает уровни AIFM2, блокируя ферроптоз. Этот путь тесно связан с метастатическим поведением в опухолях пациентов и в моделях на животных. Для неспециалистов ключевая мысль такова: некоторые раковые клетки перенаправляют стандартный метаболический фермент в эпигенетический инструмент, который перепрограммирует активность генов и выстраивает биохимический щит против мощной формы клеточной гибели. Авторы предполагают, что препараты, нацеленные на PDHA1, PPARA или AIFM2, — или терапии, целенаправленно индуцирующие ферроптоз — могли бы в будущем сочетаться, чтобы лишить метастатические клетки рака простаты этого преимущества выживания и сделать их гораздо более уязвимыми в самый критический момент их пути: при переходе от одного органа к другому.
Цитирование: Cong, Y., Chen, K., Ju, Y. et al. PDHA1 enhances resistance to ferroptosis in anoikis-resistant prostate cancer by upregulating AIFM2. Cell Death Discov. 12, 105 (2026). https://doi.org/10.1038/s41420-026-02958-7
Ключевые слова: метастазирование рака простаты, ферроптоз, устойчивость к анойкису, PDHA1, AIFM2