Clear Sky Science · ru
Модуляция метаболических сигнатур для ослабления резистентности к кабозантинибу в моделях острой миелоидной лейкемии с FLT3‑ITD
Почему это важно для лечения рака
Многие современные противораковые препараты разработаны для нацеливания на одну дефектную белковую мишень в опухолевых клетках. Эти таргетные препараты могут вызывать впечатляющие ремиссии, но опухоли часто находят способы приспособиться и возобновить рост. В этой статье исследуется, как один тип гемобластоза — острая миелоидная лейкемия (ОМЛ) — развивается резистентностью к одному из таких таргетных препаратов, кабозантинибу, и как перенастройка энергетического обмена клеток может помочь врачам обойти эту устойчивость.
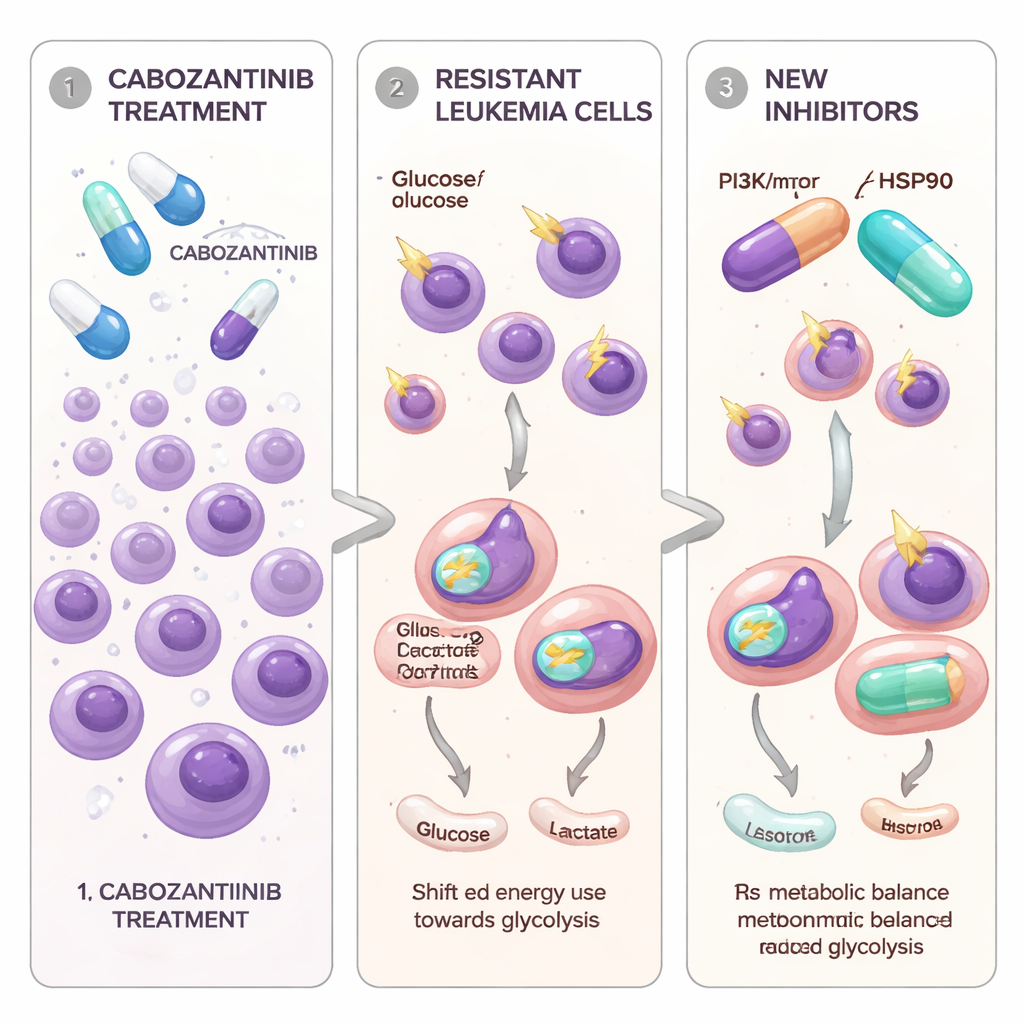
Лейкозные клетки, научившиеся уворачиваться от таргетного препарата
Исследователи сосредоточились на клетках ОМЛ с мутацией в переключателе сигнала роста FLT3‑ITD, которая известна как фактор особенно агрессивного течения болезни. Кабозантиниб — пероральный препарат, уже применяемый при некоторых солидных опухолях — в лаборатории может сильно блокировать клетки лейкемии, управляемые FLT3. Чтобы смоделировать происходящее у пациентов с течением времени, команда постепенно подвергала две линии клеток ОМЛ с мутацией FLT3 возрастающим дозам кабозантиниба, пока некоторые клетки не выживали и вновь не начинали расти. Эти новые популяции клеток, названные Molm13‑XR и MV4‑11‑XR, могли переносить концентрации кабозанитиниба во много раз выше, чем их исходные «родительские» клетки. Они также стали менее чувствительны к двум другим одобренным препаратам, нацеленным на FLT3 — сорафенибу и квизартинибу, — оставаясь при этом уязвимыми для другого ингибитора, гilteritinib.
Генетические изменения, помогающие раку выживать
Изучая изменения на генетическом уровне, учёные обнаружили, что у этих устойчивых к препарату клеток лейкемии появились новые варианты гена FLT3. Обе резистентные линии приобрели одинаковую точечную мутацию D835Y в критической области киназного домена FLT3 — известном «горячем» участке, связанном с резистентностью к нескольким препаратам. В одной из линий, MV4‑11‑XR, также выявлена необычная делеция размером 1,3 килобазы, удалившая целый экзон FLT3 и стершая часть домена, важного для связывания лекарств. Эти изменения, по-видимому, отбирались в процессе длительного воздействия кабозанитиниба: мутантные версии FLT3 стали значительно более распространёнными в резистентных клетках, чем в исходной популяции. Одновременно ключевые сигнальные пути вниз по каскаду FLT3 — такие как ERK, STAT5 и AKT — были более активно включены, что способствовало более быстрому росту и повышенной колониеобразующей способности резистентных клеток.
Клетки рака переключают системы питания
Затем команда спросила, связана ли резистентность не только с генетикой, но и с тем, как клетки получают энергию. С помощью РНК‑секвенирования и специализированных метаболических тестов они выявили устойчивый паттерн: клетки, резистентные к кабозантинибу, гораздо больше полагаются на гликолиз — быстрый распад глюкозы в цитоплазме — даже при достаточном уровне кислорода. Эти клетки поглощали больше глюкозы, вырабатывали больше лактата, демонстрировали повышенную активность ключевого фермента GAPDH и усиливали экспрессию нескольких генов, связанных с гликолизом. В то же время митохондрии — структуры, обеспечивающие более эффективное производство энергии — были менее активны и менее многочисленны. Измерения потребления кислорода показали снижение как базального, так и пикового митохондриального дыхания, а внутриклеточные уровни реактивных форм кислорода были повышены, что указывает на стресс и пониженную эффективность митохондрий.
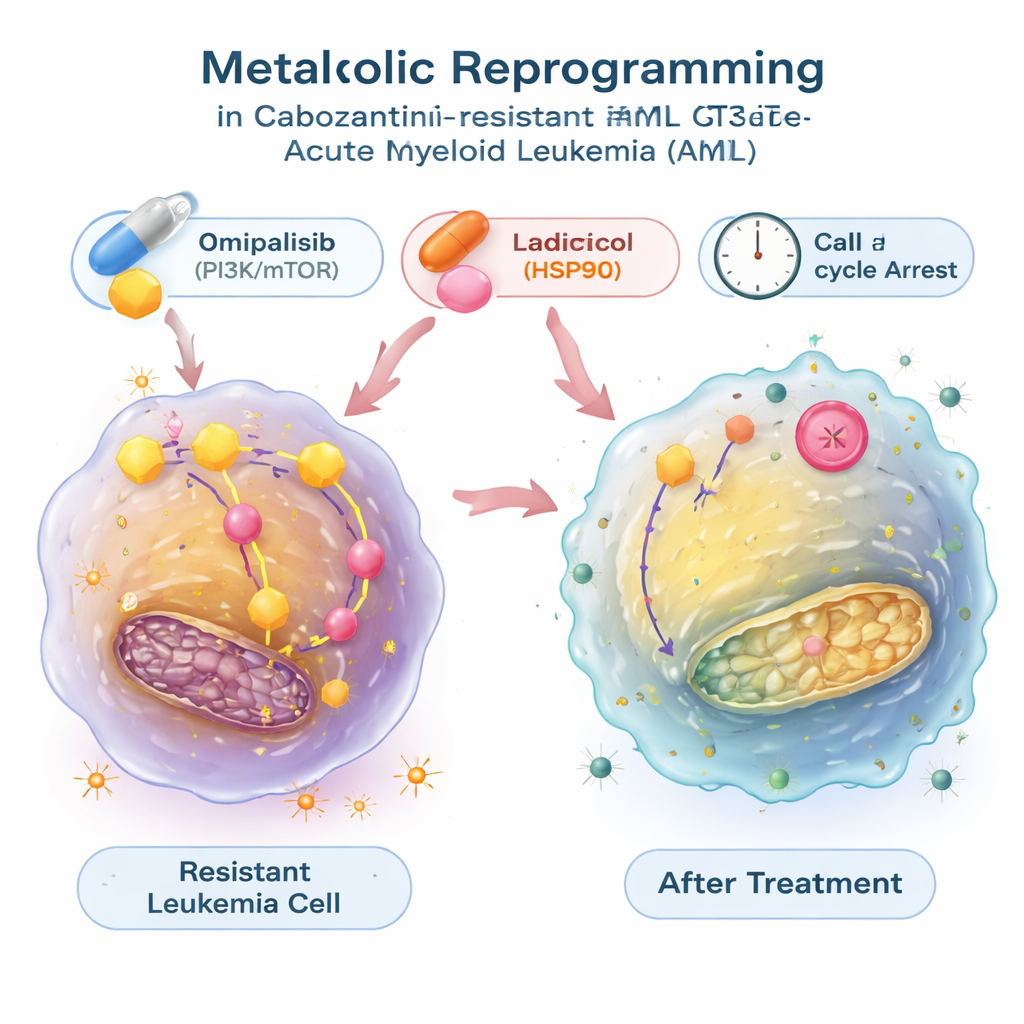
Поиск препаратов, которые возвращают метаболический переключатель
Чтобы выяснить, можно ли обратить этот энергетический сдвиг, исследователи использовали большую публичную базу данных, связывающую паттерны экспрессии генов с эффектами тысяч соединений. Они искали препараты, предсказанные как способные противодействовать метаболической сигнатуре резистентных клеток лейкемии, и сосредоточили внимание на двух из них: радицоколе, который блокирует шаперонный белок HSP90, и омипалисибе, ингибиторе сигнального пути PI3K/mTOR, контролирующего рост и метаболизм. В лабораторных тестах оба соединения не только замедляли рост резистентных клеток, но и снижали их гиперактивный гликолиз, нормализуя поглощение глюкозы и выделение лактата и уменьшая экспрессию генов, связанных с гликолизом. Эти препараты переводили клетки лейкемии в постмитотическую фазу клеточного цикла, а радицокол дополнительно вызывал значительную программируемую клеточную гибель. В комбинации с кабозантинибом омипалисиб — и в одной модели радицокол — действовали синергически, делая резистентные клетки более уязвимыми для уничтожения.
Что это значит для будущих терапий лейкемии
Для неспециалистов ключевая мысль в том, что клетки лейкемии могут уйти от действия таргетного препарата не только путём мутаций его прямой мишени, но и изменяя способы производства и использования энергии. Исследование показывает, что клетки ОМЛ, устойчивые к кабозантинибу, переходят на «сахаросжигающую» стратегию, в то время как их митохондрии ослабляются. Удар по путям, поддерживающим такую перенастройку метаболизма — например, с помощью омипалисиба или ингибиторов HSP90 — может позволить восстановить чувствительность к кабозантинибу и похожим препаратам. Хотя эти выводы получены на моделях клеток, а не у пациентов, они предполагают, что сочетание таргетной терапии с агентами, модифицирующими метаболизм, может стать перспективным подходом для замедления или преодоления резистентности при ОМЛ с мутацией FLT3.
Цитирование: Fu, YH., Ng, K.M., Tseng, CY. et al. Modulating metabolic signatures to mitigate cabozantinib resistance in FLT3-ITD acute myeloid leukemia cell models. Cell Death Discov. 12, 98 (2026). https://doi.org/10.1038/s41420-026-02957-8
Ключевые слова: острая миелоидная лейкемия, устойчивость к лекарствам, мутация FLT3, метаболизм рака, кабозантиниб