Clear Sky Science · ru
ДНК-полимераза каппа, стабилизированная Ptbp2, взаимодействует с MRE11 и способствует геномной нестабильности при лейкемии
Как клетки лейкемии сохраняют разорванную ДНК и при этом выживают
Наша ДНК постоянно подвергается атакам, однако здоровые клетки обычно очень хорошо обнаруживают и исправляют повреждения. В лейкемии же некоторые клетки учатся жить с разорванной, нестабильной ДНК — и даже превращают эту нестабильность в преимущество для выживания. В этом исследовании описано молекулярное «сотрудничество» между белком сплайсинга (Ptbp2), специальным ферментом копирования ДНК (ДНК-полимераза каппа, или Polk) и фактором распознавания повреждений (MRE11), которое помогает клеткам лейкемии восстанавливать ровно столько повреждений, чтобы остаться в живых, одновременно накапливая генетический хаос, ускоряющий прогрессирование рака.
Скрытый помощник в клетках лейкемии
Исследователи сосредоточились на хроническом миелоидном лейкозе (ХМЛ), кровяном раке, обычно инициируемом фузией гена BCR::ABL1. Хотя современные препараты, блокирующие BCR::ABL1, эффективны на ранних стадиях болезни, многие пациенты в агрессивной фазе «бластного криза» отвечают на лечение плохо. Предыдущие работы показали, что Ptbp2 — белок, связывающий РНК и влияющий на обработку сообщений — усиливается под действием BCR::ABL1 и действует как онкоген при ХМЛ. В этой работе команда обнаружила, что Ptbp2 прикрепляется к хвостовой части (3′ UTR) мРНК Polk и защищает её от деградации. В результате при высоком уровне Ptbp2 клетки лейкемии синтезируют больше белка Polk.
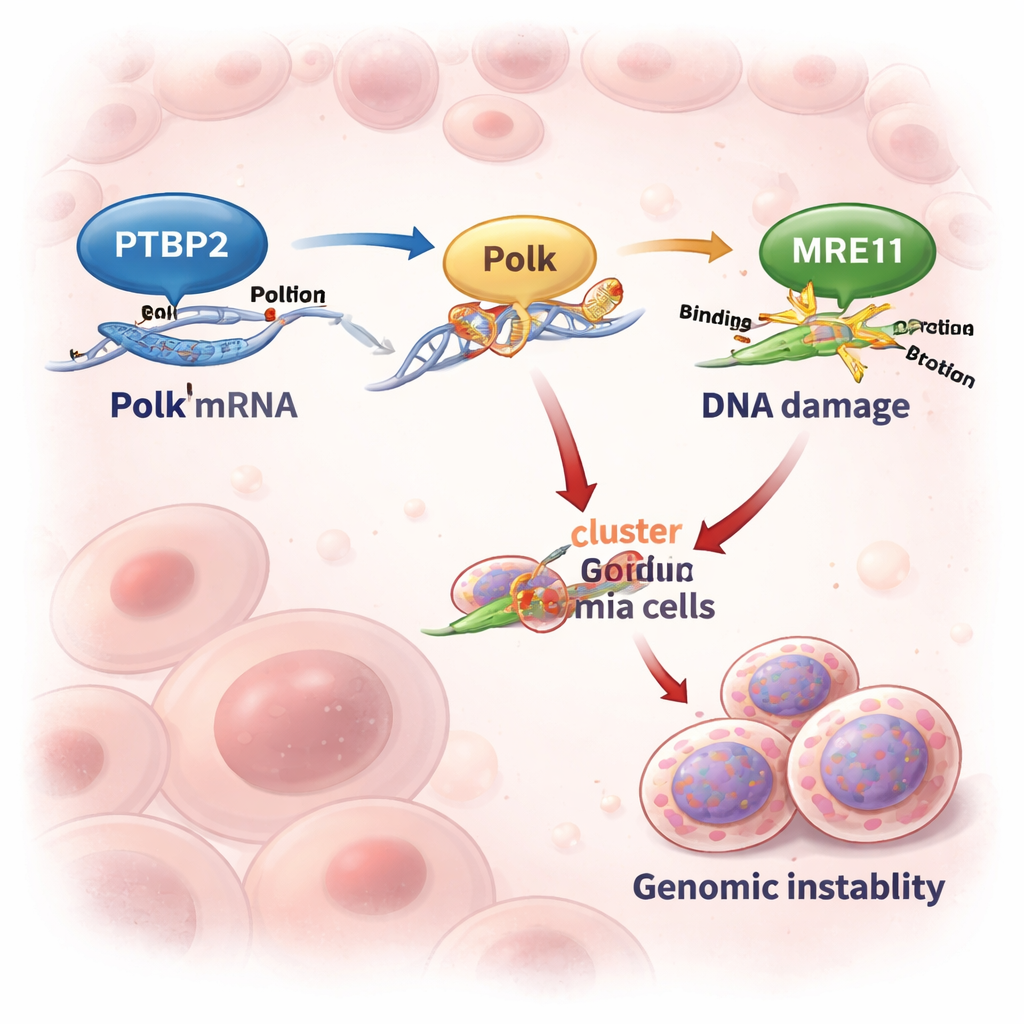
Включение неточной копировальной машины ДНК
Polk — это «резервная» ДНК-полимераза, способная копировать поврежденную ДНК, когда обычный репликативный аппарат останавливается. Эта способность может спасать клетки под стрессом — но ценой служит то, что Polk делает ошибки и способен вносить мутации. В клеточных линиях и образцах пациентов с продвинутым ХМЛ уровни Ptbp2 и Polk растут и падают синхронно. Когда учёные инактивировали Ptbp2 в клетках лейкемии, уровни Polk резко снижались, а мРНК Polk деградировала почти в два раза быстрее. Повторное введение Polk в клетки, лишённые Ptbp2, восстановило их поведение, что показало: основная роль Ptbp2 здесь — поддерживать высокий уровень и активность Polk.
Ремонт повреждений — но не идеально
Чтобы выяснить, как этот дуэт влияет на репарацию ДНК, исследователи обрабатывали клетки гидроксивурецилом, препаратом, который останавливает репликацию ДНК и часто используется при ХМЛ. Клетки без Ptbp2 испытывали значительно больше повреждений ДНК, что проявлялось длинными «хвостами кометы» и яркими очагами γH2AX — признаками разорванных хромосом. Такие повреждённые клетки чаще погибали. Напротив, клетки с высоким уровнем Ptbp2 и Polk лучше переносили препарат, более эффективно восстанавливали повреждения и выживали, хотя их восстановление было неаккуратным. Переэкспрессия Polk в клетках с нокаутом Ptbp2 вернула прежнюю устойчивость, подтвердив, что партнёрство Ptbp2–Polk помогает клеткам лейкемии пережить стресс репликации и избежать апоптоза.
Сеть повреждений ДНК, благоприятствующая нестабильности
На этом история с Polk не заканчивается. Команда показала, что Polk физически взаимодействует с MRE11 — ключевым участником комплекса MRN, распознающего разрывы ДНК и активирующего путь ответа на повреждение ATM–CHK2. При удалении Ptbp2 уровни Polk снижались, активность и уровни MRE11 падали, и сигнализация ATM–CHK2 ослабевала. Восстановление Polk возвращало MRE11 и его активацию. Детальные эксперименты с ДНК-волокнами показали, что Ptbp2 и Polk помогают защищать остановленные вилки репликации от укорочения, во многом посредством MRE11. Блокирование MRE11 препаратом подрывало эту защиту вилок и усиливало повреждения ДНК. Парадоксально, но при активной сигнализации Ptbp2–Polk–MRE11 клетки накапливали больше хромосомных аномалий — таких как обмен сестринских хроматид, разрывы, щели, многополярные веретена и многоядерные гигантские клетки — классические признаки геномной нестабильности, способные подпитывать более агрессивное течение болезни.
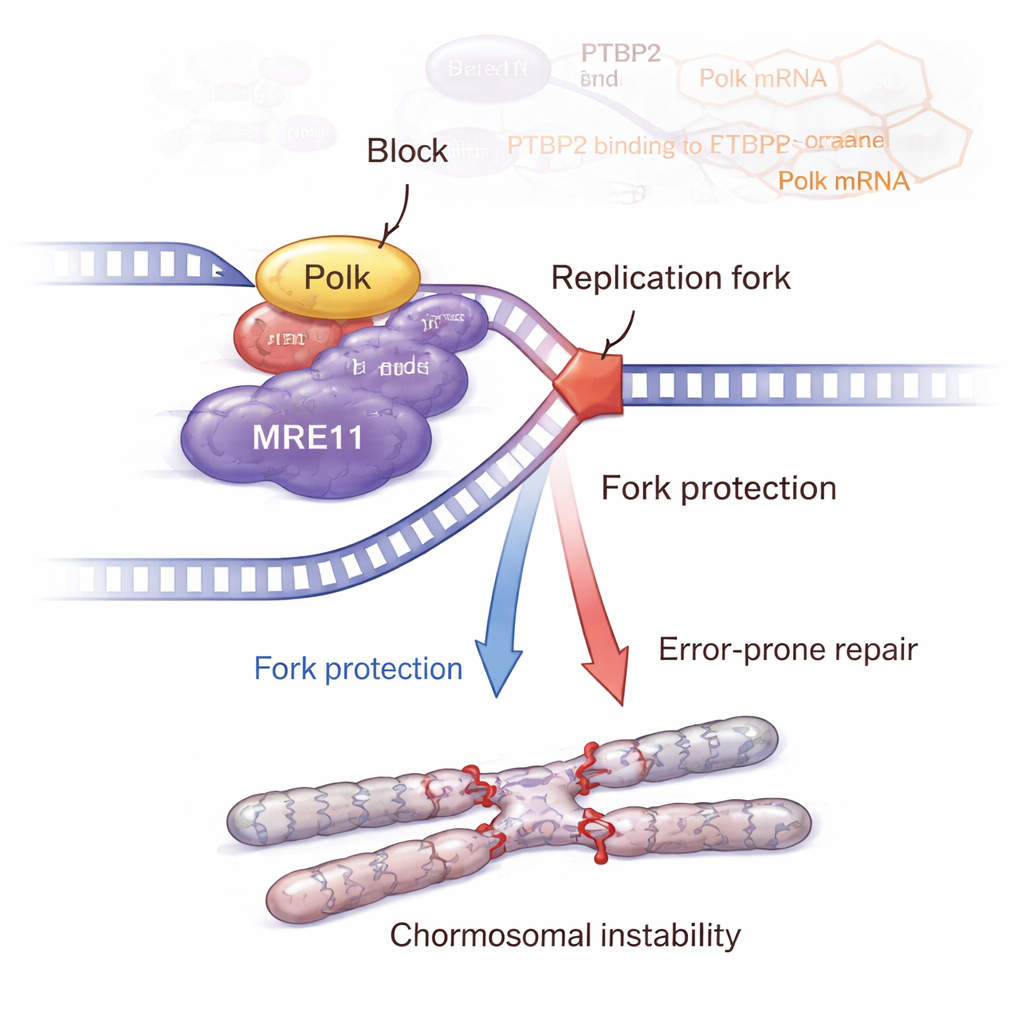
От мышей к потенциально новым методам лечения
В модельных исследованиях на мышах клетки лейкемии с интактным Ptbp2 формировали более крупные и более аномальные опухоли, чем клетки без Ptbp2. Ткани этих животных демонстрировали повышенные уровни Ptbp2, Polk, маркера пролиферации Ki-67 и искажённые структуры деления клеток. В отдельной модели, похожей на ХМЛ и индуцируемой BCR::ABL1, добавление лишнего Ptbp2 усиливало Polk и увеличивало число атипично делящихся клеток и инвазивных скоплений лейкемии в селезёнке и печени, указывая на более быстрое прогрессирование болезни. В совокупности эти данные свидетельствуют о том, что ось Ptbp2–Polk–MRE11–ATM–CHK2 позволяет клеткам лейкемии выживать при сильном ДНК-стрессе, одновременно постепенно накапливая вредные мутации.
Почему это важно для пациентов
Для не-специалиста ключевой вывод таков: некоторые клетки лейкемии избегают контроля, балансируя на тонкой грани — они восстанавливают ДНК достаточно, чтобы выжить, но не настолько хорошо, чтобы избежать мутаций. Ptbp2 стабилизирует Polk, который затем взаимодействует с MRE11, защищая стрессовую ДНК и поддерживая сигналы о повреждении — однако этот ремонт несовершенен и способствует генетическому хаосу. Поскольку продвинутые стадии ХМЛ и другие раки, по-видимому, зависят от этого хрупкого равновесия, нацеливание на Ptbp2 или его контроль над Polk может склонить клетки от выживания к самоуничтожению и предложить многообещающий новый подход для терапии, особенно в трудно лечимой стадии бластного криза.
Цитирование: Lama, S., Barik, B., IS, S. et al. DNA polymerase kappa stabilized by Ptbp2 interacts with MRE11 and promotes genomic instability in leukemia. Cell Death Discov. 12, 96 (2026). https://doi.org/10.1038/s41420-026-02951-0
Ключевые слова: хронический миелоидный лейкоз, геномная нестабильность, репарация ДНК, ДНК-полимераза каппа, PTBP2