Clear Sky Science · ru
Раскрывая уязвимости глиомы: нацеливание на пути регулируемой гибели клеток для инновационных терапий
Почему гибель клеток при опухолях мозга имеет значение
Глиомы — одни из самых частых и смертельных опухолей мозга у взрослых. Даже при применении хирургии, лучевой терапии и химиотерапии они часто рецидивируют и трудно поддаются контролю. В этом обзорном материале рассмотрен новый подход: использование различных запрограммированных путей гибели клеток. Понимая и направляя эти «самоуничтожающие» маршруты, исследователи надеются выявить слабые места глиомных клеток и сделать будущие методы лечения более эффективными и персонализированными.
Как глиомы перехитривают стандартную терапию
Глиомы развиваются из вспомогательных клеток мозга и варьируют от медленно растущих форм до высокоагрессивной глиобластомы. Плохие прогнозы обусловлены несколькими взаимосвязанными проблемами: генетическими мутациями, эпигенетическими изменениями, трудноубиваемыми стволоподобными клетками, аномальным кровоснабжением и сильно подавляющей иммунной средой. К тому же гематоэнцефалический барьер ограничивает проникновение лекарств в опухоль. В совокупности эти факторы позволяют опухолевым клеткам выживать после операции и стандартных препаратов, адаптироваться к стрессу и в конечном счёте восстановиться. 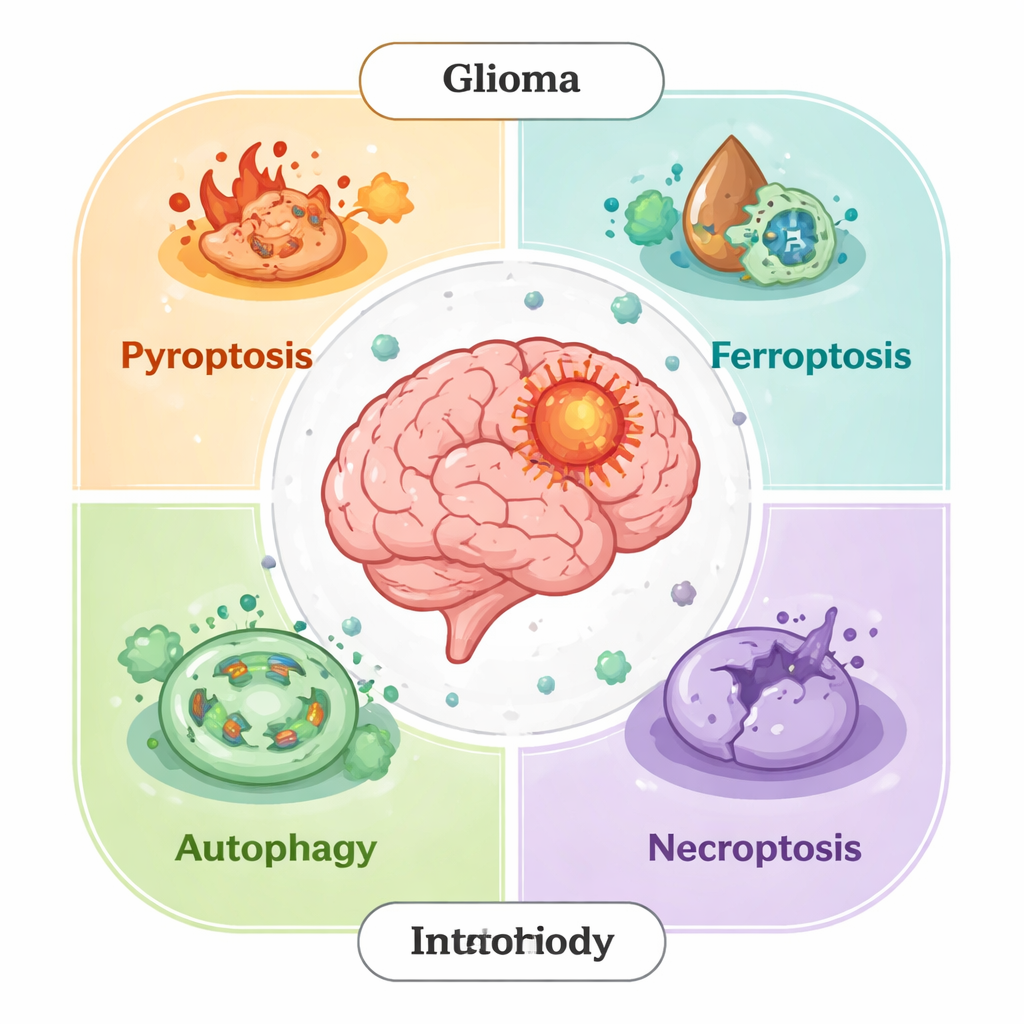
Многообразие форм самоуничтожения клеток
Долгое время учёные сосредотачивались на одном основном виде запрограммированной гибели — апоптозе. Сейчас мы знаем, что это лишь часть картины. Клетки глиомы могут также погибать по другим регулируемым путям: пироптозу (воспалительный «всплеск» с раздуванием и разрывом), ферроптозу (повреждение мембран, вызванное железом), некроптозу (контролируемая форма разрыва клеток) и гибели, зависящей от аутофагии (самопереваривание, выходящее за пределы выживаемости). В здоровых тканях эти процессы удаляют повреждённые клетки и предотвращают развитие рака. В опухолях же глиомные клетки часто перенастраивают эти пути — блокируют сигналы смерти, укрепляют антиоксидантную защиту или превращают аутофагию в механизм выживания — чтобы противостоять лечению и формировать микроокружение, благоприятное для их роста.
Преобразование путей гибели в терапию
Вместо того чтобы рассматривать эти пути как проблему, исследователи учатся использовать их в качестве оружия. Стратегии, индуцирующие пироптоз, применяют «умные» наночастицы, термостимуляцию светом, генетически модифицированные вирусы или гидрогели с лекарствами, заставляющие глиомные клетки набухать, разрываться и выделять сигналы опасности, привлекающие иммунитет. Подходы на основе ферроптоза заставляют опухоль войти в железозависимый коллапс, блокируя ключевые защитные ферменты вроде GPX4, нарушая синтез глутатиона или изменяя метаболизм липидов в клетке. Многие из этих тактик доставляются с помощью передовых носителей, включая графдиин и другие наночастицы, чтобы помочь препаратам преодолеть гематоэнцефалический барьер и концентрироваться в опухоли, минимально затрагивая здоровую ткань мозга. 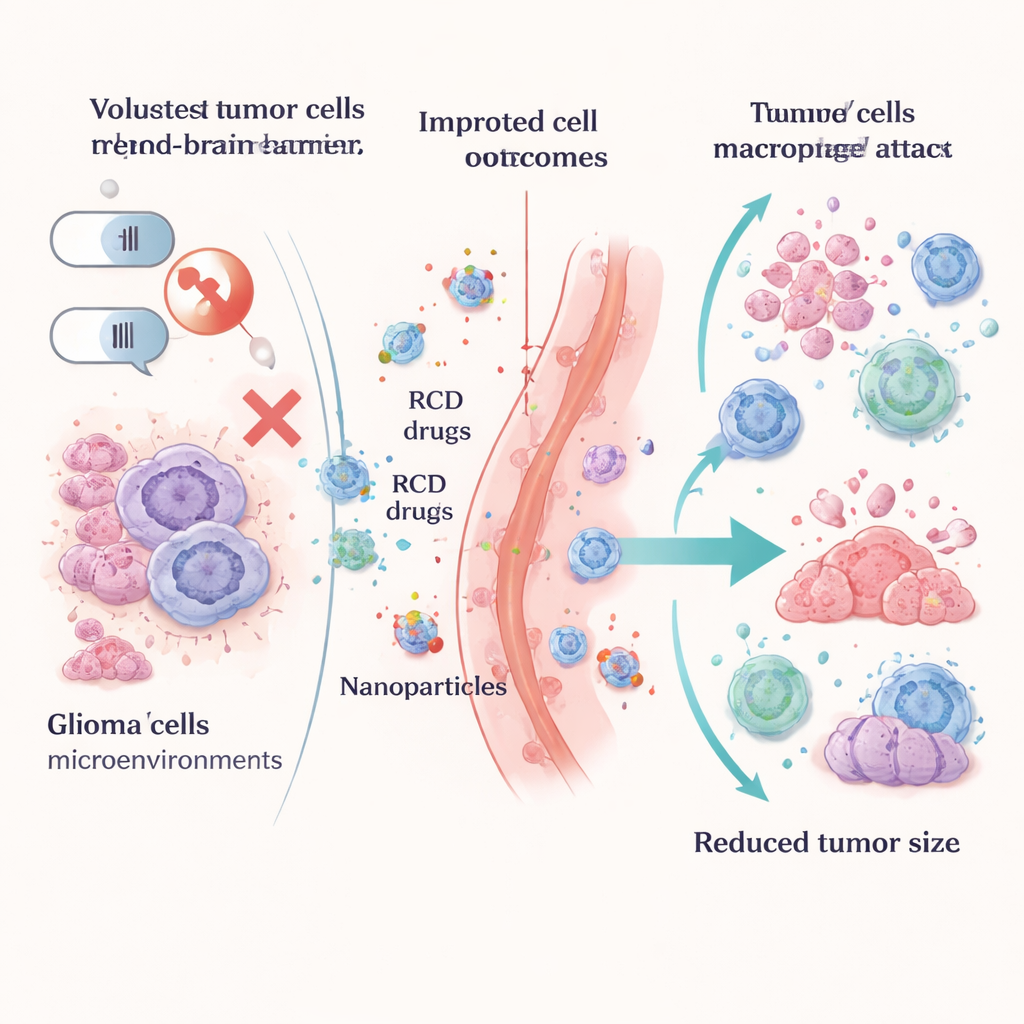
Перезагрузка иммунного ландшафта опухоли
Терапии, нацеленные на некроптоз, призваны преодолеть устойчивость клеток, утративших ответ на стандартные сигналы гибели. Натуральные соединения, такие как шиконин, эмодин и производные целастрола, могут направлять глиомные клетки в некроптоз, что не только убивает их, но и высвобождает молекулы, привлекающие иммунные клетки в опухоль. Параллельно учёные изучают аутофагию: иногда её блокируют, чтобы помешать опухолевым клеткам пережидать лучевую и химиотерапию с помощью «самоочистки», а иногда усиливают, доводя процесс до гибели клетки. Ранние клинические испытания таких препаратов, как хлорохин и гидроксихлорохин, показывают, что модуляция аутофагии у пациентов возможна и безопасна, хотя явных преимуществ по выживаемости пока не продемонстрирована.
От лабораторных открытий к персонализированной помощи
Трансляция этих идей в реальные терапии остаётся сложной задачей. Глиомы сильно вариабельны между пациентами и внутри одной опухоли, поэтому одна стратегия гибели не подойдёт всем. Гематоэнцефалический барьер по-прежнему ограничивает доставку лекарств, а иммунное микроокружение может ослаблять даже продуманные комбинации терапии. Авторы выделяют перспективные направления: сочетание индукторов ферроптоза с ингибиторами иммунных контрольных точек, комбинирование онколитических вирусов с препаратами, усиливающими сигналы «съешь меня» в раковых клетках, или добавление модуляторов аутофагии в выбранные схемы химио- и лучевой терапии. Мультиомные профилирования и более точные биомаркеры должны помочь выявлять пациентов, которые с наибольшей вероятностью выиграют от конкретных комбинаций стратегий.
Взгляд в будущее: заставить опухоль выбрать самоуничтожение
Проще говоря, статья приходит к выводу, что будущее лечения глиом может заключаться в искусственном провоцировании у опухолевых клеток их собственных «кнопок самоуничтожения» в контролируемом виде. Освоив запуск и координацию пироптоза, ферроптоза, некроптоза и гибели, зависящей от аутофагии — и сочетая эти подходы с современными иммунотерапиями и точной доставкой препаратов — исследователи надеются превратить в настоящее время мрачный диагноз в состояние, с которым можно лучше справляться и, в конечном итоге, лечить более эффективно.
Цитирование: Guo, J., Zong, L., Huang, Y. et al. Unlocking glioma vulnerabilities: targeting regulated cell death pathways for innovative therapies. Cell Death Discov. 12, 95 (2026). https://doi.org/10.1038/s41420-026-02949-8
Ключевые слова: глиома, регулируемая гибель клеток, пироптоз, ферроптоз, терапия глиобластомы