Clear Sky Science · ru
Митофагия при раке поджелудочной: механистические сведения и значение для новых терапевтических стратегий
Почему «электростанции» наших клеток важны при раке поджелудочной
Протоковая аденокарцинома поджелудочной железы — один из самых смертоносных видов рака, отчасти потому, что опухоли быстро вырабатывают устойчивость почти ко всем терапиям. В этой обзорной статье анализируется неожиданный участник истории этой устойчивости: митофагия, встроенная в клетку система распознавания и утилизации изношенных митохондрий — крошечных «электростанций», вырабатывающих энергию. Понимание того, как рак поджелудочной захватывает и перенаправляет этот механизм очистки, может открыть новые пути к более эффективным и долговременным методам лечения.
Клеточные бригады уборки и трюки выживания рака
Митохондрии выполняют гораздо больше функций, чем просто генерируют энергию: они управляют метаболизмом, программируемой гибелью клеток и обезвреживанием реактивных форм кислорода. Когда митохондрии повреждены или их слишком много, клетки включают митофагию для пометки и удаления дефектных органелл. Это может происходить двумя основными путями. Первый, известный как путь PINK1/Parkin, опирается на сенсор повреждения (PINK1) и фермент-маркер (Parkin), который помечает неисправные митохондрии для уничтожения. Второй задействует рецепторные белки, такие как BNIP3, NIX и FUNDC1, расположенные на поверхности митохондрий, которые напрямую связывают их с аутофагосомами — «мешками» для утилизации, без участия того же пометочного шага. Эти пути часто работают совместно, давая клетке гибкие способы подстраиваться под стресс, например дефицит кислорода или воздействие лекарств. 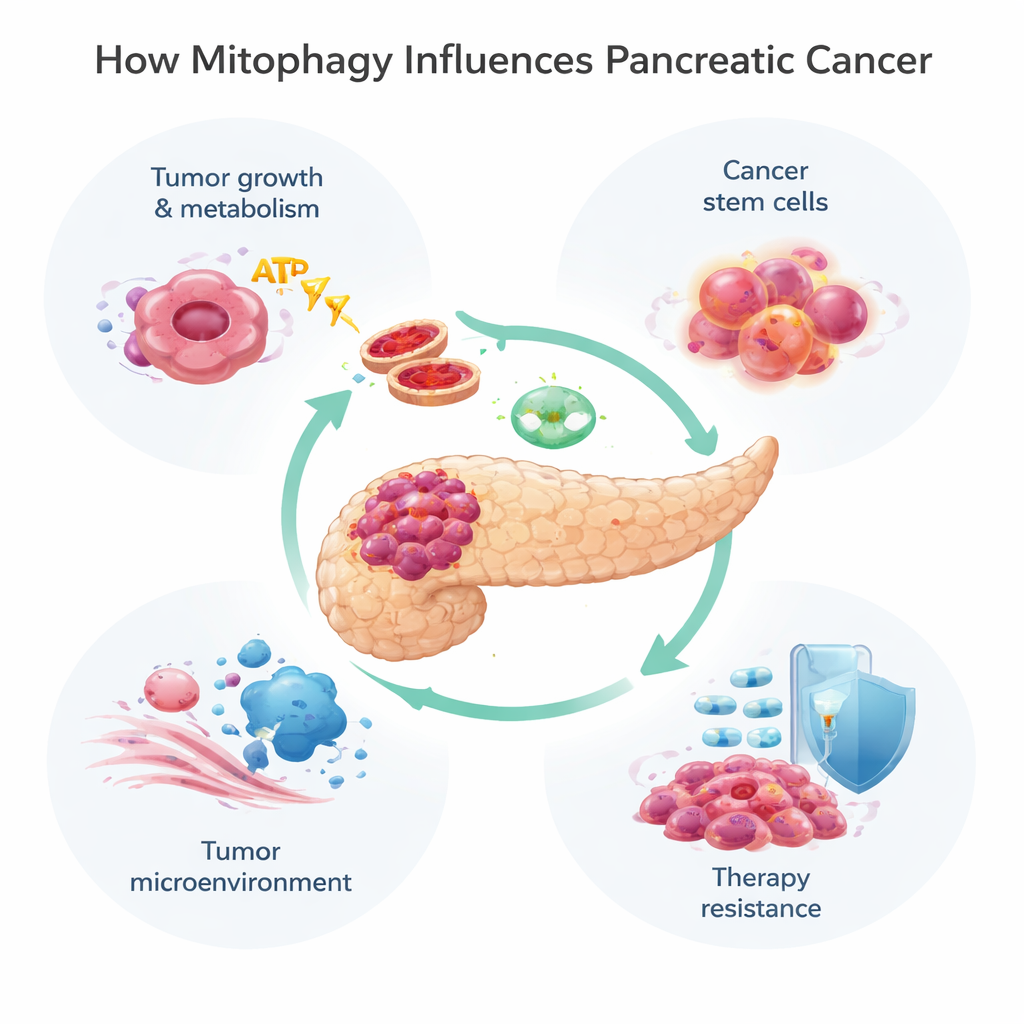
Как опухоли поджелудочной перестраивают использование энергии
Опухоли поджелудочной обитают в суровой среде: они плохо снабжаются кровью и кислородом и окружены плотной рубцовой тканью. Чтобы выжить, раковые клетки перенастраивают свои энергетические системы, часто переходя от кислородозависимого дыхания в митохондриях к более примитивному сжиганию сахаров — гликолизу. Митофагия помогает тонко настраивать этот сдвиг. На ранних стадиях опухолеобразования утрата PINK1 или Parkin ускоряет развитие рака, позволяя накапливаться ионам железа, повышается уровень реактивных форм кислорода и усиливается склонность к гликолизу. Одновременно другой митофагический белок, NIX, может удалять даже функциональные митохондрии, сдвигая клетки в сторону гликолитического метаболизма и ускоренного роста. BNIP3 демонстрирует более сложную картину: он появляется на ранних стадиях, затем во многих прогрессирующих опухолях его подавляют, и восстановление его экспрессии может замедлять рост, что указывает на то, что одни пути митофагии сдерживают рак, а другие — подпитывают его.
Раковые стволовые клетки и окружение опухоли
Не все раковые клетки одинаковы. Небольшая подгруппа, часто называемая раковыми стволовыми клетками, способна к самоподдержанию, образованию новых опухолей и особенно хорошо переносит химиотерапию. В раке поджелудочной эти клетки зависят от митофагии, чтобы оставаться метаболически гибкими. Модифицирующий белок ISG15 поддерживает этот процесс и помогает сохранять стволоподобные свойства, прямо связывая митофагию с рецидивом и провалом лечения. За пределами самих раковых клеток митофагия также формирует микроокружение опухоли — совокупность клеток‑поддержки, иммунных клеток и соединительной ткани вокруг опухоли. Например, фибробласты, связанные с опухолью, могут переходить в состояние «обратного эффекта Варбурга», при котором они усиливают собственную митофагию и гликолиз, а затем снабжают опухоль энергетически богатыми побочными продуктами. Митофагия также влияет на то, как иммунные клетки распознают и атакуют опухоль, изменяя представление иммунных маркеров, таких как MHC‑I, и «тормозов», например PD‑L1, которые опухоль использует, чтобы скрываться.
Почему блокирование или усиление очистки меняет ответ на лекарства
Многие стандартные и экспериментальные терапии при раке поджелудочной, включая химиопрепарат гемцитабин и новый таргетный препарат против распространенной мутации KRAS‑G12D, повреждают митохондрии. Опухолевые клетки часто реагируют включением митофагии, очищая повреждения и избегая гибели. Исследования показывают, что митофагия, управляемая PINK1, может ослаблять убивающее действие химиотерапии и некоторых природных соединений, помогая клеткам выживать. С другой стороны, при определённых условиях чрезмерное стимулирование митофагии — особенно через BNIP3 и NIX — может лишить клетки слишком большого числа функционирующих митохондрий, приведя к энергетическому краху и индукции клеточной гибели. Эта двойственная природа означает, что митофагия может либо защищать опухоли от лечения, либо, при правильном направлении, делать их более уязвимыми. 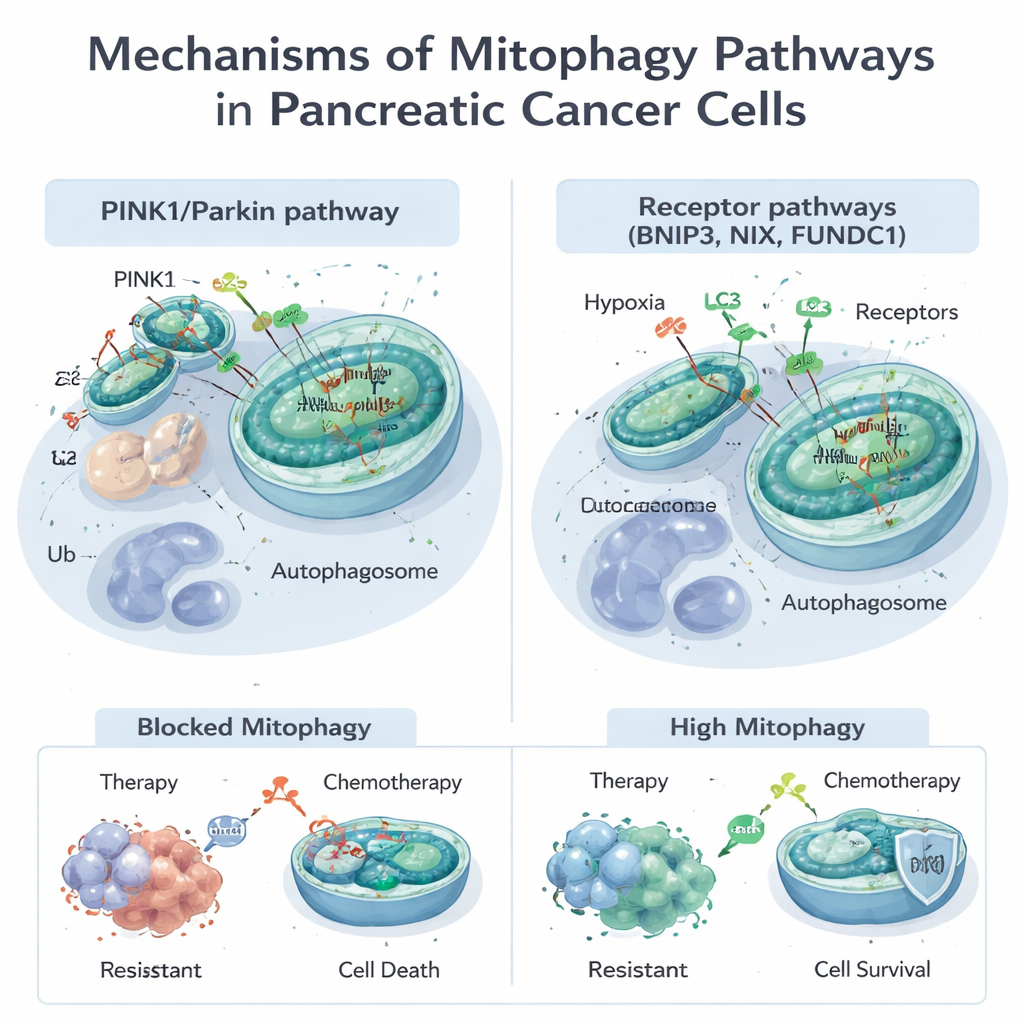
Новые идеи лечения и потребность в точном подборе пациентов
Поскольку митофагия находится на стыке метаболизма, стресс‑ответов и клеточной гибели, она представляет собой привлекательную мишень для комбинированных терапий. Нынешние лекарственные стратегии в основном действуют косвенно: одни соединения вмешиваются в процессы деления и слияния митохондрий; другие, такие как хлорохин и гидроксихлорохин, блокируют заключительные этапы переработки, нарушая слияние аутофагосом с кислыми компартментами деградации. Ряд клинических испытаний проверяет эти препараты в сочетании с традиционной химиотерапией при раке поджелудочной. Однако результаты пока неоднозначны — некоторые пациенты выигрывают, другие нет. Часть проблемы в том, что опухоли сильно различаются по базовому уровню митофагии и метаболическому профилю: некоторые сильно зависят от митохондриального дыхания, другие — от гликолиза. Авторы утверждают, что будущий успех потребует лучших биомаркеров и генетических подписей для группировки пациентов по активности митофагии и использованию энергии, а также разработки более точных препаратов, которые выборочно регулируют конкретные митофагические маршруты, вместо грубого включения или выключения аутофагии. Для широкого круга читателей ключевой вывод таков: умение читать и аккуратно корректировать систему митохондриальной очистки может помочь превратить рак поджелудочной из упрямого врага в более управляемое заболевание.
Цитирование: Wang, Z., Lyu, Z., Palmen, R. et al. Mitophagy in pancreatic cancer: mechanistic insights and implications for novel therapeutic strategies. Cell Death Discov. 12, 93 (2026). https://doi.org/10.1038/s41420-026-02948-9
Ключевые слова: рак поджелудочной железы, митофагия, митохондрии, устойчивость к химиотерапии, метаболизм опухоли