Clear Sky Science · ru
Остеопонтин, производимый при колоректальном раке, перенастраивает макрофаги в про-метастатическое состояние M2 через ось PI3K/AKT/CSF1-CSF1R
Почему это важно для людей с раком толстой кишки
Большинство смертельных исходов при колоректальном (рак толстой и прямой кишки) раке связаны не с первичной опухолью, а с её распространением в другие органы. В этом исследовании изучают, как раковые клетки «общаются» с окружающими иммунными клетками, способствуя метастазированию. Выявив ключевой сигнал, который раковые клетки посылают, чтобы перепрограммировать иммунные клетки из борцов в их пособников, работа указывает на новые терапевтические подходы, которые могли бы замедлить или остановить метастазы при распространённом колоректальном раке.
Вязкий белок с тёмной стороной
Исследователи сосредоточились на белке остеопонтине (OPN), который синтезируется как раковыми клетками, так и некоторыми иммунными клетками внутри опухолей. OPN давно связывают с худшими прогнозами при многих видах рака, но механизм его влияния на метастазирование при колоректальном раке оставался неясным. При анализе больших баз данных пациентов и образцов опухолей команда обнаружила, что уровень OPN в ткани колоректального рака значительно выше, чем в нормальной ткани кишечника, особенно у пациентов с прогрессирующей болезнью и отдалёнными метастазами. У пациентов с более высоким содержанием OPN в опухоли выживаемость в целом была ниже, что указывает на тесную связь OPN с агрессивным, труднолечимым раком.
Дело не только в самих раковых клетках
Удивительно, но когда учёные в лаборатории заставляли колоректальные раковые клетки продуцировать больше или меньше OPN, сами по себе эти клетки не становились более инвазивными или подвижными. Их пролиферация, миграция и способность проникать через искусственные мембраны изменялись минимально. Это поставило под сомнение распространённую идею о том, что OPN в основном действует, прямо усиливая свойства самих раковых клеток. Вместо этого команда обратила внимание на соседство опухоли — так называемую опухолевую микроокружение — особенно на группу иммунных клеток, называемых макрофагами, которые могут либо атаковать опухоль (состояние «M1»), либо поддерживать её (состояние «M2»).
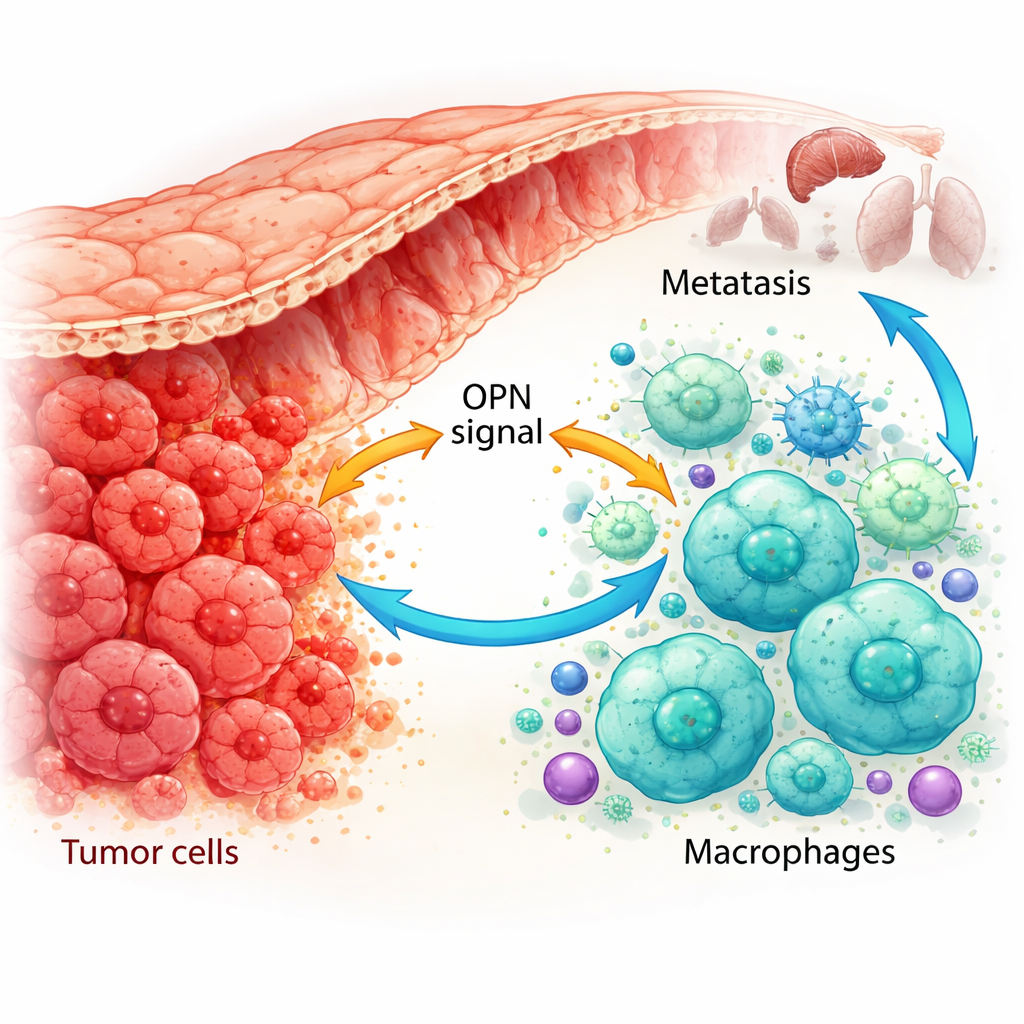
Как иммунные клетки перепрограммируются в помощников опухоли
С помощью одиночных клеточных транскриптомов и расширенного окрашивания тканей пациентов исследователи показали, что OPN продуцируется не только раковыми клетками, но и макрофагами, ассоциированными с опухолью. В опухолях, которые уже дали метастазы, и раковые клетки, и конкретный подтип макрофагов содержали много OPN. Эти макрофаги склонялись к M2-подобному, опухоль-поддерживающему состоянию и встречались чаще при высоких уровнях OPN в опухоли. В моделях на мышах опухоли, сконструированные для повышенного продуцирования OPN, привлекали больше таких M2-подобных макрофагов и росли быстрее, тогда как опухоли с пониженным OPN имели меньше M2-макрофагов и росли медленнее. Это указывает на то, что OPN является мощным фактором привлечения и перепрограммирования макрофагов в микроокружении опухоли.
Скрытая цепочка сигналов: от OPN к метастазам
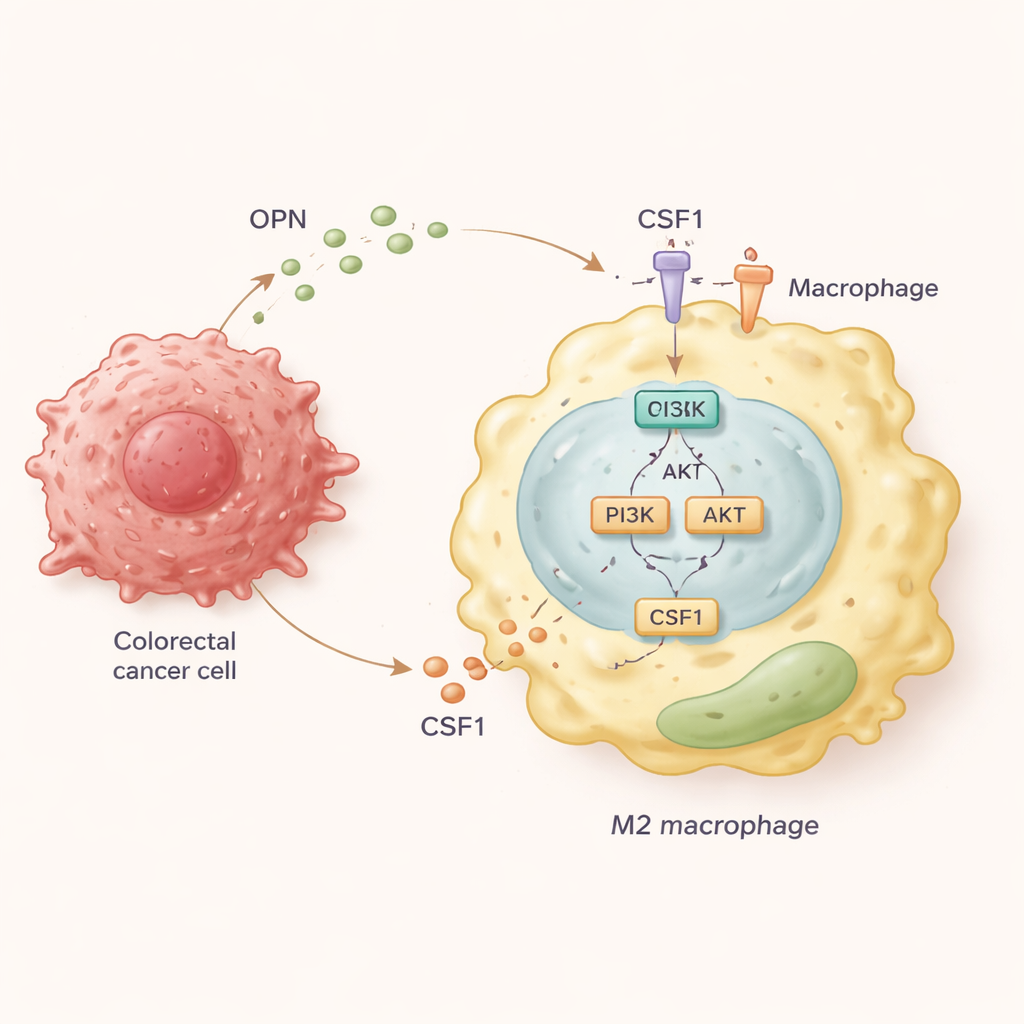
Чтобы выяснить молекулярную последовательность событий, команда выращивала человеческие макрофаги вместе с колоректальными раковыми клетками, производившими разные количества OPN. Они обнаружили, что клетки с высоким уровнем OPN сдвигают макрофаги в сторону состояния M2 и стимулируют двунаправленное взаимодействие: макрофаги мигрировали к опухоли, а раковые клетки становились более инвазивными в ответ на сигналы от этих макрофагов. Вглубь исследования показало, что OPN активирует внутри макрофагов сигнальный путь PI3K/AKT. Эта активация, в свою очередь, заставляет макрофаги выделять большие количества молекулы CSF1 и увеличивать экспрессию её рецептора CSF1R на поверхности. CSF1 затем действует по петле обратной связи, ещё сильнее закрепляя M2, про-метастатическое состояние и продолжая притягивать макрофаги в опухоль.
Прерывание петли, чтобы замедлить распространение
В моделях на мышах с распространившимся внутрибрюшным колоректальным раком исследователи протестировали препарат-блокатор CSF1R под названием PLX3397. У мышей с опухолями с высоким уровнем OPN развивалось много метастатических узлов, но лечение ингибитором CSF1R значительно уменьшало как число метастазов, так и присутствие M2-подобных макрофагов в опухолях. Раковые клетки демонстрировали меньше признаков роста и больше признаков программируемой гибели. Важно, что препарат в основном истощал макрофаги, поддерживающие опухоль, не оказывая сильного влияния на более воспалительный тип макрофагов, что указывает на относительно таргетированный способ ослабить иммунную поддержку опухоли.
Что это значит для будущего лечения
Главная мысль для непрофессионала заключается в том, что некоторые колоректальные раки успешно распространяются не только потому, что сами раковые клетки агрессивны, но и потому, что они захватывают соседние иммунные клетки и превращают их в соучастников. В этом исследовании OPN, производимый раковыми клетками, действует как главный переключатель, перепрограммирующий макрофаги через сигнальную цепочку PI3K/AKT и CSF1/CSF1R, создавая благоприятную среду для метастазирования. Разрыв этой цепочки — в частности на этапе CSF1R — позволил уменьшить распространение опухоли у мышей. Это указывает на то, что измерение уровней OPN могло бы помочь выявить пациентов, которые получают выгоду от препаратов, нацеленных на макрофаги, а также что комбинирование таких препаратов с существующими методами лечения или иммунотерапией может дать новую надежду людям с запущенным колоректальным раком.
Цитирование: Liang, X., Qin, F., Yuan, Z. et al. Colorectal cancer-derived osteopontin rewires macrophages into a pro-metastatic M2 state via the PI3K/AKT/CSF1-CSF1R axis. Cell Death Discov. 12, 92 (2026). https://doi.org/10.1038/s41420-026-02945-y
Ключевые слова: колоректальный рак, остеопонтин, макрофаги, ассоциированные с опухолью, метастазирование, ингибирование CSF1R