Clear Sky Science · ru
Таргетирование сигнальной оси NXPH4/ALDH1L2 подавляет резистентность к энзалутамиду при раке предстательной железы
Почему это важно для пациентов с раком предстательной железы
Многие мужчины с прогрессирующим раком предстательной железы полагаются на мощный препарат, блокирующий гормоны, — энзалутамид. Сначала он часто эффективно действует, уменьшая опухоли и замедляя развитие болезни. Но у большинства пациентов со временем опухоль находит способы обойти действие лекарства и начинает снова расти. В этом исследовании проанализировано, как происходит такое уклонение, и выявлена новая уязвимость в медикаментозно‑резистентных опухолях — что открывает возможный путь к более длительной и эффективной терапии существующими средствами.
Распространённое лечение встречает упрямую болезнь
Рост рака предстательной железы тесно связан с мужскими гормонами, или андрогенами, которые действуют через белок, называемый андрогенным рецептором. Энзалутамид разработан для подавления этого рецептора и является стандартной терапией, когда опухоли перестают реагировать на традиционное снижение уровня гормонов. К сожалению, многие опухоли адаптируются, превращаясь в то, что врачи называют кастрационно‑резистентным раком предстательной железы. Авторы работы поставили задачу выяснить, какие гены помогают клеткам выживать при лечении энзалутамидом, с надеждой, что блокирование этих помощников вернёт эффективность лекарства.
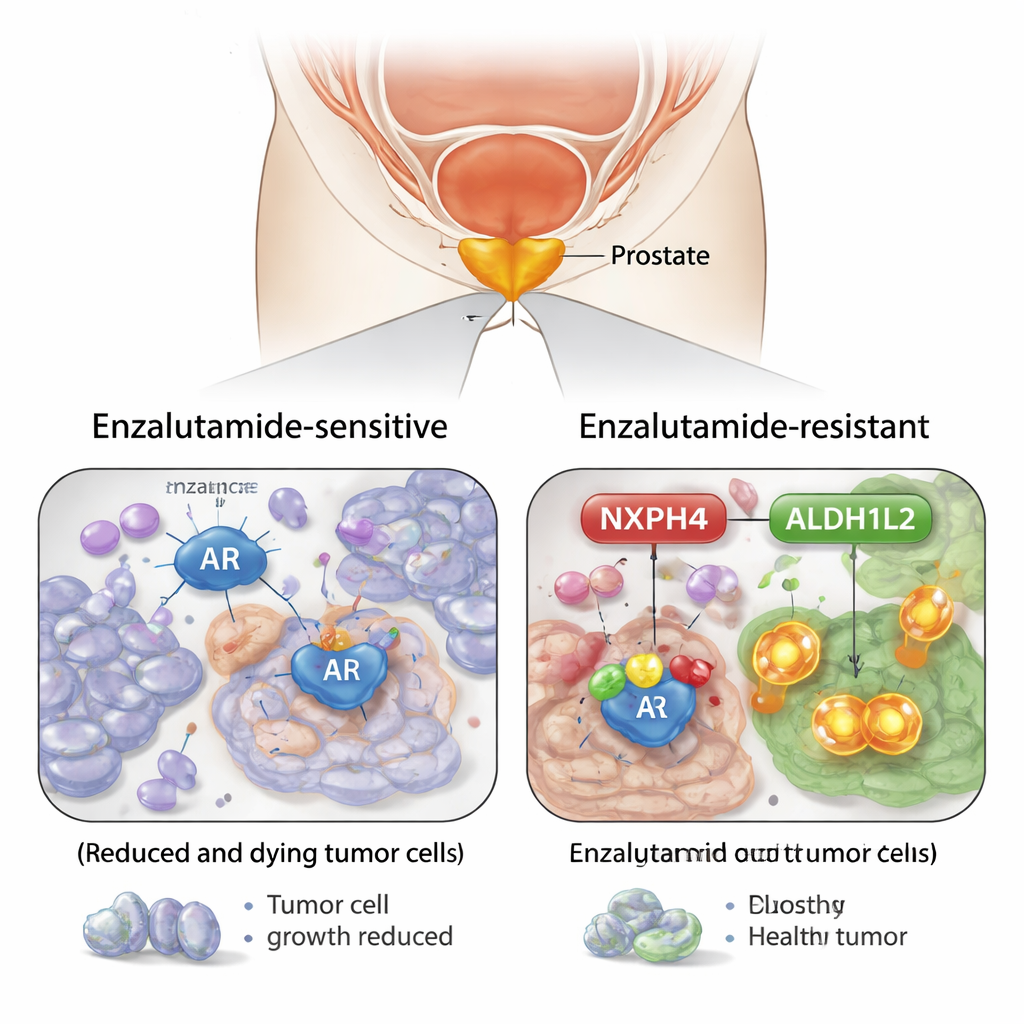
Выявление неожиданного вспомогательного молекула
Сравнивая клетки рака предстательной железы, чувствительные к энзалутамиду, с клетками, ставшими резистентными, исследователи идентифицировали белок под названием NXPH4 как ключевой фактор. Резистентные клетки продуцировали значительно больше NXPH4, и его уровень последовательно повышался при длительном воздействии энзалутамида. Образцы тканей пациентов показали ту же закономерность: более высокий уровень NXPH4 в более агрессивных опухолях и в раках, переставших реагировать на препарат. При снижении уровня NXPH4 в резистентных клетках эти клетки становились более уязвимыми для энзалутамида и формировали меньше колоний как в культуре, так и у мышей. Напротив, вынужденная сверхэкспрессия NXPH4 делала клетки труднее лечимыми.
Как гормоны включают NXPH4
Исследование также выясняло, почему NXPH4 так обилен в этих опухолях. Ответ снова указывал на андрогенный рецептор. Ученые показали, что при обработке клеток гормоном дигидротестостероном уровень NXPH4 повышается. При дополнительной экспрессии андрогенного рецептора NXPH4 увеличивался; при блокаде рецептора NXPH4 падал. Детальные эксперименты с ДНК подтвердили, что андрогенный рецептор физически связывается с регуляторным участком гена NXPH4, активируя его. Это означает, что та же гормон‑опосредованная система, которая стимулирует рост рака предстательной железы, также настраивает клетки на повышение уровня NXPH4, создавая предпосылки для последующей лекарственной резистентности.
Разгон «энергетических фабрик» клетки
Глубже изучая механизм, команда обнаружила, что NXPH4 меняет управление энергией и стрессом в митохондриях — крошечных электростанциях клетки. При условиях блокирования гормонов часть NXPH4 перемещается в митохондрии и связывается с другим белком, ALDH1L2, который важен для производства NADPH — ключевой молекулы, помогающей контролировать вредные реактивные формы кислорода (ROS). В резистентных клетках NXPH4 и ALDH1L2 образуют комплекс, который усиливает митохондриальное дыхание, поддерживает мембранный потенциал, увеличивает уровень NADPH и снижает ROS. Такая комбинация сохраняет митохондрии в рабочем состоянии и позволяет клеткам переносить стресс от энзалутамида, вместо того чтобы погибнуть, как обычно.
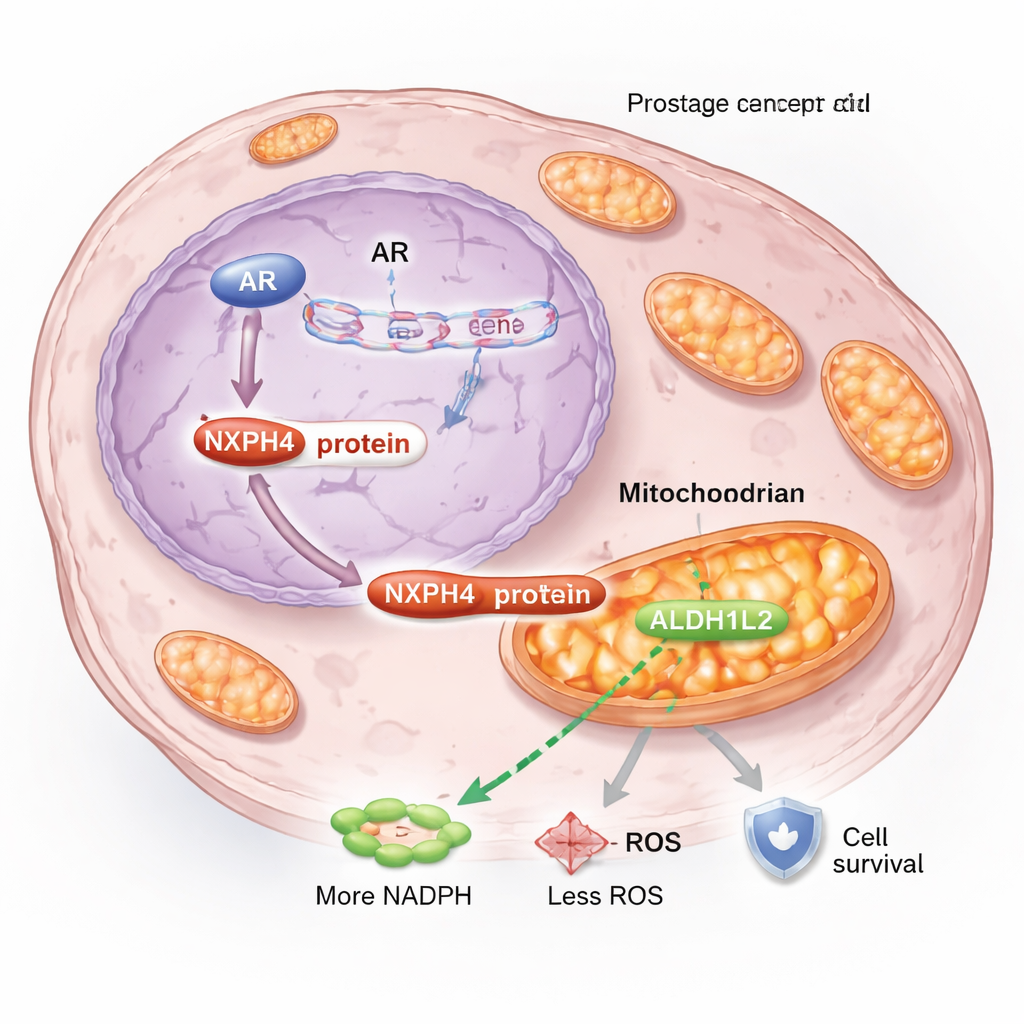
Нарушение цепи резистентности
Когда исследователи нарушили эту митохондриальную систему поддержки, результаты были впечатляющими. Понижение NXPH4 в резистентных клетках снизило митохондриальную активность, повысило окислительный стресс, замедлило рост и сделало клетки гораздо более восприимчивыми к энзалутамиду. Подавление ALDH1L2 давало похожий эффект и сводило на нет защитные преимущества от избыточного NXPH4, подтверждая, что эти два белка действуют совместно. В моделях на мышах опухоли с дефицитом NXPH4 росли медленнее, а сочетание потери NXPH4 с лечением энзалутамидом уменьшало опухоли ещё сильнее, чем каждый подход по‑отдельности. Эти данные указывают на то, что партнёрство NXPH4–ALDH1L2 — не просто побочный эффект резистентности, а движущая сила процесса.
Что это может значить для будущего лечения
Проще говоря, работа показывает, что некоторые раки предстательной железы переживают терапию энзалутамидом, перенастраивая свой энергоснабжающий механизм. NXPH4, активируемый андрогенным рецептором, объединяется с ALDH1L2 внутри митохондрий, чтобы поддерживать их функцию, защищать от окислительного повреждения и помогать опухолевым клеткам переживать блокаду гормонов. Таргетирование NXPH4 или его взаимодействия с ALDH1L2 может ослабить эту цепь выживания. Хотя препаратов, направленных непосредственно против NXPH4, пока нет, исследование выделяет эту пару молекул как перспективную мишень. В будущем сочетание энзалутамида с лекарствами, нарушающими сигнальную ось NXPH4‑ALDH1L2, может помочь пациентам дольше опережать резистентный рак предстательной железы.
Цитирование: Sun, X., Zhang, Y., Zhang, W. et al. Targeting NXPH4/ALDH1L2 signaling suppresses enzalutamide resistance in prostate cancer. Cell Death Discov. 12, 91 (2026). https://doi.org/10.1038/s41420-026-02944-z
Ключевые слова: рак предстательной железы, резистентность к энзалутамиду, митохондриальный метаболизм, NXPH4, ALDH1L2