Clear Sky Science · ru
Роттлерин инициирует двойную деградацию SLC7A11 и GPX4, вызывая ферроптоз и хемоусиление при гепатоцеллюлярной карциноме
Почему это природное соединение важно для рака печени
Гепатоцеллюлярная карцинома, наиболее распространённая форма первичного рака печени, часто диагностируется поздно и остаётся трудной для лечения. В этом исследовании изучается, может ли растительное соединение роттлерин, давно известное своими широкими противоопухолевыми эффектами, быть использовано для запуска более новой формы клеточной гибели — ферроптоза — в клетках рака печени. Поняв молекулярный механизм действия роттлерина, исследователи надеются открыть новые пути для более эффективных и менее подверженных развитию резистентности методов лечения.
Новый способ убивать раковые клетки
Традиционные противораковые препараты обычно направляют опухолевые клетки в хорошо изучённые программы гибели, такие как апоптоз. Ферроптоз отличается: это зависимый от железа процесс, вызванный накоплением токсичных липидов в мембранах клеток. Клетки рака печени особенно уязвимы к такому повреждению, потому что они сильно зависят от антиоксидантных систем, удерживающих эти липидные токсины под контролем. Команда поставила вопрос, может ли роттлерин подорвать эти защиты и тем самым заставить клетки рака печени вступить в ферроптоз.
Как роттлерин замедляет рост опухоли
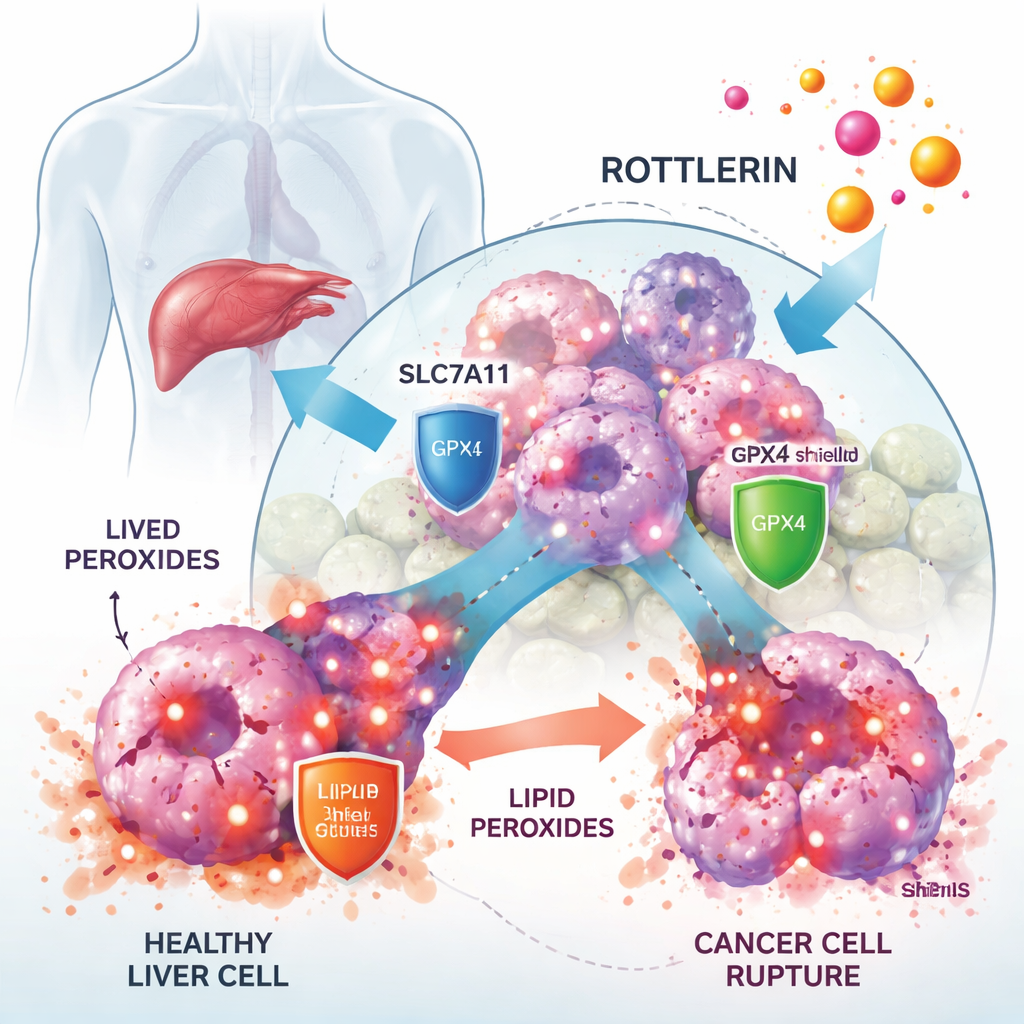
Работая с культурами человеческих клеток рака печени, исследователи показали, что роттлерин резко снижал рост раковых клеток при низких концентрациях в микромолярном диапазоне, тогда как нормальные клетки, связанные с печенью, были менее затронуты. При добавлении специфического блокатора ферроптоза Ferrostatin‑1 большая часть гибели клеток, вызванной роттлерином, была предотвращена, что сильно указывает на ферроптоз как основной механизм гибели. Микроскопия и биохимические тесты подтвердили это: обработанные роттлерином клетки накапливали высокие уровни липидных перекисей, демонстрировали изменённые митохондрии и сниженные запасы антиоксидантного молекулы глутатиона — все признаки ферроптоза.
Обезоруживание антиоксидантных щитов клеток
Клетки рака печени выживают, опираясь на критическую защитную ось, состоящую из транспортёра SLC7A11 и фермента GPX4. SLC7A11 импортирует цистин — строительный блок для глутатиона, а GPX4 использует глутатион для нейтрализации липидных перекисей до того, как они повредят мембраны. В исследовании обнаружили, что роттлерин со временем снижал уровни белков SLC7A11 и GPX4. Это происходило не потому, что клетки переставали их синтезировать, а потому, что эти белки помечались небольшими «метками уничтожения» (убиквитином) и направлялись в протеасому — клеточную машину по утилизации белков. Блокирование протеасомы обращало эту потерю, а искусственное повышение уровня SLC7A11 или GPX4 в клетках частично защищало их от роттлерина. В совокупности эти данные показывают, что роттлерин действует как двойной деградатор двух ключевых защит от ферроптоза.
Усиление существующих препаратов для рака печени
Многие пациенты с прогрессирующим раком печени получают сорафениб — стандартный препарат первой линии, который сам способен индуцировать ферроптоз, но эффективность часто ограничена развитием резистентности. Авторы проверили, могут ли низкие, в противном случае слабые дозы роттлерина повысить чувствительность опухолевых клеток к препаратам, индуцирующим ферроптоз, таким как сорафениб и RSL3. В культурах клеток сочетание низкой дозы роттлерина с одним из этих препаратов заметно увеличивало гибель раковых клеток и смещало кривые доза‑ответ, указывая на усиление мощности. Важно, что этот сенсибилизирующий эффект сохранялся даже при генетическом снижении классической мишени роттлерина — белка PKCδ, что показывает: ключевое действие происходит не через этот киназный путь, а через деградацию SLC7A11 и GPX4. В модельных мышах с человеческими опухолями печени комбинированное лечение роттлерином и сорафенибом замедляло рост опухолей больше, чем сорафениб один, и дополнительно снижало уровни SLC7A11 и GPX4 в опухолях.
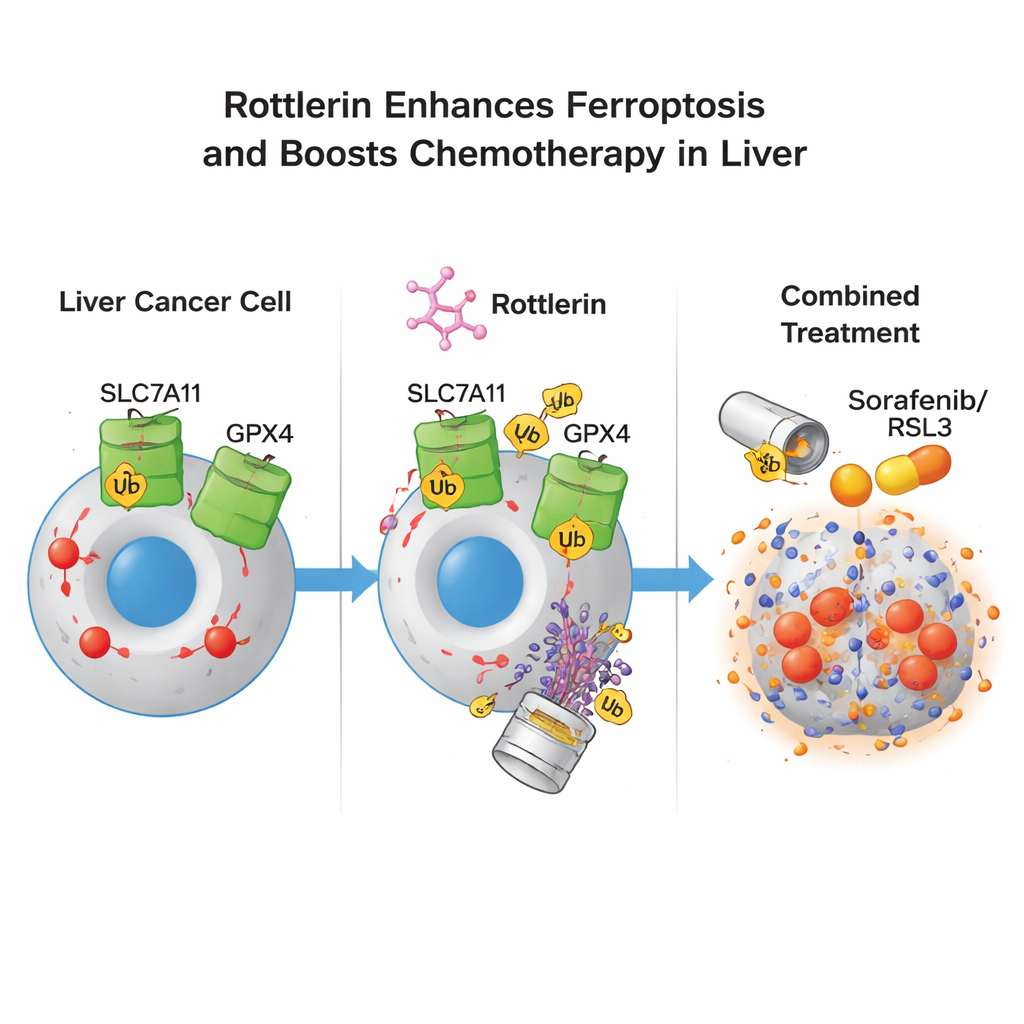
Что это может значить для будущих методов лечения
Для неспециалистов суть в том, что роттлерин действует как «отмычка с двумя зубцами» в отношении клеток рака печени: он одновременно снимает две критические «защёлки» — SLC7A11 и GPX4 — которые обычно защищают клетки от разрушительной волны липидной оксидации. Как только эти «защёлки» исчезают, раковые клетки значительно чаще подвергаются ферроптозу, особенно в сочетании с существующими препаратами, направляющими их в этом направлении. Хотя необходимы дополнительные исследования, прежде чем роттлерин или родственные соединения смогут быть применены у пациентов, стратегия двойной деградации выглядит многообещающей для обхода адаптивных защит, которые часто делают печёночные опухоли столь трудными для лечения.
Цитирование: Luo, H., Jin, X., Gao, C. et al. Rottlerin triggers dual degradation of SLC7A11 and GPX4 to drive ferroptosis and chemosensitization in hepatocellular carcinoma. Cell Death Discov. 12, 89 (2026). https://doi.org/10.1038/s41420-026-02942-1
Ключевые слова: рак печени, ферроптоз, роттлерин, SLC7A11, GPX4