Clear Sky Science · ru
Активация GCN2 и последующей Ответной реакции на нарастающее число незавернутых белков с помощью небольшого перорального молекулы NXP800 замедляет рост опухоли при остеосаркоме
Превращая стресс рака в уязвимость
Остеосаркома — редкий, но агрессивный рак кости, который в основном поражает детей и молодых взрослых. Десятилетиями лечение опиралось на интенсивную химиотерапию и операцию, однако выживаемость при распространённой болезни почти не улучшилась. В этом исследовании изучают новый пероральный препарат NXP800, который нацелен на скрытую уязвимость раковых клеток: их постоянную борьбу с внутренним стрессом. Подталкивая этот стресс за критическую точку, NXP800 может заставить опухолевые клетки самоуничтожиться, при этом щадя большинство здоровых клеток.
Тяжёлый рак кости, нуждающийся в новых вариантах лечения
Остеосаркома обычно развивается в длинных костях рук и ног и может быстро распространяться в лёгкие. Стандартная терапия сочетает несколько сильнодействующих химиопрепаратов с операцией по удалению опухоли. Хотя этот подход излечивает многих пациентов с локализованной болезнью, прогноз плох у тех, чьи опухоли рецидивируют или уже метастазировали к моменту постановки диагноза. Поскольку существующие препараты исчерпали свои возможности, исследователи ищут терапии, которые атакуют остеосаркому принципиально иным образом, желательно нацеливаясь на черты, отличающие раковые клетки от нормальных тканей.
Делаем стресс оружием против опухолевых клеток
Раковые клетки живут в условиях постоянного давления. Они быстро делятся, потребляют много энергии и кислорода и часто сталкиваются с неблагоприятными условиями, такими как гипоксия или воздействие химиотерапии. Чтобы справляться, они полагаются на аварийные системы, которые помогают правильно сворачивать и обрабатывать белки и настраивать обмен веществ. Одна из таких систем известна как «ответ на накопление незавёрнутых белков» (unfolded protein response), который запускается, когда «белковая фабрика» клетки — эндоплазматический ретикулум — перегружена. Другая система, «интегрированный стрессовый ответ», чувствует разные виды стресса и замедляет синтез белка. Как правило, эти пути помогают раковым клеткам выживать — но если их перегрузить слишком сильно и надолго, они могут переключиться с защиты клетки на запуск её гибели.
NXP800 поражает ключевой сенсор стресса
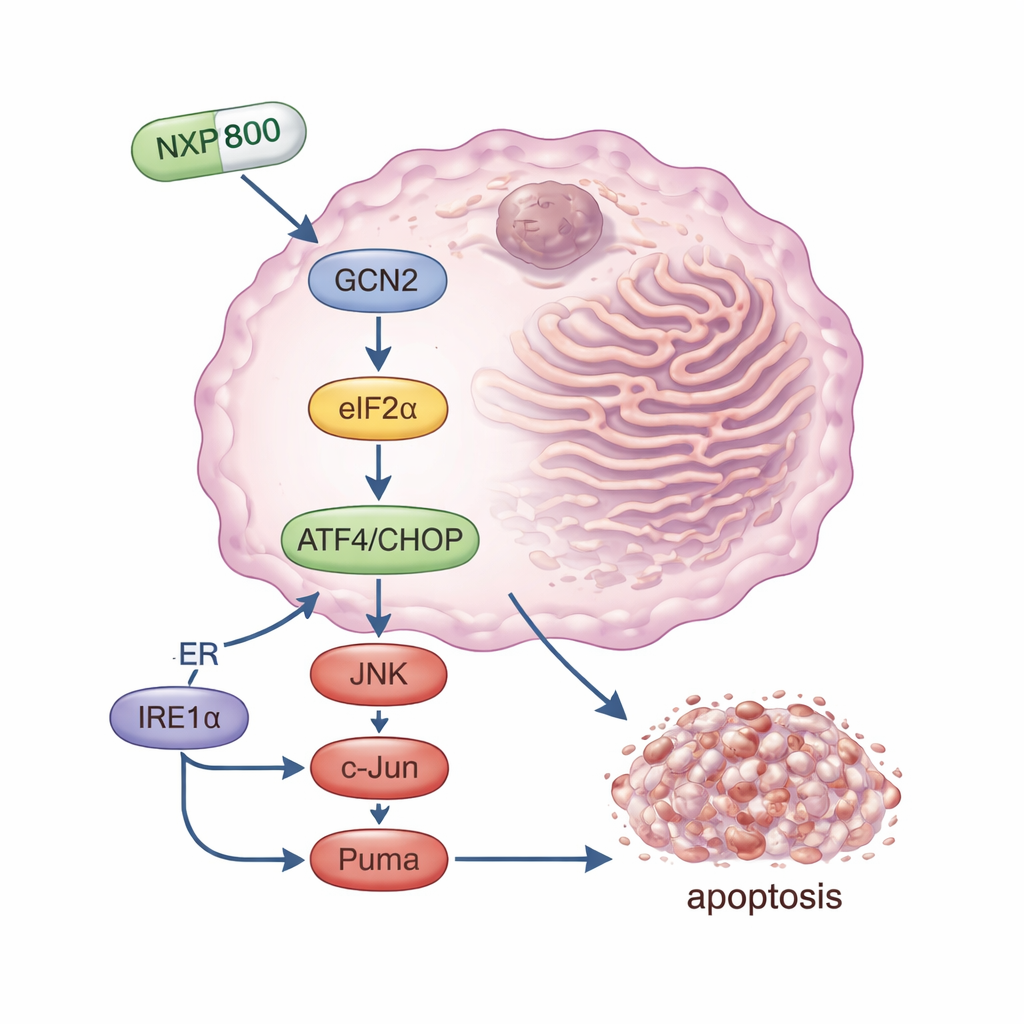
NXP800 — это пероральная малая молекула, изначально разработанная для блокирования пути теплового шока, вовлечённого в выживание рака. В этом исследовании учёные обнаружили, что в клетках остеосаркомы её основной эффект иной: она сильно активирует белок-датчик стресса GCN2. После активации GCN2 модифицирует другой фактор, eIF2α, который быстро снижает общий синтез белка и одновременно повышает уровни определённых «главных переключателей» стресса, особенно белка ATF4 и его партнёра CHOP. Вместе эти молекулы сдвигают клетку в сторону программируемой гибели. Команда показала, что при блокировании GCN2 — либо заглушая его ген, либо применяя отдельный ингибитор — NXP800 уже не способен эффективно запускать эту каскадную реакцию, и раковые клетки становятся значительно менее чувствительны к препарату. Это указывает на GCN2 как на ключевую мишень NXP800 при остеосаркоме.
Активация нескольких путей гибели внутри опухоли
Кроме ветви стресса через GCN2, NXP800 также включал другой путь, связанный с клеточной гибелью. Он активировал сенсор IRE1α, который, в свою очередь, усиливал сигнальные белки JNK и c-Jun. Эта ветвь известна тем, что стимулирует производство Puma — мощного провоцирующего смерть молекулы, повреждающей внутренние механизмы выживания клетки. В лабораторных экспериментах NXP800 замедлял рост клеток остеосаркомы, вызывал остановку клеточного цикла и активировал ферменты и изменения белков, характерные для апоптоза, или контролируемой клеточной гибели. Важно, что нормальные стволовые клетки, связанные с костью, были гораздо меньше затронуты, что предполагает некоторую селективность в отношении опухолевых клеток, уже живущих на грани переносимого стресса.
От лабораторной скамьи к живым моделям
Чтобы проверить, переносятся ли эти клеточные эффекты в реальный контроль над опухолью, исследователи протестировали NXP800 на мышах с имплантированными рядом с большой берцовой костью человеческими клетками остеосаркомы. У мышей, получавших NXP800 перорально, опухоли росли значительно медленнее и по окончании исследования имели примерно половину объёма по сравнению с опухолями у нелечёных животных. Образцы опухолей от лечённых животных демонстрировали явные признаки механизма действия препарата: более высокие уровни маркёров стресса eIF2α и ATF4, меньше активно делящихся клеток и больше клеток, подвергающихся апоптозу. Отдельные эксперименты по безопасности на здоровых мышах не выявили существенных повреждений органов, и показатели функции печени не ухудшились, что поддерживает управляемый профиль безопасности при применённых дозах.
Что это может значить для пациентов
В совокупности работа показывает, что NXP800 может замедлять рост остеосаркомы, целенаправленно чрезмерно активируя собственные стрессовые защитные механизмы раковой клетки до тех пор, пока они не вызовут её самоуничтожение. Нацеливаясь на сенсор стресса GCN2 и связанные пути, препарат предлагает принципиально новый способ ослабить опухоли, устойчивые к традиционной химиотерапии. Поскольку NXP800 уже испытывается в ранних клинических испытаниях при других видах рака, эти данные открывают возможность его репозиционирования для лечения остеосаркомы, как в монорежиме, так и в комбинации с существующими препаратами. Хотя для подтверждения пользы и безопасности потребуются испытания на людях, это исследование даёт убедительное доказательство принципа: обращение клеточного стресса против самой опухоли может открыть новую терапевтическую главу для пациентов с этой тяжёлой формой рака кости.
Цитирование: Racineau, E., Lallier, M., Postec, A. et al. Activating GCN2 and subsequently the Unfolded Protein Response with the small oral molecule NXP800 delays tumor growth in osteosarcoma. Cell Death Discov. 12, 94 (2026). https://doi.org/10.1038/s41420-026-02941-2
Ключевые слова: остеосаркома, NXP800, ответ на стресс, путь GCN2, апоптоз