Clear Sky Science · ru
Потеря DIAPH3 ускоряет развитие глиомы у мышей
Почему это исследование мозга важно
Глиобластома — одна из самых смертоносных опухолей мозга: несмотря на операцию, радиацию и химиотерапию, большинство пациентов живут чуть больше года. Это исследование задаёт простой, но ключевой вопрос: какие ранние изменения внутри клеток мозга двигают их к формированию таких агрессивных опухолей и почему эти опухоли так трудно уничтожить радиацией? Отслеживая один структурный белок в клетках мозга мышей, исследователи показали, как его утрата дестабилизирует хромосомы, ускоряет появление опухолей и помогает стволоподобным клеткам опухоли выживать после облучения, которое должно было их уничтожить.
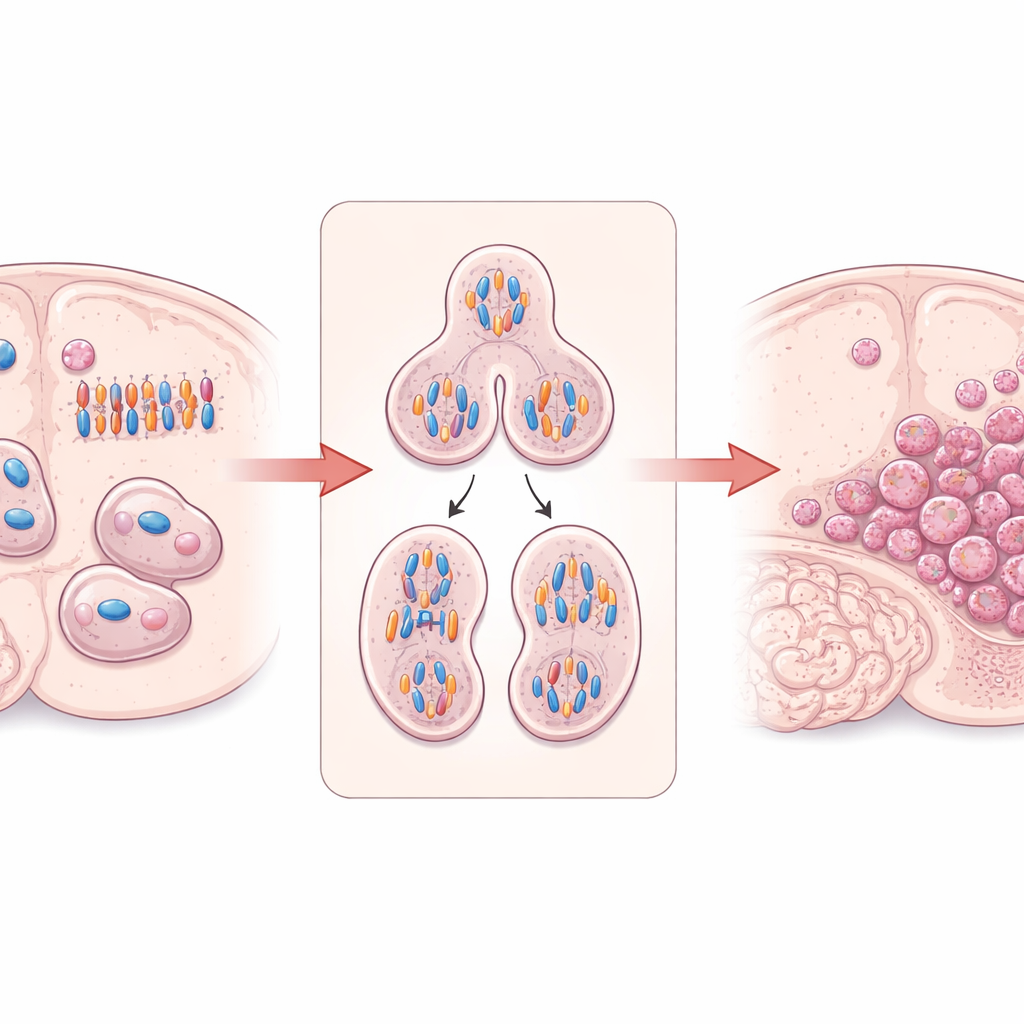
«Строитель» клетки, который следит за правильным делением
В центре внимания работы — DIAPH3, белок, участвующий в построении и организации внутреннего каркаса клетки из актиновых филаментов и микротрубочек. В делящихся стволовых клетках мозга DIAPH3 необходим для формирования верного веретена деления — структуры, которая расщепляет дублированные хромосомы, — и для механизма цитокинеза, разделяющего клетку на две. Ранние исследования показали, что при отсутствии DIAPH3 в развивающемся мозге мышей делящиеся клетки часто неверно перераспределяют хромосомы, что ведёт к анеуплоидии, остановке клеточного цикла и гибели клеток. Любопытно, что небольшой участок человеческой хромосомы 13, содержащий ген DIAPH3, часто удаляется при глиобластоме, а более высокие уровни DIAPH3 у некоторых пациентов связаны с лучшей выживаемостью, что указывает на возможную роль этого белка как опухолевого супрессора в мозге.
Генетическая модификация мышиного мозга для роста опухолей
Чтобы проверить, действительно ли потеря DIAPH3 способствует раку мозга, команда создала мышей, у которых два гена можно было избирательно удалить в стволовых клетках, формирующих кору: Diaph3 и Trp53, последний кодирует известного охранника генома p53. У мышей с удалённым только Diaph3 в этой области опухоли не развивались даже спустя два года, что говорит о том, что p53 способен устранить сильно аномальные клетки. В отличие от этого, мыши с удалённым только Trp53 или с двойным удалением Trp53 и Diaph3 в конечном счёте формировали диффузные высокозлокачественные глиомы, которые по микроскопическому строению очень напоминали человеческие. Повторные ультра‑высокопольные МРТ-последовательности показали, что животные с удалёнными обоими генами развивали обнаруживаемые опухоли раньше, и к среднему возрасту у них чаще встречались крупные глиомы, особенно в обонятельных луковицах, по сравнению с мышами с удалённым только Trp53. Скорость роста опухоли после её появления была сопоставима в группах — изменилось только то, как быстро появлялись опухоли.
Хромосомный хаос и перестроенная активность генов
Чтобы разобраться, почему утрата DIAPH3 ускоряет возникновение опухолей, исследователи проанализировали активность генов в обонятельных луковицах молодых мышей до появления видимых опухолей. У животных с удалёнными одновременно Diaph3 и Trp53 126 генов экспрессировались иначе по сравнению с мутантами только по Trp53, и почти половина из них ранее была связана с раком. Многие изменения объединялись в пути, отвечающие за рост клеток, миграцию и формирование сосудов, включая VEGF, MAPK, RAS, Rap1 и cAMP‑сигнальные каскады, а также сети G‑белок‑связанных рецепторов. Эта изменённая молекулярная картина указывала на то, что клетки раньше подталкиваются к состоянию, сходному с раковым. Анализ числа копий по всему геному в полностью сформировавшихся опухолях показал, что дефицит DIAPH3 не увеличивал существенно мелкие фокальные изменения ДНК, но усиливал крупные потери и выигрыши целых хромосом — ровно ту анеуплоидию, которую можно ожидать при нарушенной сегрегации хромосом.
Встроенные повреждения ДНК и более выносливые стволовые клетки опухоли
Анеуплоидные опухолевые клетки несли больше внутренних повреждений ДНК, что выявлялось повышенным уровнем маркера разрывов ДНК γ‑H2AX, распределённого по ядрам клеток. Тем не менее эти опухоли продолжали расти, что означает, что они приобрели механизмы толерантности к таким стрессам. Сравнивая экспрессию генов в установившихся опухолях, исследователи обнаружили сотни генов, изменённых при потере DIAPH3, включая заметную амплификацию и перепроизводство рецептора фактора роста FGFR2 во многих опухолях с двойной мутацией. Известно, что FGFR2 усиливает аппаратуру репарации ДНК в клетках глиобластомы, и его активация связывается с устойчивостью к радиации. Команда выделила из мышиных опухолей стволоподобные глиомные клетки и проверила их ответ на клинически релевантную дозу ионизирующего излучения. До облучения частота стволоподобных клеток была схожей в обоих генотипах, но после облучения культуры из опухолей, лишённых DIAPH3, сохраняли примерно вдвое больше жизнеспособных стволоподобных клеток, чем культуры из опухолей только с удалённым Trp53, что демонстрирует большую радиорезистентность.
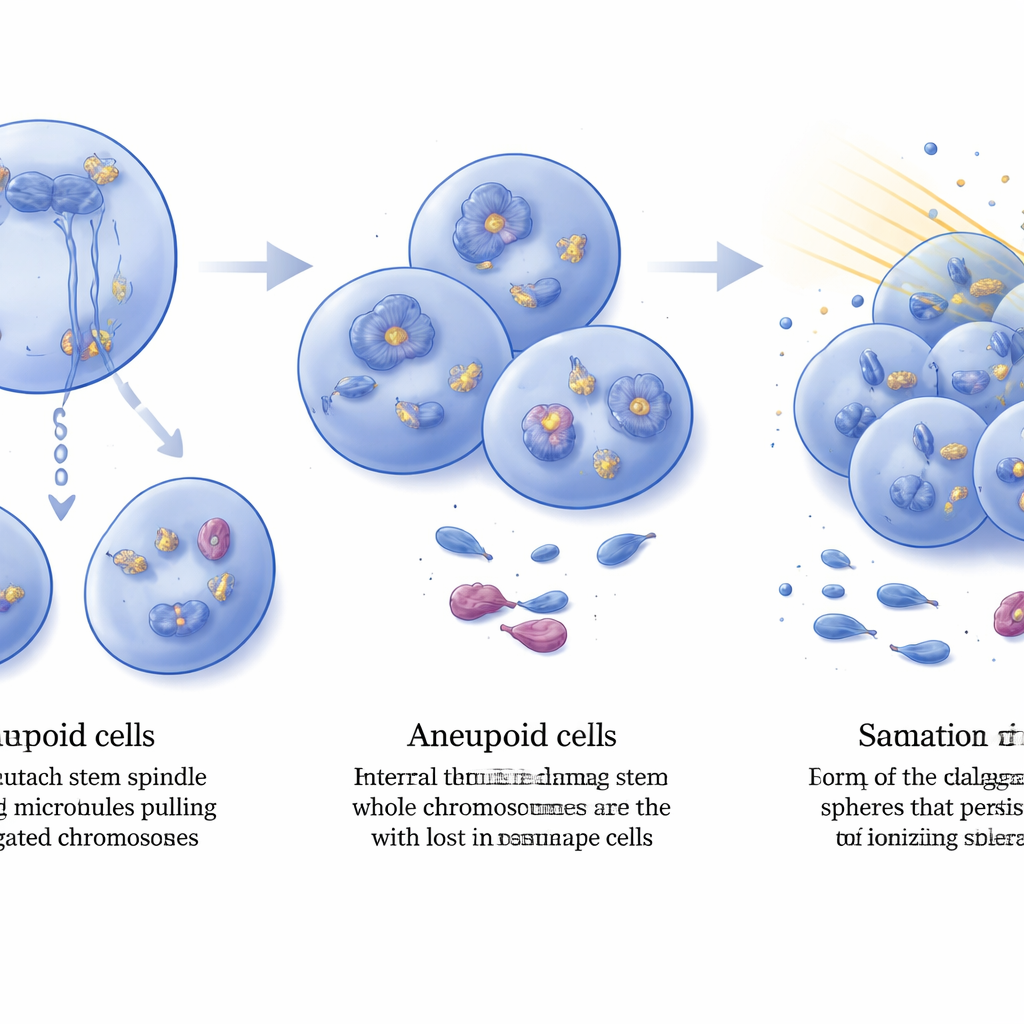
Что это означает для рака мозга
В совокупности исследование рисует DIAPH3 как стража, помогающего стволовым клеткам мозга делиться с правильным числом хромосом. Когда отсутствуют и DIAPH3, и p53, деление клеток становится ошибко‑подверженным, целые хромосомы теряются или приобретаются, и повреждения ДНК накапливаются. Вместо гибели некоторые клетки адаптируются через амплификацию факторов, связанных с репарацией — например, FGFR2 — превращаясь в анеуплоидные высокозлокачественные глиомы, чьи стволоподобные клетки необычно устойчивы к радиации. Хотя модели на мышах не воспроизводят все черты человеческой глиобластомы, эти результаты поддерживают идею DIAPH3 как потенциального прогностического маркера и узловой точки в сети процессов, контролирующих инициацию опухоли, стабильность генома и ответ на лечение — открывая новые пути для терапий, которые могли бы сделать эту разрушительную опухоль мозга более уязвимой для существующих методов лечения.
Цитирование: Chehade, G., Durá, I., Ruiz-Reig, N. et al. Loss of DIAPH3 accelerates glioma genesis in mice. Cell Death Dis 17, 342 (2026). https://doi.org/10.1038/s41419-026-08652-x
Ключевые слова: глиобластома, хромосомная нестабильность, стволовые клетки опухолей мозга, радиационная устойчивость, гены-супрессоры опухолей