Clear Sky Science · ru
Ось HNF4α-HKDC1 организует перестройку метаболизма для продвижения миграции и метастазирования при продвинутом раке желудка
Почему это важно для пациентов
Большинство смертей от рака желудка вызваны не первичной опухолью, а тем, что раковые клетки уходят в отдалённые участки тела и там закрепляются. В этой работе раскрыт скрытый молекулярный «включатель», который помогает клеткам рака желудка изменить использование энергоносителей и стать более подвижными. Ещё важнее то, что исследование указывает на уже одобренный FDA препарат, который можно потенциально перепрофилировать, чтобы выключить этот переключатель и замедлить или предотвратить распространение.
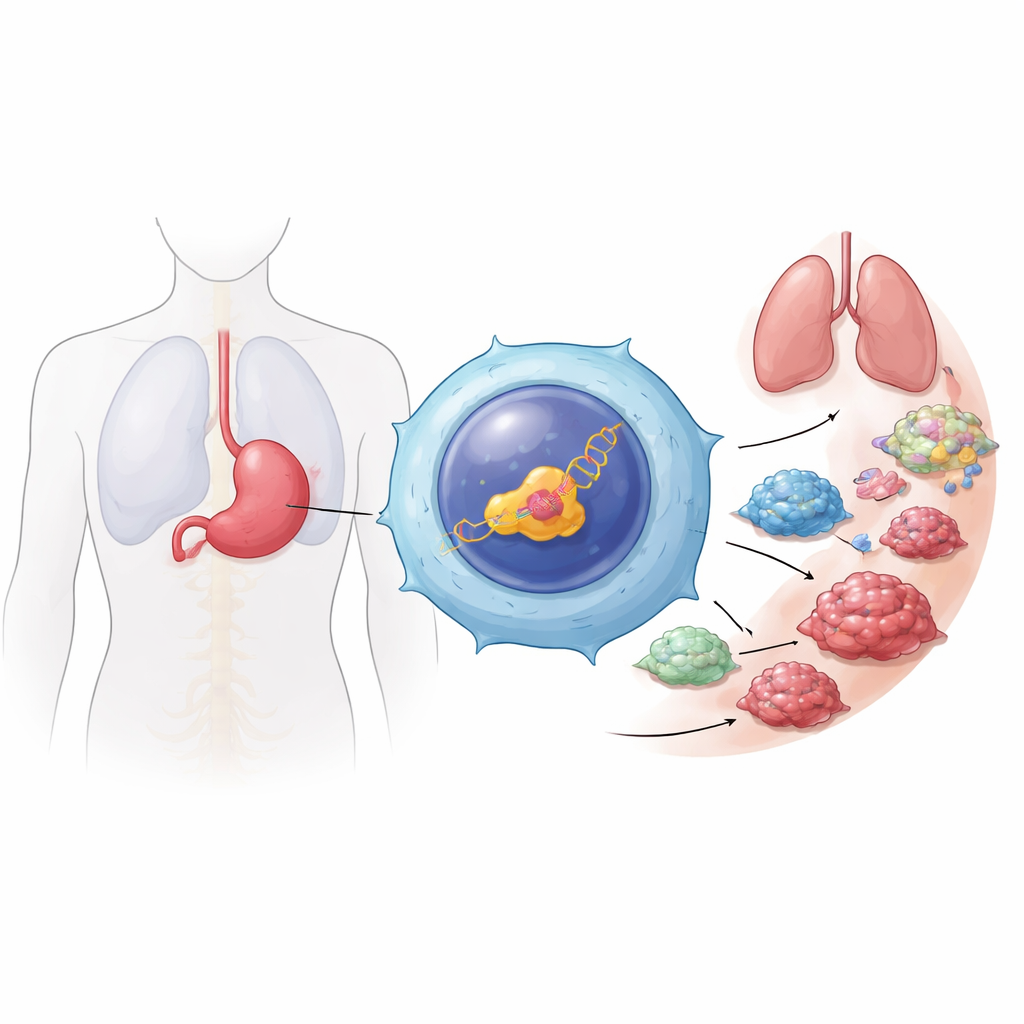
Опасный сдвиг при раке желудка
Рак желудка занимает пятое место по частоте во всём мире и часто выявляется на поздних стадиях, когда он уже распросранён. Авторы сосредоточились на метастазировании — этапе, когда клетки опухоли отделяются, перемещаются по брюшной полости или крови и колонизируют новые места. Анализируя крупные публичные онкологические базы данных и образцы тканей пациентов, они обнаружили, что специфический вариант регулятора генов HNF4α, управляемый промотором P2 (P2‑HNF4α), особенно обилен в отдалённых метастатических очагах по сравнению с первичной опухолью и прилегающей нормальной тканью. Этот вариант обнаруживался преимущественно внутри опухолевых клеток, а не в окружающих нормальных клетках, что указывает на его тесную связь с инвазивным поведением рака.
Мастер‑переключатель, усиливающий подвижность клеток
Чтобы проверить причинно‑следственную связь, исследователи изменяли уровни P2‑HNF4α в панеле человеческих клеточных линий рака желудка, отражающих основные молекулярные подтипы болезни. При снижении HNF4α в клетках, которые его обычно экспрессируют, клетки значительно теряли способность мигрировать и инвазировать через искусственные мембраны или заживать раны в культуральных условиях. При вынужденной экспрессии представительного изоформа P2‑HNF4α в клетках с низким уровнем HNF4α они становились заметно более подвижными и инвазивными, включая трехмерные сфероидные тесты, имитирующие реальные опухоли. В мышах клетки, модифицированные для чрезмерной продукции P2‑HNF4α, образовывали значительно больше метастатических узелков в брюшной полости, что демонстрирует, что этот фактор активно стимулирует распространение in vivo.
Питающее распространение перенастроение энергетического обмена
Раковые клетки часто меняют пути метаболизма, чтобы поддержать рост и подвижность. Сочетая секвенирование РНК и профиль метаболитов, команда обнаружила, что подавление HNF4α ослабляет ключевой энергетический путь — гликолиз, распад глюкозы. Уровни нескольких гликолитических ферментов и их промежуточных продуктов снижались, как и показатели энергетической активности, такие как потребление кислорода, образование кислот и генерация АТФ. Дальнейший анализ выделил один фермент, HKDC1, как наиболее сильно и последовательно связанный с HNF4α. HKDC1 участвует в самом первом шаге переработки глюкозы и направляет сахар как на образование лактата, так и на митохондриальное дыхание — два пути, которые вместе обеспечивают энергию и создают химическое окружение, благоприятное для движения клеток.
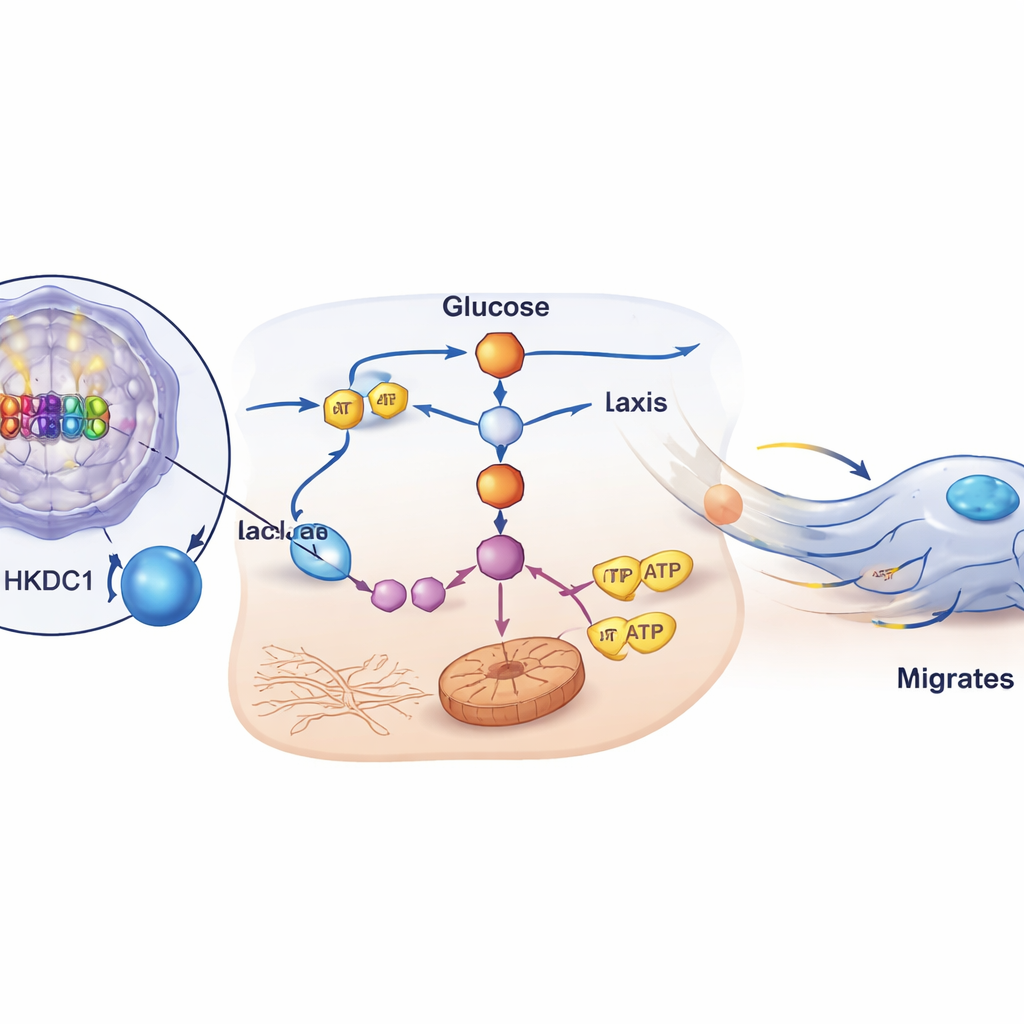
Прямая молекулярная связь и ключевой соучастник
Учёные показали, что P2‑HNF4α не просто коррелирует с HKDC1 — он прямо активирует этот ген. Используя данные о связывании по всему геному, ДНК‑репортерные анализы и тесты связывания белка с ДНК, они картировали специфические участки в энхансере гена HKDC1, где HNF4α сидит и активирует транскрипцию. При снижении HKDC1 в клетках их способность мигрировать и формировать перитонеальные метастазы у мышей резко падала, хотя краткосрочная выживаемость клеток не изменялась. Важно, что восстановление HKDC1 в клетках с нокаутированным HNF4α возвращало гликолитическую активность, энергетическое производство и миграционное поведение, а добавление метаболитов, таких как лактат или α‑кетоглутарат, также восстанавливало подвижность. В совокупности эти данные свидетельствуют, что HKDC1 является центральным нисходящим фактором, через который P2‑HNF4α перенастраивает метаболизм для питания метастазирования.
Выключение переключателя существующим препаратом
Поскольку HNF4α принадлежит к семейству белков, часто рассматриваемых как лекарственные мишени, команда проверила, может ли одобренный препарат блокировать эту про‑метастатическую ось. Ранее они идентифицировали микофеноловую кислоту, активную форму препарата микофенолата мофетила (MMF), как антагониста HNF4α в раке лёгкого. В настоящем исследовании лечение MMF снижало уровни HKDC1 и миграцию клеток в линиях рака желудка с высокой экспрессией HNF4α, тогда как в клетках с низким HNF4α эффект был минимален. В мышиных моделях MMF существенно сокращал абдоминальные метастазы и понижал экспрессию HKDC1 — но только при наличии высокой активности P2‑HNF4α в опухолях. Это говорит о том, что HNF4α может служить и терапевтической мишенью, и биомаркером для отбора пациентов, наиболее вероятно получающих пользу от стратегий на основе MMF.
Что это значит для будущей помощи пациентам
Проще говоря, это исследование выделяет молекулярную систему контроля топлива — P2‑HNF4α через HKDC1 — которая помогает клеткам рака желудка разгонять энергетическую машину и становиться лучше в распространении. Демонстрируя, что существующий препарат может вмешиваться в эту систему и уменьшать метастазирование в доклинических моделях, работа открывает реалистичный путь к новым лечению для продвинутого рака желудка. Если будущие клинические исследования подтвердят эти результаты, тестирование опухолей на активность HNF4α может помочь направлять применение MMF или родственных препаратов для замедления или предотвращения летального распространения болезни.
Цитирование: Xu, X., Wu, H., Shang, J. et al. HNF4α-HKDC1 axis orchestrates a metabolic rewiring to promote migration and metastasis in advanced gastric cancer. Cell Death Dis 17, 347 (2026). https://doi.org/10.1038/s41419-026-08627-y
Ключевые слова: метастазирование рака желудка, HNF4A, HKDC1, метаболизм рака, микопенолата мофетил