Clear Sky Science · ru
Метаболическая оркестровка, управляемая GGCT: перераспределение глутамина в синтез глутатиона при одновременном усилении аннаплероза глюкозой для пролиферации опухоли
Почему это важно для лечения рака
Раковые клетки быстро растут, и для этого им требуется огромное количество топлива, при этом им необходимо постоянно защищаться от токсичных побочных продуктов собственного метаболизма. В этом исследовании показано, как малоизвестный фермент GGCT помогает опухолям печени и предстательной железы хитро перенаправлять два распространённых субстрата — глутамин и глюкозу — так, чтобы они одновременно подпитывали рост и поддерживали контроль над вредными молекулами, называемыми реактивными формами кислорода. Понимание этого метаболического жонглирования может открыть новые пути для лишения опухолей питательных веществ или подавления их защитных механизмов.
Как опухолевые клетки жонглируют топливом и защитой
Опухолевые клетки сильно зависят от глутамина — аминокислоты, выполняющей двойную роль: она может разрушаться для подпитки основного энергетического цикла клетки и одновременно служить источником строительных блоков для глутатиона, мощного антиоксиданта, нейтрализующего реактивные формы кислорода. Авторы сначала подтвердили, что уровень глутамина выше в опухолях печени, чем в соседних здоровых тканях, и что раковые клетки, выращенные при повышенном содержании глутамина, активнее делятся как в культуре, так и в мышиных моделях. При недостатке глутамина клетки замедляют рост, падают ключевые белки клеточного цикла, и опухоли в животных моделях уменьшаются — отчасти потому, что ослабевают антиоксидантные защиты и накапливаются реактивные формы кислорода.
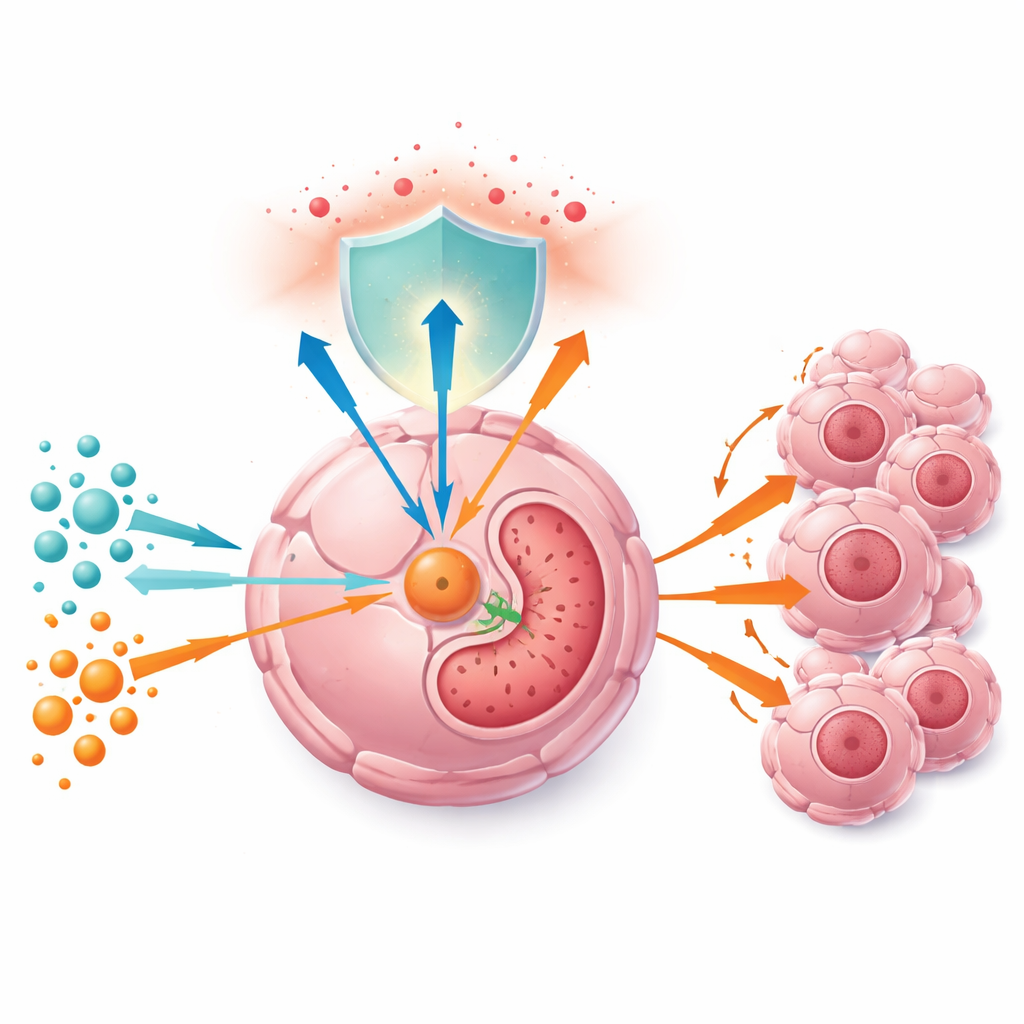
Метаболический переключатель на виду
Анализируя образцы пациентов и крупные онкологические базы данных, команда обнаружила, что фермент GGCT постоянно присутствует в большем количестве в опухолях печени и предстательной железы по сравнению с нормальными тканями, и более высокий уровень GGCT предсказывает худший прогноз. В образцах опухолей и в культивируемых клетках уровни GGCT повышаются вместе с концентрацией глутамина, что указывает на то, что опухоли «считывают» доступность глутамина через этот белок. Исследователи описали цепочку регуляции: глутамин поддерживает активность про‑ростового фактора c‑Myc, который подавляет малую регуляторную РНК miR‑29b‑3p; когда miR‑29b‑3p низка, GGCT снимается с тормоза и накапливается. При дефиците глутамина эта цепочка обращается: miR‑29b‑3p повышается, сообщения GGCT разрушаются быстрее, и уровень фермента падает.
Перенаправление глутамина и привлечение большего количества глюкозы
Чтобы понять, что GGCT делает в клетке, авторы снизили или повысили его уровни и измерили поведение клеток и сотни метаболитов. Заглушение GGCT тормозило клетки в цикле деления, уменьшало их колонии и резко снижало уровень глутатиона при одновременном повышении реактивных форм кислорода; добавление химического антиоксиданта частично восстанавливало рост. Под микроскопом митохондрии становились аномально удлинёнными и менее эффективными в потреблении кислорода, в то время как клетки пытались компенсировать это усилением гликолиза, первого шага расщепления сахара. Подробный метаболический профиль показал, что промежуточные метаболиты центрального энергетического цикла снижались при потере GGCT и возрастали при его избыточной экспрессии.
Прослеживание пути атомов углерода
Далее команда проследила меченые атомы глутамина и глюкозы, проходящие через метаболизм опухоли. При сверхэкспрессии GGCT меньше меченого глутамина попадало в энергетический цикл, а больше направлялось на синтез нового глутатиона, поддерживая антиоксидантную защиту. Одновременно меченая глюкоза сильнее вносила вклад в цикл, компенсируя перераспределение глутамина. Мутантная форма GGCT, лишённая нормальной ферментативной активности, не могла вызвать эти сдвиги и не стимулировала пролиферацию, что показывает, что каталитическая функция GGCT критична. Важно, что добавление лишнего пирувата или изменение путей входа в энергетический цикл восстанавливало уровни энергии в клетке, но не снижало уровень реактивных форм кислорода, указывая на то, что GGCT главным образом контролирует редокс‑баланс через глутатион, а не простыми изменениями энергетического снабжения.
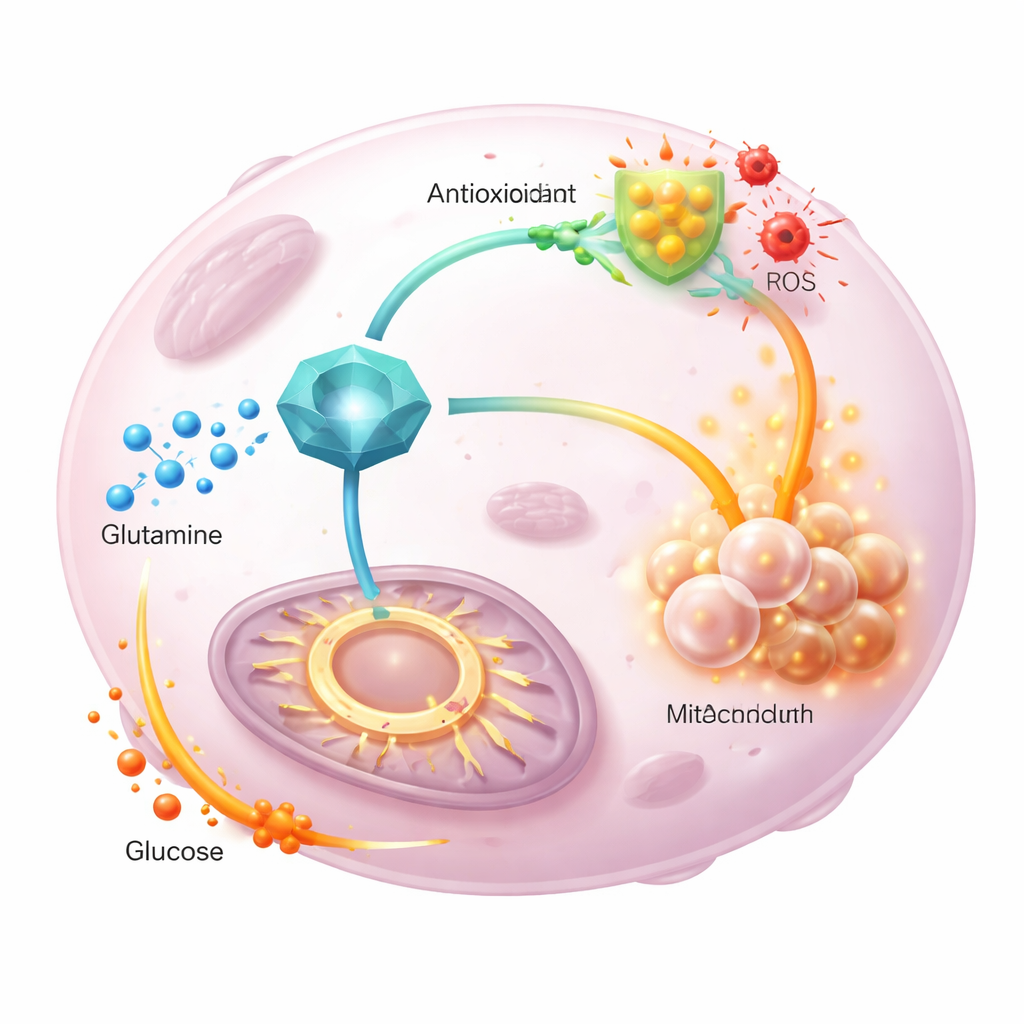
Что это значит для будущих терапий
В сумме результаты выдвигают GGCT как центрального координатора, позволяющего опухолям разделять функции глутамина: он направляет большую часть этого нутриента на производство антиоксиданта, одновременно привлекая глюкозу в энергетический цикл, чтобы поддерживать деление клеток. В модельных животных подавление GGCT замедляло рост опухолей, снижало уровень глутатиона и повышало окислительный стресс, и эти эффекты частично обращались при применении антиоксидантного препарата. Для непрофессионального читателя ключевая мысль в том, что некоторые раки выживают, используя GGCT как метаболический переключатель; препараты, которые отключают этот переключатель, могли бы одновременно ослабить защиту опухоли от окислительного повреждения и нарушить её гибкое использование питательных веществ, делая стандартные терапии более эффективными.
Цитирование: Yang, L., Sun, H., Wang, R. et al. Metabolic orchestration driven by GGCT: diverting glutamine to glutathione biosynthesis while enhancing glucose anaplerosis for tumor proliferation. Cell Death Dis 17, 358 (2026). https://doi.org/10.1038/s41419-026-08619-y
Ключевые слова: метаболизм рака, глутамин, глутатион, окислительный стресс, фермент GGCT