Clear Sky Science · ru
Адипогенная транслдифференцировка перенапрограммирует EMT‑богатые клетки ПДАК в постмитотическое состояние, похожее на адипоциты, и ограничивает метастазирование
Превращение агрессивных раковых клеток в безвредный жир
Рак поджелудочной железы — один из самых смертоносных видов рака, во многом потому, что он рано дает метастазы и плохо поддается стандартным методам лечения. В этой работе рассматривается заметно другой подход: вместо того чтобы пытаться отравить или лишить опухолевые клетки питания, что если удастся склонить наиболее опасные клетки поджелудочной к превращению в клетки, похожие на адипоциты, которые больше не делятся и не распространяются по организму? В исследовании показано, как ученые направляли высокоагрессивные раковые клетки поджелудочной в стабильное состояние, похожее на жировые клетки, что замедляло рост опухолей и снижало распространение у мышей, открывая новый путь контроля этого разрушительного заболевания.
Почему рак поджелудочной так трудно остановить
Панкреатическая дольковая аденокарцинома (ПДАК), основная форма рака поджелудочной железы, имеет крайне неблагоприятный прогноз: лишь около одного из восьми пациентов жив к пятилетнему рубежу после постановки диагноза. Отчасти проблема в том, что многие клетки опухоли находятся в пластичном, «меняющемся» состоянии, называемом EMT, которое делает их более подвижными, инвазивными и устойчивыми к лекарствам. Попытки блокировать многочисленные сигналы, поддерживающие это состояние, давали лишь ограниченный эффект. В то же время поджелудочная железа и ее опухоли демонстрируют удивительную склонность к накоплению жировых клеток, что породило вопрос: можно ли использовать эту скрытую гибкость клеточной идентичности. Авторы предположили, что если EMT‑богатые клетки ПДАК уже склонны к изменению, то их, возможно, удастся перенаправить в спокойную, жировую идентичность вместо инвазивной.
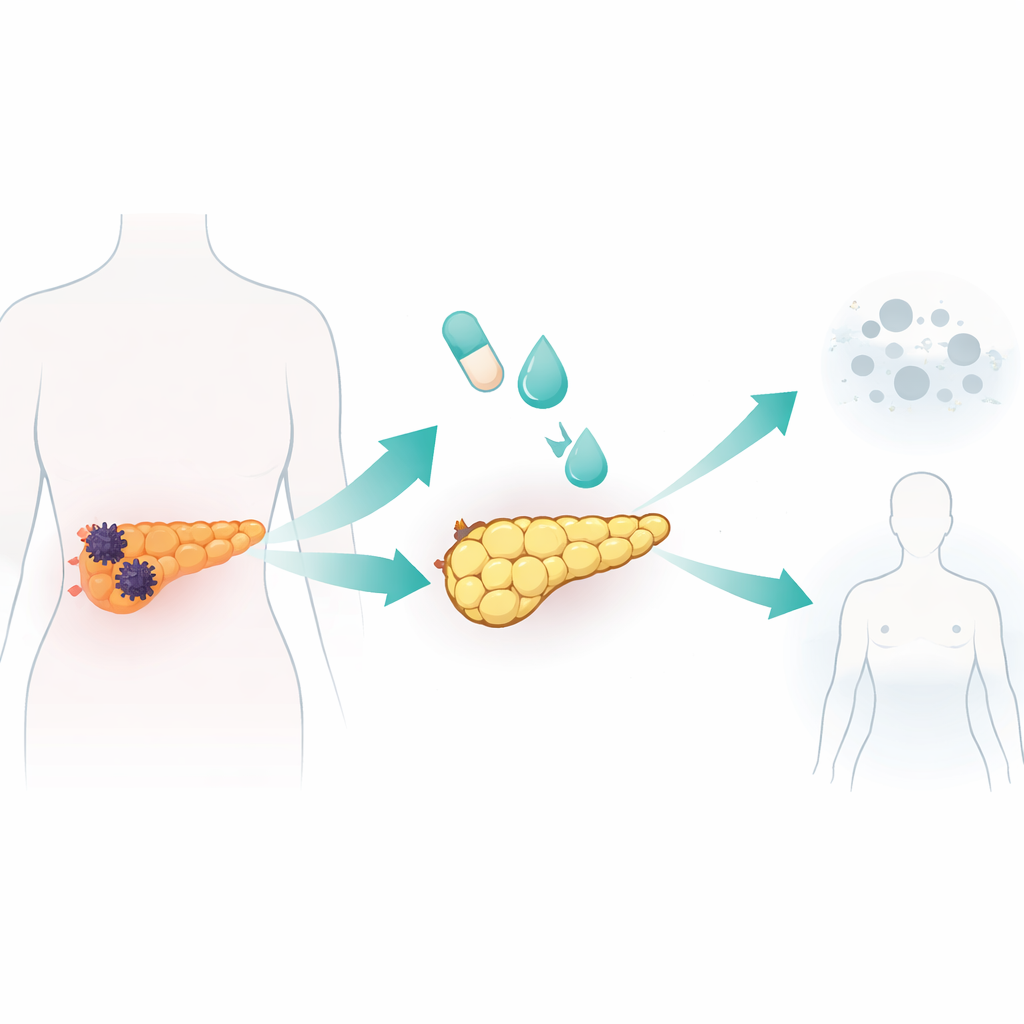
Перенаправление раковых клеток в жировые клетки в лаборатории
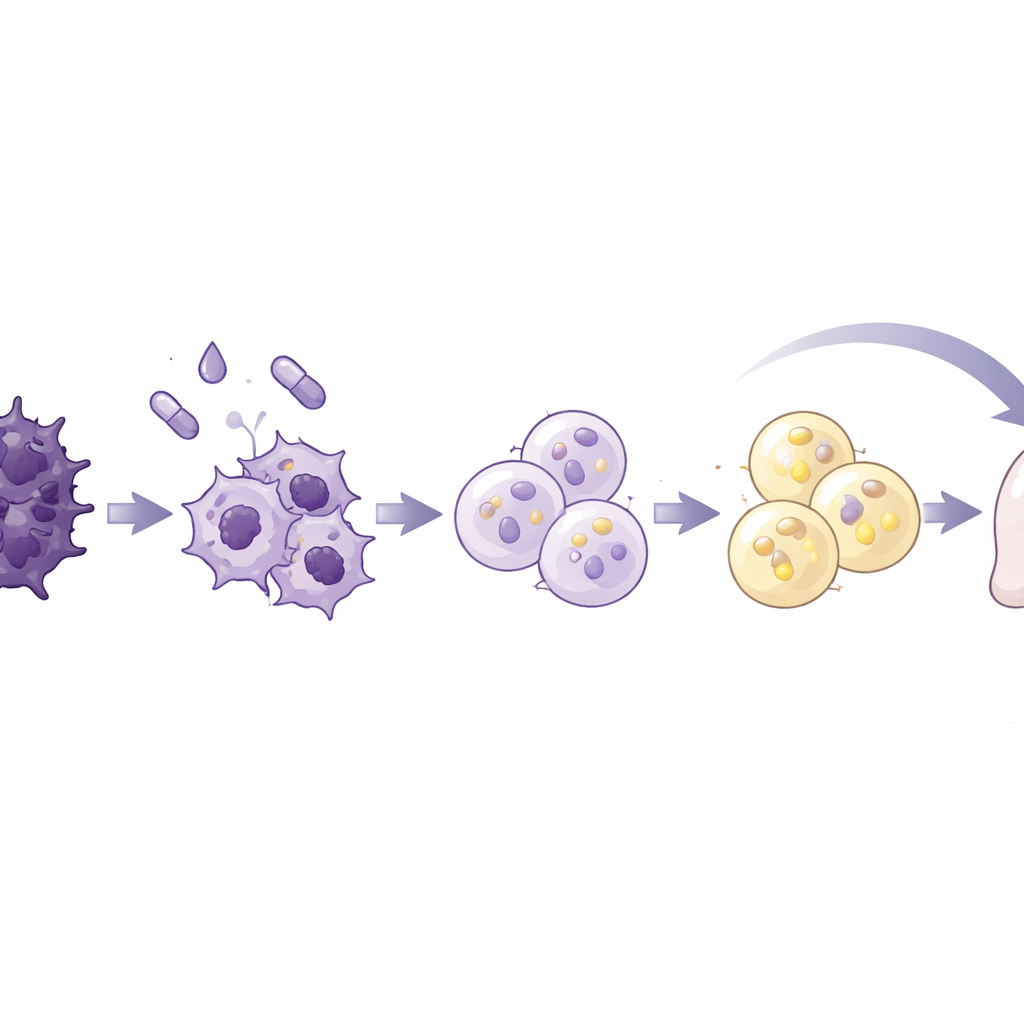
Команда испытала стандартный коктейль для индукции адипогенеза, применявшийся ранее в исследованиях жировой биологии и рака молочной железы, на семи линиях человеческих клеток рака поджелудочной и одной нормальной линии клеток поджелудочной. Смесь включала инсулин и стероид вместе с розиглитазоном — препаратом, активирующим главный регулятор жировой дифференцировки, а также белок‑сигнальную молекулу BMP2, чтобы разблокировать клеточную пластичность. Одна из линий раковых клеток, называемая AsPC‑1, оказалась особенно чувствительной. В течение десяти дней эти клетки становились крупнее и более округлыми, заполнялись липидными каплями — типичными признаками жировых клеток. Они включали гены и белки, характерные для зрелых адипоцитов, демонстрировали активный жировой метаболизм, выделяли адипонектин и реагировали на сигналы расщепления запасов липидов. Что важно, преобразованные клетки прекратили пролиферацию, остановились в ранней фазе клеточного цикла и значительно снизили подвижность и инвазии по сравнению с необработанными раковыми клетками.
Выключение ракового программы в глубине клетки
Чтобы понять молекулярные изменения, исследователи профилировали упаковку ДНК и активность генов в преобразованных клетках. Они обнаружили широкое уплотнение хроматина — комплекса ДНК и белков, контролирующего доступ к генам, — а также глобальное снижение экспрессии генов, что характерно для неделящихся клеток. Гены, поддерживающие EMT, инвазию и метастазирование, включая матрикс‑разрушающие ферменты и ключевые регуляторы EMT, были сильно репрессированы, тогда как адипоцит‑связанные гены усилили экспрессию. Общий генный профиль сместился от мезенхимальной, высокоподвижной идентичности к состоянию, близкому к зрелым жировым клеткам. Сигналы, связанные с ростом клеток и ответом на важный индуктор EMT — TGF‑бета, были ослаблены, в то время как пути, связанные с обработкой липидов и клеточной адгезией, были усилены. Эти изменения указывают на то, что клетки не просто замедлились, а были фундаментально перепрограммированы.
Проба стратегии на мышах
Далее ученые проверили, поможет ли вынужденная конверсия в жировые клетки контролировать опухоли в живых организмах. Они имплантировали человеческие клетки рака поджелудочной в поджелудочную железу или селезенку мышей, моделируя первичные опухоли и метастазы в печени. У мышей, получавших розиглитазон и BMP2, развивались меньшие панкреатические опухоли с более богатыми липидными каплями и маркерами жировых клеток внутри опухолей, а также с пониженным уровнем генов EMT и инвазии. В модели метастазирования лечение не меняло начального закрепления опухолевых очагов, но со временем замедляло наращивание опухолевой нагрузки в печени по сравнению с не леченными животными. Важно, что соседние нормальные ткани поджелудочной не демонстрировали явной конверсии в жировые клетки, а жировое состояние в опухолях сохранялось по крайней мере в течение месяца после прекращения приема препаратов, что свидетельствует о стойкости и избирательности эффекта.
Что это может означать для будущей онкологии
Исследование поддерживает провокационную концепцию: для высокопластичных, богатых EMT раков поджелудочной может быть возможным «превращать вместо уничтожать», перенаправляя опасные, мигрирующие опухолевые клетки в стабильные, неделящиеся клетки, похожие на адипоциты, которые хуже распространяются. Хотя это работа ранней стадии, выполненная на клетках и моделях на мышах, и не все опухоли поджелудочной одинаково отзывчивы, она открывает новый терапевтический путь, действующий через изменение клеточной идентичности, а не просто блокирование сигнала роста. В будущем такие подходы к транслдифференцировке могут комбинироваться с таргетной терапией или иммунотерапией, чтобы удерживать рак поджелудочной в более тихом, управляемом состоянии и снижать риск летальных метастаз.
Цитирование: Qian, Y., Yan, Z., Wang, J. et al. Adipogenic transdifferentiation reprograms EMT-high PDAC cells into a post-mitotic adipocyte-like state and limits metastasis. Cell Death Dis 17, 330 (2026). https://doi.org/10.1038/s41419-026-08613-4
Ключевые слова: рак поджелудочной железы, клеточная пластичность, транслдифференцировка, эпителиально-мезенхимальный переход, клетки, похожие на адипоциты