Clear Sky Science · ru
Механизм обратной связи от клеток рака простаты к макрофагам, усиленный STAT1, регулирует прогрессирование опухоли и устойчивость к радиотерапии
Почему это исследование важно
Радиотерапия — ключевой метод лечения рака простаты, однако многие опухоли со временем перестают на неё реагировать, что позволяет болезни возвращаться или распространяться. В этом исследовании выявлена скрытая химическая «переписка» между клетками рака простаты и соседними иммунными клетками — макрофагами, которая помогает опухолям выживать после облучения. Расшифровав этот цикл, исследователи выделили новые мишени для лекарств, которые могли бы повысить эффективность радиотерапии у мужчин с прогрессирующим раком простаты.
Клетки рака, которые иначе сжигают сахар
Клетки рака простаты, как и многие опухоли, опираются на изменённую форму утилизации сахара, известную как аэробный гликолиз. Вместо того чтобы полностью окислять сахар с помощью кислорода, они выбирают более быстрый, но менее эффективный путь, который приводит к образованию больших количеств молочной кислоты. Исследователи идентифицировали внутри опухолевых клеток белок STAT1 как ключевой переключатель, который включает это состояние повышенного «аппетита» к сахару. STAT1 усиливает активность трёх основных ферментов, управляющих гликолизом, увеличивая как захват сахара, так и производство молочной кислоты. В культурах клеток и на моделях мышей опухоли с повышенным уровнем STAT1 росли быстрее и были более устойчивы к радиации, тогда как блокирование гликолиза ослабляло эти агрессивные черты. 
Как «отходы» опухоли перекраивают иммунные клетки
Молочная кислота часто рассматривается как метаболический «отход», но в микроокружении опухоли она действует скорее как сигнальная молекула. Исследователи показали, что молочная кислота, выделяемая клетками рака простаты, захватывается макрофагами через мембранный переносчик MCT1. Попав внутрь, эта кислота активирует внутриклеточную систему тревоги, известную как путь NFκB, что направляет макрофаги в поддерживающее состояние M2. Вместо того чтобы атаковать рак, макрофаги типа M2 склонны подавлять иммунные ответы и поддерживать рост опухоли, например стимулируя образование кровеносных сосудов. Когда учёные блокировали гликолиз в раковых клетках, подавляли образование молочной кислоты или препятствовали её поступлению в макрофаги, эти иммунные клетки переключались с опухоль-поддерживающего состояния M2 к более оборонительному профилю.
Макрофаги посылают сигналы роста обратно опухоли
История не заканчивается простым изменением характера макрофагов. После активации NFκB внутри них макрофаги начинают синтезировать и секретировать мощную сигнальную молекулу MCP-1. Эта молекула диффундирует обратно к клеткам рака простаты и связывается с клеточной поверхностной рецепторной молекулой под названием CCR2. Такое связывание включает ещё один внутриклеточный путь в раковых клетках, с участием белков JAK и STAT1. Иными словами, тот самый STAT1, который изначально запустил усиленный гликолиз, снова включается сигналом, который в конечном счёте восходит к молочной кислоте, которую он помог создать. Когда команда добавляла MCP-1 к клеткам рака простаты, гликолиз усиливался, клетки быстрее росли и мигрировали, а также эффективнее восстанавливали повреждения ДНК, вызванные радиацией. Блокирование CCR2 или JAK предотвращало эти эффекты.
Самоусиливающаяся петля выживания
В сумме результаты показывают самоусиливающуюся петлю между клетками опухоли и макрофагами. STAT1 внутри клеток рака простаты усиливает расщепление сахара и выделение молочной кислоты. Эта молочная кислота импортируется в макрофаги, где активирует NFκB и переводит их в опухоль-поддерживающее состояние M2, одновременно вызывая производство MCP-1. MCP-1 затем возвращается к раковым клеткам, активирует CCR2 и путь JAK/STAT1 и ещё больше укрепляет гликолиз и устойчивость к радиотерапии. Эксперименты на животных показали, что препараты, блокирующие CCR2 или JAK, особенно в сочетании с облучением, замедляли рост опухоли и снижали количество макрофагов M2, подчёркивая клинический потенциал нацеливания на этот контур. 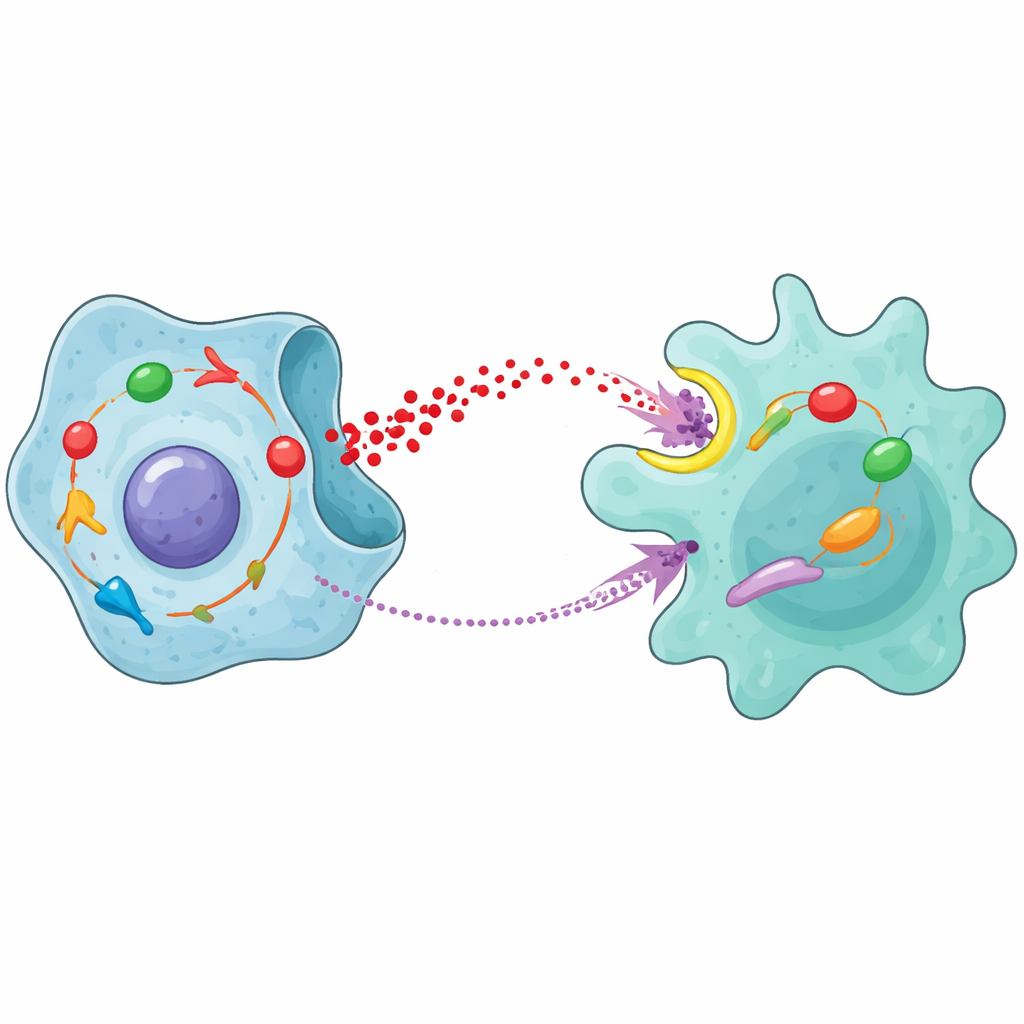
Что это значит для пациентов
Для неспециалиста ключевая идея такова: опухоли простаты и определённые иммунные клетки формируют химическое партнёрство, которое помогает раку переживать радиотерапию. Опухолевые клетки меняют способы использования сахара, производя молочную кислоту, которая перепрограммирует соседние макрофаги в союзников вместо врагов. Эти перепрограммированные клетки затем посылают сигналы обратно, делая опухоли более жёсткими и труднокишемыми для уничтожения. Прерывая эту петлю — на уровне обработки молочной кислоты, сигнала MCP-1 или нижестоящего пути JAK/STAT1 — будущие терапии могли бы ослабить защиту опухоли и позволить радиотерапии работать эффективнее, давая новую надежду мужчинам с трудно излечимым раком простаты.
Цитирование: Chen, JY., Xue, YT., Lin, B. et al. A feedback mechanism from prostate cancer cells to macrophages, reinforced by STAT1, regulates tumor progression and resistance to radiotherapy. Cell Death Dis 17, 282 (2026). https://doi.org/10.1038/s41419-026-08577-5
Ключевые слова: рак простаты, устойчивость к радиотерапии, опухолевая микроокружение, макрофаги, метаболизм лактата