Clear Sky Science · ru
HNRNPH1 стимулирует прогрессирование глиобластомы, регулируя сплайсинг генов клеточного цикла
Почему это исследование рака мозга важно
Глиобластома — одна из самых смертельных форм рака мозга, отчасти потому, что её клетки быстро делятся и при этом умеют избегать самоуничтожения. В этом исследовании раскрывается, как малоизвестная молекула внутри опухолевых клеток помогает им сохранять упорядоченное деление вместо того, чтобы разрушиться. Обнажив эту скрытую систему поддержки, работа указывает на новые пути, которыми врачи могли бы однажды заставить клетки глиобластомы перейти грань и остановить рост опухолей.
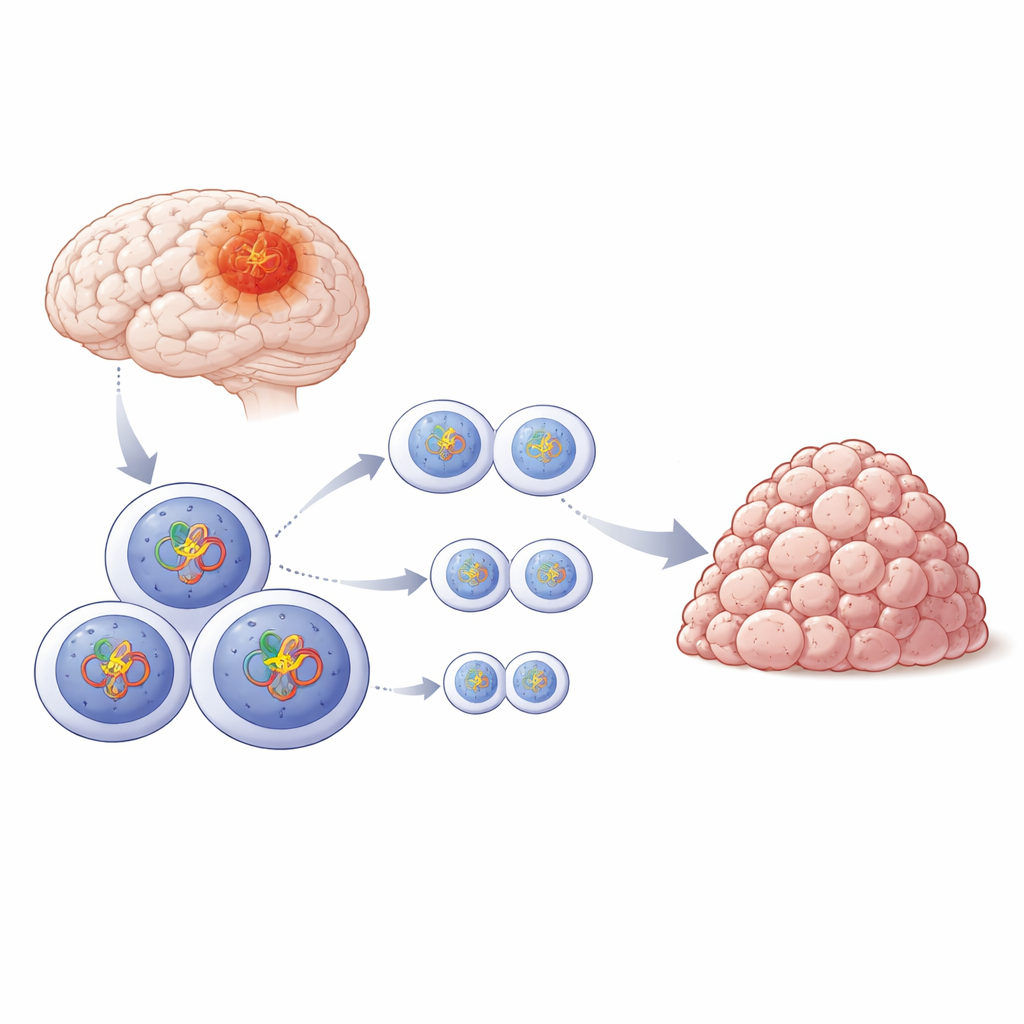
Скрытый помощник внутри опухолевых клеток
Исследователи сосредоточились на глиобластоме — агрессивной опухоли мозга, которая часто устойчива к операции, облучению и химиотерапии. Раковые клетки обычно несут множество мутаций в ДНК, заставляющих их делиться, но при этом им по-прежнему нужна целая машина для копирования и разделения хромосом в каждом цикле деления. Если эта машина дает сбой, клетки могут погибнуть в процессе, называемом «митотической катастрофой». Команда задала вопрос, какие молекулярные участники помогают клеткам глиобластомы сохранять этот хрупкий процесс деления, несмотря на поврежденные геномы.
Регулятор движения для генетических сообщений
Учёные сосредоточили внимание на белке под названием HNRNPH1, входящем в семейство молекул, связывающих РНК — краткоживущие сообщения, копируемые с ДНК. Эти белки помогают решать, как необработанные РНК-транскрипты разрезаются и сшиваются перед тем, как превратиться в белки, в процессе, известном как сплайсинг. Анализ больших наборов данных пациентов и образцов опухолей показал, что HNRNPH1 синтезируется в тканях глиобластомы значительно выше, чем в нормальном мозге. Одноклеточное и пространственное картирование показало, что он особенно богат в опухолевых клетках, напоминающих незрелые, быстро делящиеся клетки мозга, и в хорошо оксигенированных, высокопролиферативных областях опухоли, но значительно ниже в бедных кислородом, стрессовых зонах.
Как HNRNPH1 поддерживает правильное деление клеток
Чтобы выяснить, что происходит при удалении HNRNPH1, команда использовала генное редактирование и РНК-интерференцию, чтобы уменьшить уровни этого белка в культуре клеток глиобластомы. Это вызвало масштабные изменения в активности тысяч генов, с особенно сильным воздействием на те, которые контролируют контрольную точку G2/M — финальный этап проверки качества перед делением клетки. Было обнаружено, что HNRNPH1 непосредственно связывается с РНК-предписаниями нескольких ключевых регуляторов деления, включая белки, помогающие правильному разделению хромосом. При потере HNRNPH1 эти РНК неправильно сплайсировались или синтезировались в меньших количествах, что приводило к дефициту белков, необходимых для упорядоченной митоза.
Когда помощника нет, деление клеток нарушается
Клетки, лишённые HNRNPH1, замедляли рост, накапливались на поздних стадиях клеточного цикла и развивали увеличенные, деформированные или фрагментированные ядра — классические признаки нарушенного деления. Под микроскопом было меньше клеток, находящихся в нормальной митозе, и их внутренняя «опора» для разделения хромосом была нарушена. Команда также обнаружила, что HNRNPH1 направляет сплайсинг ещё одного регулятора, UHRF2, переключая его РНК между продуктивной и дефектной формами. Без HNRNPH1 больше сообщений UHRF2 было неправильно отредактировано, что снижало количество функционального белка и ещё сильнее нарушало контроль клеточного цикла.
Доказательства из опухолей в живых головах
Затем учёные проверили значимость HNRNPH1 в моделях на мышах. Они имплантировали человеческие клетки глиобластомы, либо нормальные, либо с пониженным уровнем HNRNPH1, в головной мозг мышей. Животные, получившие контрольные клетки, быстро развивали большие опухоли и умирали раньше. Мыши, получившие клетки с пониженным HNRNPH1, развили значительно меньшие или отложенные опухоли и жили дольше. Однако опухоли, которые в конечном итоге выросли, снова восстановили активность HNRNPH1, что указывает на то, что клетки, не сумевшие восстановить этот белок, оказались в сильном невыгодном положении и не могли поддерживать рост опухоли.
Что это значит для будущего лечения
В целом исследование показывает, что клетки глиобластомы зависят от HNRNPH1 для правильной обработки сети генетических сообщений, управляющих делением клеток, что позволяет им пролиферировать, не уничтожая себя немедленно. Для неспециалиста этот белок можно представить как закулисного редактора, который делает инструкцию клетки рака читаемой. Нарушение HNRNPH1 — или конкретных событий сплайсинга, которые он контролирует — могло бы сделать опухолевые клетки более уязвимыми к фатальным ошибкам при делении, открывая потенциально новый маршрут для терапии, который подталкивает глиобластому за её предельную точку, дополняя существующие методы лечения.
Цитирование: Villa, G.R., Alimonti, P., Toker, J.S. et al. HNRNPH1 drives glioblastoma progression by regulating the splicing of cell cycle genes. Cell Death Dis 17, 352 (2026). https://doi.org/10.1038/s41419-026-08576-6
Ключевые слова: глиобластома, клеточный цикл, сплайсинг РНК, биология опухолей, рак мозга