Clear Sky Science · ru
Ингибирование вакциниоподобной киназы 2 выявляет уязвимость метаболизма глутатиона при раке поджелудочной железы
Почему это важно для рака поджелудочной железы
Рак поджелудочной железы — один из самых смертельных видов рака, отчасти потому что стандартные методы лечения часто оказываются неэффективны. В этом исследовании выявлена скрытая слабость у некоторых опухолей поджелудочной железы: зависимость от клеточного «щита» против токсичных продуктов кислородного метаболизма. Поняв, когда этот щит уязвим, и как он укрепляется с помощью онкогена VRK2, авторы предлагают новые способы избирательно отравлять раковые клетки, не повреждая здоровую ткань.
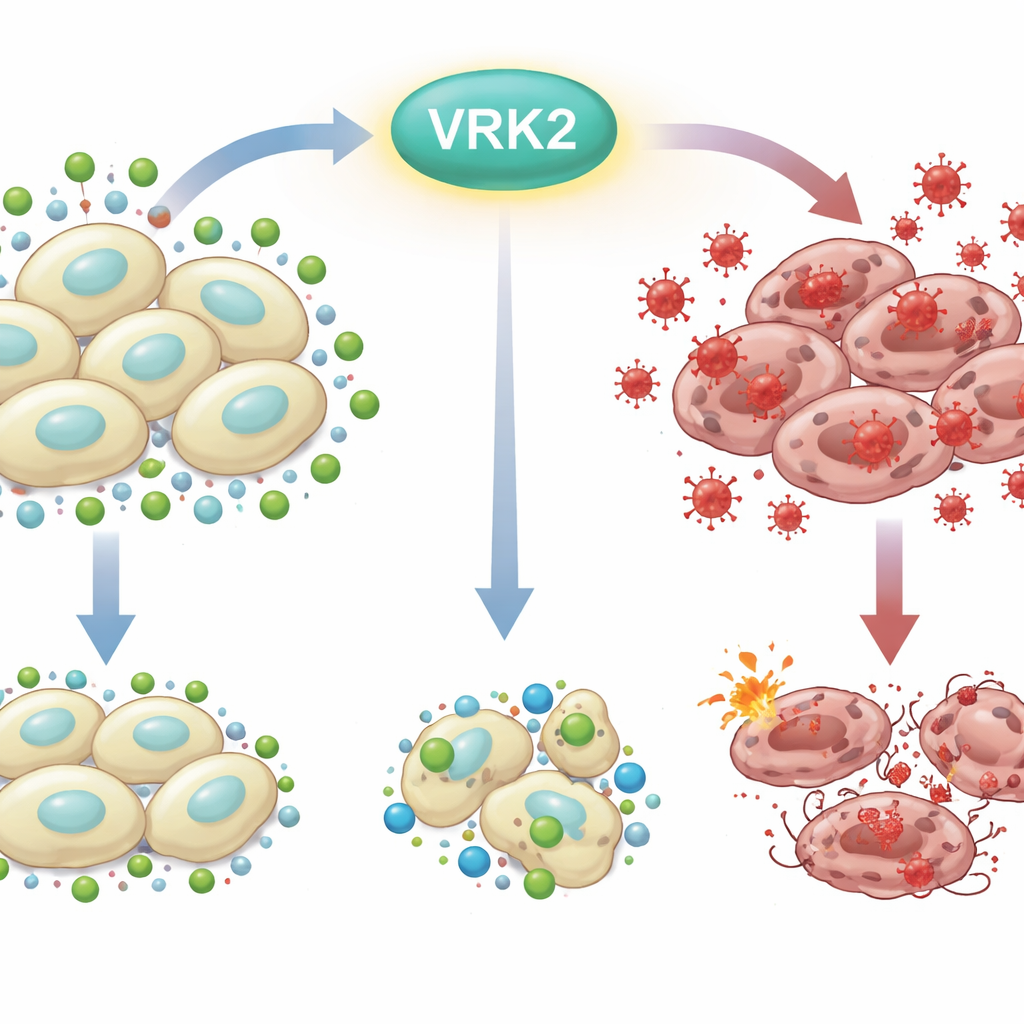
Проблема «ржавчины» в клетке
Каждая клетка постоянно борется с «ржавлением изнутри», вызванным реактивными формами кислорода — высокореактивными формами кислорода, способными повреждать ДНК, липиды и белки. Для выживания клетки используют химические защиты, и глутатион является одним из важнейших щитов. Клетки рака поджелудочной железы, которые существуют в суровых условиях и быстро растут, сильно опираются на метаболические уловки, чтобы поддерживать достаточный уровень глутатиона. Нарушение равновесия между разрушительными окислителями и защитными антиоксидантами может привести к гибели раковых клеток.
Поиск скрытой уязвимости
Исследователи начали с выключения VRK2 — гена, способствующего развитию рака и ранее связанного с плохим прогнозом при раке поджелудочной железы — и затем протестировали 281 соединение, нацеленное на метаболизм. Они обнаружили, что клетки без VRK2 особенно чувствительны к препаратам, блокирующим синтез глутатиона. В этих клетках уровни глутатиона падали, а реактивные формы кислорода резко увеличивались, что приводило к гибели клеток. Добавление дополнительных антиоксидантов или молекул, подобных глутатиону, спасало клетки, подтверждая, что ключевая уязвимость заключалась именно в нарушенной способности детоксифицировать окислительный стресс.
Как VRK2 помогает клеткам «облачиться в броню»
Далее команда выясняла, почему VRK2 влияет на метаболизм глутатиона. Они сосредоточились на транспортёре SLC7A11, который расположен в плазматической мембране и ввозит цистин — строительный блок для синтеза глутатиона. Удивительно, но VRK2 не менял общий уровень продукции SLC7A11; вместо этого он контролировал, попадает ли этот транспортёр на поверхность клетки. В нормально функционирующих клетках с активным VRK2 SLC7A11 перемещается из эндоплазматического ретикулума в аппарат Гольджи, а затем к мембране. VRK2 усиливает этот трафик, химически модифицируя белок сортировки грузов Sec24C, который помогает загружать SLC7A11 в транспортные везикулы. Когда VRK2 отсутствует или блокирован, SLC7A11 застревает внутри клетки, на поверхность выходит меньше транспортёров, и защитный щит глутатиона ослабевает.
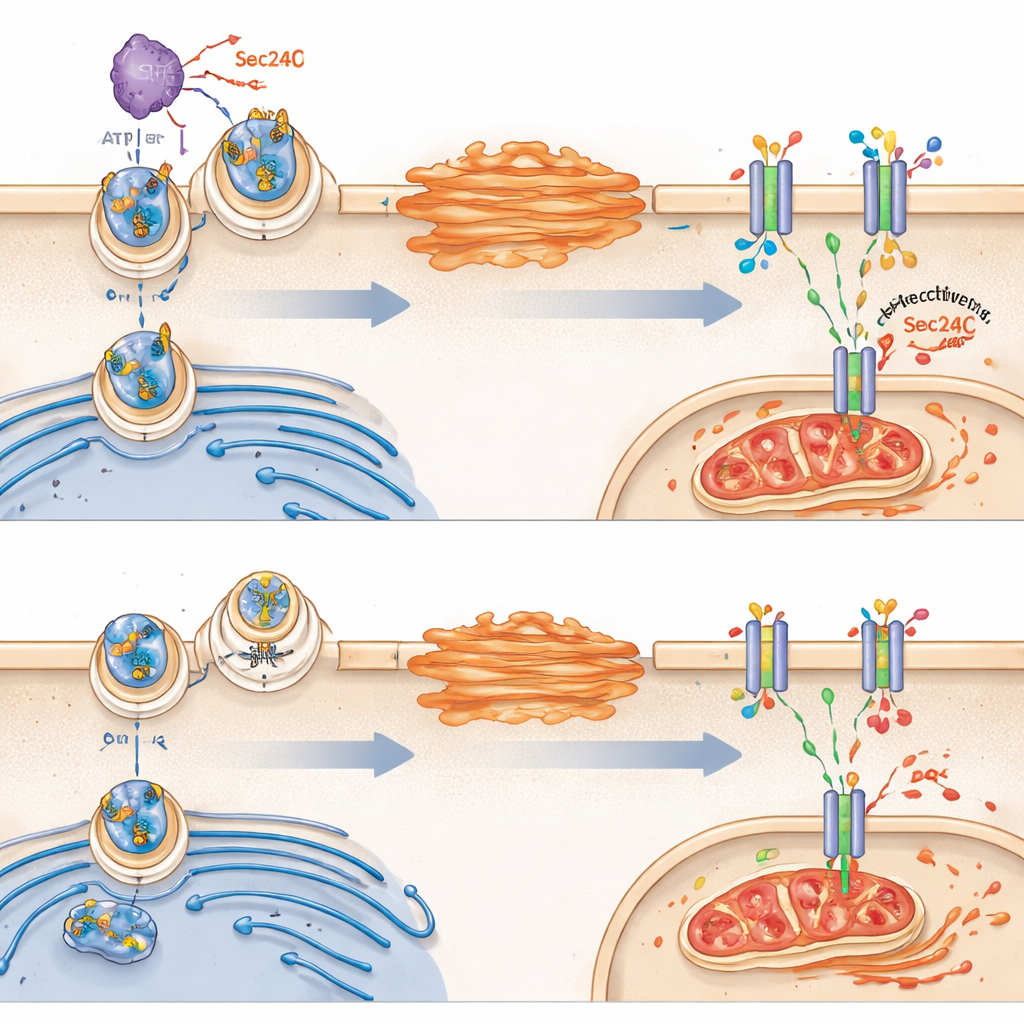
От сломанного щита до ферроптоза
Без достаточного количества SLC7A11 в мембране клетки, лишённые VRK2, испытывают трудности с поглощением цистина и поддержанием уровня глутатиона. Это делает их особенно уязвимыми к форме железозависимой смерти клетки, называемой ферроптозом, который характеризуется неконтролируемым окислением липидов мембраны и повреждением митохондрий. В исследовании показано, что препараты, блокирующие синтез глутатиона, вызывали признаки ферроптоза в VRK2-дефицитных клетках, включая деформацию митохондрий и накопление продуктов окисления липидов. Блокирование ферроптоза, но не других видов гибели клеток, защищало эти клетки, что подчёркивает: их ахиллесова пята — неспособность сдерживать окислительное повреждение.
Кому это может помочь при выборе персонализированной терапии
Наконец, исследователи провели опыты на животных моделях и на клетках, полученных непосредственно от пациентов. Опухоли с низким уровнем VRK2 уменьшались при лечении препаратом, нацеленным на глутатион, тогда как опухоли с высоким уровнем VRK2 в основном сопротивлялись ему. Однако при одновременном введении ингибитора VRK2 опухоли с высоким выражением VRK2 вновь становились чувствительны к подавлению глутатиона. Это свидетельствует о том, что уровень VRK2 может разделять пациентов на группы: те, чьи опухоли изначально уязвимы к терапии, нацеленной на глутатион, и те, кто может выиграть от двухэтапной стратегии — сначала блокировка VRK2, затем атака на метаболизм глутатиона.
Что это означает для пациентов
Проще говоря, работа показывает, что некоторые раки поджелудочной железы выживают благодаря VRK2, который поддерживает их антиоксидантный щит. Убрать VRK2 — и щит истончается; дополнительно лишить клетки глутатиона — и раковые клетки рухнут под ударом окислительного стресса. Измерение уровня VRK2 в опухолях могло бы помочь врачам решить, кто с наибольшей вероятностью получит пользу от препаратов, нарушающих метаболизм глутатиона, а кому сначала потребуется блокировка VRK2. Хотя нужны дополнительные клинические испытания, исследование намечает ясный путь к более целенаправленным, основанным на метаболизме методам лечения для рака, которому крайне необходимы лучшие варианты терапии.
Цитирование: Chen, S., Fu, X., Zhang, T. et al. Vaccinia-related kinase 2 inhibition elicits vulnerability of glutathione metabolism in pancreatic cancer. Cell Death Dis 17, 325 (2026). https://doi.org/10.1038/s41419-026-08573-9
Ключевые слова: рак поджелудочной железы, метаболизм глутатиона, VRK2, ферроптоз, SLC7A11