Clear Sky Science · ru
Подавление EGFR новым бигуанидом 4C усиливало чувствительность рака яичников к ингибиторам PARP за счёт понижения BRCA2 и Rad51
Почему это исследование важно
У многих людей с диагнозом рак яичников современные таргетные препараты эффективны лишь у небольшой части пациентов, чьи опухоли несут определённые генетические дефекты. В этом исследовании изучается способ расширить пользу важного класса лекарств — ингибиторов PARP — на гораздо большую группу пациентов, у которых такие мутации отсутствуют. Сочетая новый экспериментальный препарат с уже существующими средствами, исследователи демонстрируют стратегию, которая загоняет раковые клетки в фатальный тупик, при этом щадя здоровые ткани.
Препятствие в текущем лечении рака яичников
Рак яичников часто обнаруживают на поздних стадиях и он остаётся одним из самых смертельных злокачественных заболеваний у женщин. Ингибиторы PARP, такие как олапариб, могут быть исключительно эффективны, но преимущественно у пациентов, чьи опухоли уже имеют дефекты в пути репарации ДНК, связанном с генами BRCA1 и BRCA2. Большинство опухолей при этом сохраняют работоспособный механизм восстановления и способны исправлять повреждения ДНК, вызванные этими препаратами, что позволяет раковым клеткам выживать. Ключевую роль в этой системе играют два белка — BRCA2 и Rad51, которые помогают восстанавливать разрывы в ДНК посредством гомологичной рекомбинации. Поиск способов избирательно ослабить этот путь в раковых клетках мог бы сделать ингибиторы PARP эффективными для гораздо большего числа пациентов.
Роль хорошо известного регулятора роста
Команда сосредоточилась на привычной для онкологии молекуле — рецепторе эпидермального фактора роста (EGFR), который находится на поверхности многих опухолевых клеток и стимулирует их рост. Они обнаружили, что EGFR делает не только сигналы роста: в клетках рака яичников с нормальными генами BRCA высокий уровень EGFR коррелировал с плохим выживаемостью пациентов и устойчивостью к ингибиторам PARP. Когда уровень EGFR снижали или подавляли в культурах клеток и у мышей, опухоли становились гораздо более уязвимыми к олапарибу. Исследователи показали, что EGFR способствует перемещению BRCA2 и Rad51 в ядро клетки после повреждения ДНК, где эти белки могут восстанавливать разрывы и ослаблять эффект лечения. Простое блокирование ферментной активности EGFR было недостаточно — для существенного нарушения этого пути репарации нужно было уменьшить общий уровень белка EGFR.
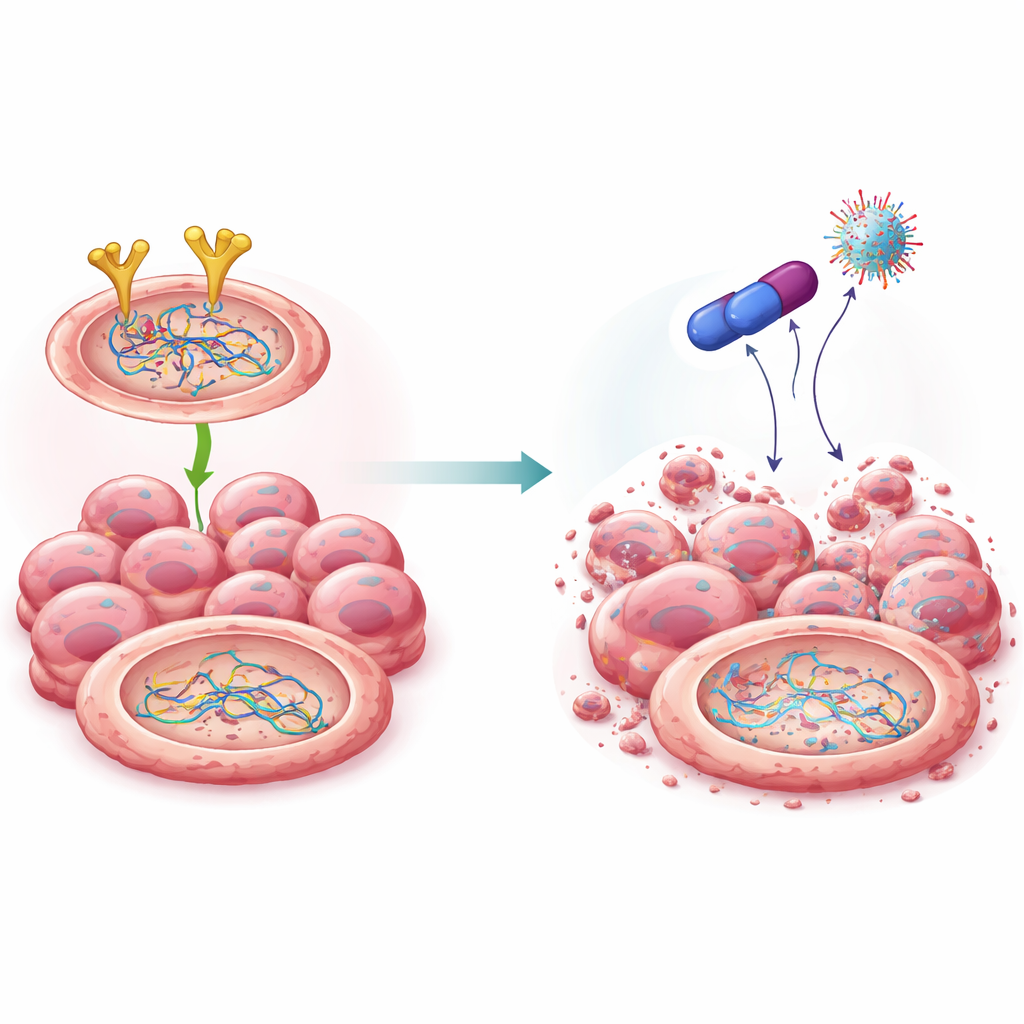
Новое соединение, лишающее защитников репарации их силы
Опираясь на предыдущие работы с классом препаратов — бигуанидов, учёные синтезировали несколько химических аналогов и выделили одно выдающееся соединение, названное 4C. Это вещество оказалось сильно токсичным для клеток рака яичников, но относительно щадящим для нормальных клеток. Молекулярное моделирование и лабораторные тесты показали, что 4C непосредственно связывается с EGFR и помечает его для утилизации в протеасомной системе клетки. В отличие от некоторых существующих препаратов против EGFR, 4C снижал общий уровень белка EGFR, а не просто подавлял его активность. По мере падения уровня EGFR стабильность BRCA2 и Rad51 также уменьшалась: они помечались для удаления, разрушались и теряли способность обеспечивать эффективную репарацию ДНК. Важно, что это «подрезание» происходило на уровне белков, без изменения самих генов.
Блокирование пути спасения внутри клетки
Исследование выявило более детальную цепочку событий, связывающих повреждение ДНК с выживанием опухоли. После того как ингибиторы PARP повреждают ДНК, другой сенсорный белок ATM посылает сигнал из ядра в цитоплазму. В ответ EGFR объединяется с BRCA2 и Rad51 и помогает им переместиться в ядро, где они осуществляют ремонт. Исследователи обнаружили, что третий белок, c-Cbl, обычно действует как нечто вроде «тегировщика» для утилизации BRCA2 и Rad51. EGFR конкурирует с c-Cbl за доступ к этим белкам репарации, защищая их от пометок на разрушение. Когда 4C снижает уровень EGFR, c-Cbl получает более лёгкий доступ к BRCA2 и Rad51, что приводит к их пометке, расщеплению и исчезновению. При сокращении числа белков репарации в ядре повреждённая ДНК накапливается, и раковые клетки становятся гораздо более чувствительны к ингибиторам PARP.
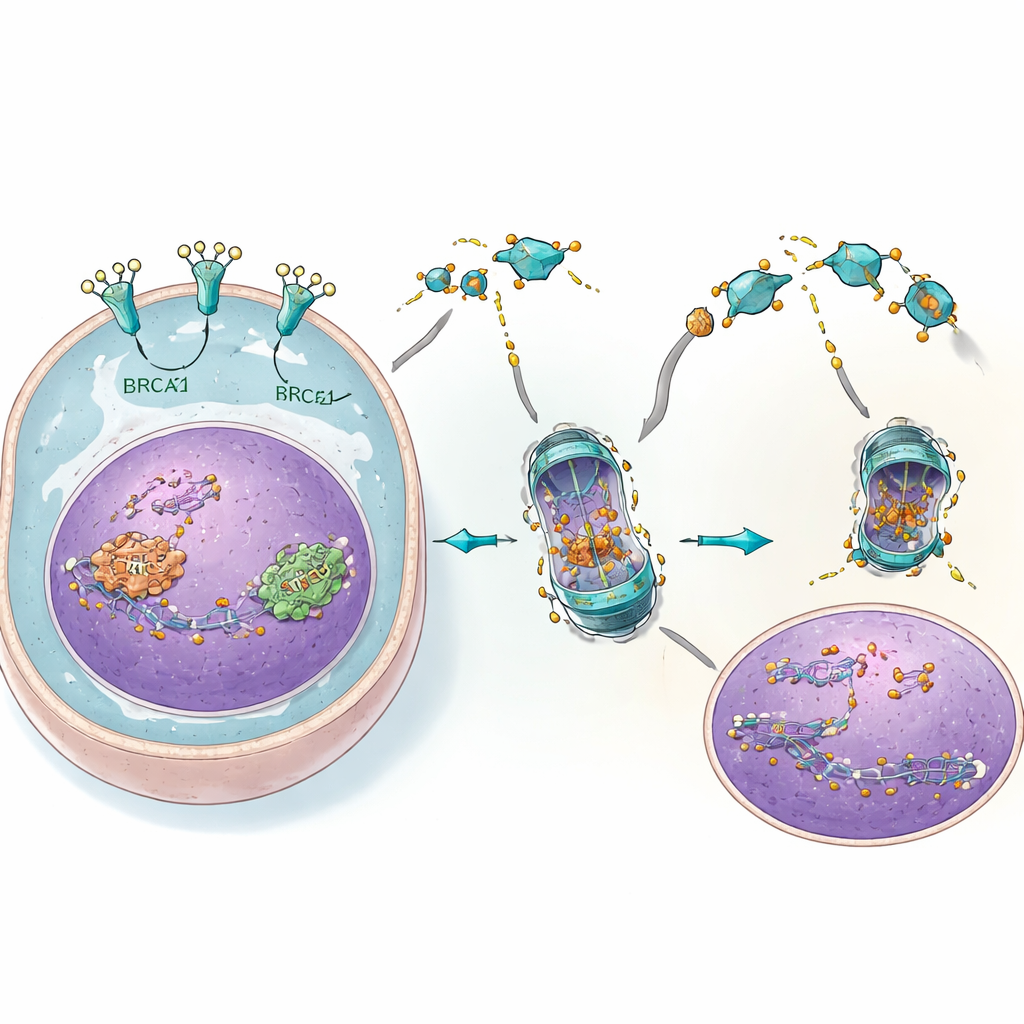
От клеток до животных: мощная комбинация
В культурах клеток и модельных системах на мышах сочетание 4C с ингибиторами PARP давало мощный комбинированный эффект. Опухоли с нормальными генами BRCA, устойчивые к каждому из препаратов по отдельности, заметно уменьшались или прекращали расти при одновременном применении обеих средств. Маркёры повреждения ДНК резко возрастали, что согласуется с идеей о перегрузке репарационных механизмов. При этом нормальные клетки и важные органы, такие как печень и почки, почти не демонстрировали признаков повреждения, вероятно, потому что у них значительно более низкий уровень EGFR и они меньше зависят от этого конкретного «резервного» пути репарации. Комбинация также снижала способность клеток рака яичников распространяться по организму.
Что это может значить для пациентов
Эта работа предлагает способ обратить силу раковой клетки против неё самой. Нацеливаясь на EGFR с помощью нового соединения 4C, исследователи лишают BRCA2 и Rad51 их защитной роли, заставляя опухоли с сохранённой системой репарации ДНК вести себя подобно BRCA-мутациям в ответе на ингибиторы PARP. Эта вынужденная уязвимость, известная как «синтетическая летальность», может расширить спектр применения существующих препаратов для большего числа женщин с раком яичников, сохраняя при этом управляемый профиль побочных эффектов. Хотя 4C остаётся экспериментальным и потребует обширной проверки в более продвинутых моделях и клинических испытаниях, исследование даёт чёткий план того, как разрушение конкретных помощников репарации в опухолевых клетках может улучшить результаты лечения.
Цитирование: Xiao, D., Yao, J., Yang, X. et al. Repression of EGFR by new biguanide 4C potentiated ovarian cancer to PARP inhibitors through down-regulation of BRCA2 and Rad51. Cell Death Dis 17, 317 (2026). https://doi.org/10.1038/s41419-026-08556-w
Ключевые слова: рак яичников, ингибиторы PARP, EGFR, репарация ДНК, таргетная терапия