Clear Sky Science · ru
Потеря PRKACB способствует метастазированию диффузного рака желудка через активацию сигнования RhoA
Почему это исследование важно для рака желудка
Диффузный рак желудка — особенно агрессивная форма рака желудка, которая часто широко распространяется внутри брюшной полости, затрудняя лечение и повышая смертность. Это исследование выясняет, почему такие опухоли склонны к распространению: обнаружен молекулярный «тормоз», который в норме сдерживает миграцию раковых клеток, и показано, что происходит при его отключении. Понимание этого скрытого контрольного переключателя может открыть новые возможности для прогнозирования пациентов с наивысшим риском и для разработки препаратов, замедляющих или останавливающих опасное распространение.
Опасная форма рака желудка
Не все раки желудка ведут себя одинаково. Интестинальный тип обычно образует более организованные массы, тогда как диффузный рак желудка (ДРЖ) состоит из разрозненных клеток, которые легко отделяются от первичной опухоли. У пациентов с ДРЖ риск смерти выше, чем у больных с интестинальным типом, отчасти потому, что их опухоли проще образуют новые очаги по всей брюшной полости. Ранние генетические исследования уже связывали ДРЖ с повторяющимися изменениями в гене RHOA, который влияет на подвижность и форму клеток. Однако оставалось неясным, как эти изменения вписываются в более широкие сигнальные сети, контролирующие — останутся ли раковые клетки на месте или начнут миграцию.
Поиск отсутствующего тормоза в образцах опухолей
Исследователи сосредоточились на белке PRKACB — каталитическом субъединице хорошо известного фермента протеинкиназы A, который регулирует множество клеточных процессов путем фосфорилирования других белков. Предварительное протеомное сканирование указало, что уровни PRKACB необычно низки в агрессивных образцах ДРЖ. Чтобы проверить это, команда изучила опухолевые образцы от 376 пациентов, сравнивая диффузный и интестинальный типы рака и прилежащие некарцинозные ткани. Они обнаружили, что уровни PRKACB значительно снижены в диффузных опухолях, особенно на поздних стадиях, но не в интестинальном типе. У пациентов с опухолями, содержащими мало PRKACB, общая выживаемость была существенно хуже, даже с учётом других клинических факторов, что указывает на роль PRKACB как опухолевого супрессора в этом контексте.
Как низкий уровень PRKACB способствует побегу клеток
Чтобы понять функцию PRKACB в раковых клетках, команда использовала культивируемые клеточные линии, моделирующие диффузный рак желудка. При искусственном снижении PRKACB клетки становились более подвижными и инвазивными в лабораторных тестах: они легче проталкивались через преграды и формировали пальцеобразные выросты — псевдоподии — которые помогают клеткам ползать. Эти клетки также переходили от более упорядоченного эпителиального состояния к более рыхлому мезенхимоподобному состоянию, связанному с метастазированием, теряя адгезионный белок E‑кадгерин, который обычно помогает клеткам удерживаться вместе. Наоборот, повышение уровня PRKACB делало клетки менее мигрирующими и менее инвазивными. Важно, что эти изменения не влияли на скорость деления клеток, что указывает на специфическую роль PRKACB в способствовании распространению, а не росту.
Внимание к переключателю сигнования RhoA
Исследователи затем спросили, как PRKACB обеспечивает свой антиметастатический эффект. С помощью методов выявления белок–белковых взаимодействий и структурного моделирования они показали, что PRKACB напрямую связывается с RhoA — молекулярным переключателем, который меняется между неактивной и активной формами, управляя формой и движением клетки. PRKACB фосфорилирует RhoA в конкретной позиции (серин 188), что ослабляет активность RhoA и снижает сигнализацию по путям ROCK и FAK, отвечающим за перестройку цитоскелета и подвижность клеток. При подавлении PRKACB уровень фосфорилирования RhoA уменьшался, RhoA становился более активным, а сигнализация ROCK/FAK усиливалась, что приводило к более агрессивной миграции клеток. В моделях на мышах, где человеческие опухоли имплантировали в стенку желудка, снижение PRKACB вызывало большее число и большие метастатические узлы в брюшной полости и более раннее появление видимого распространения, опять же без изменения скорости роста уже установившихся метастазов.
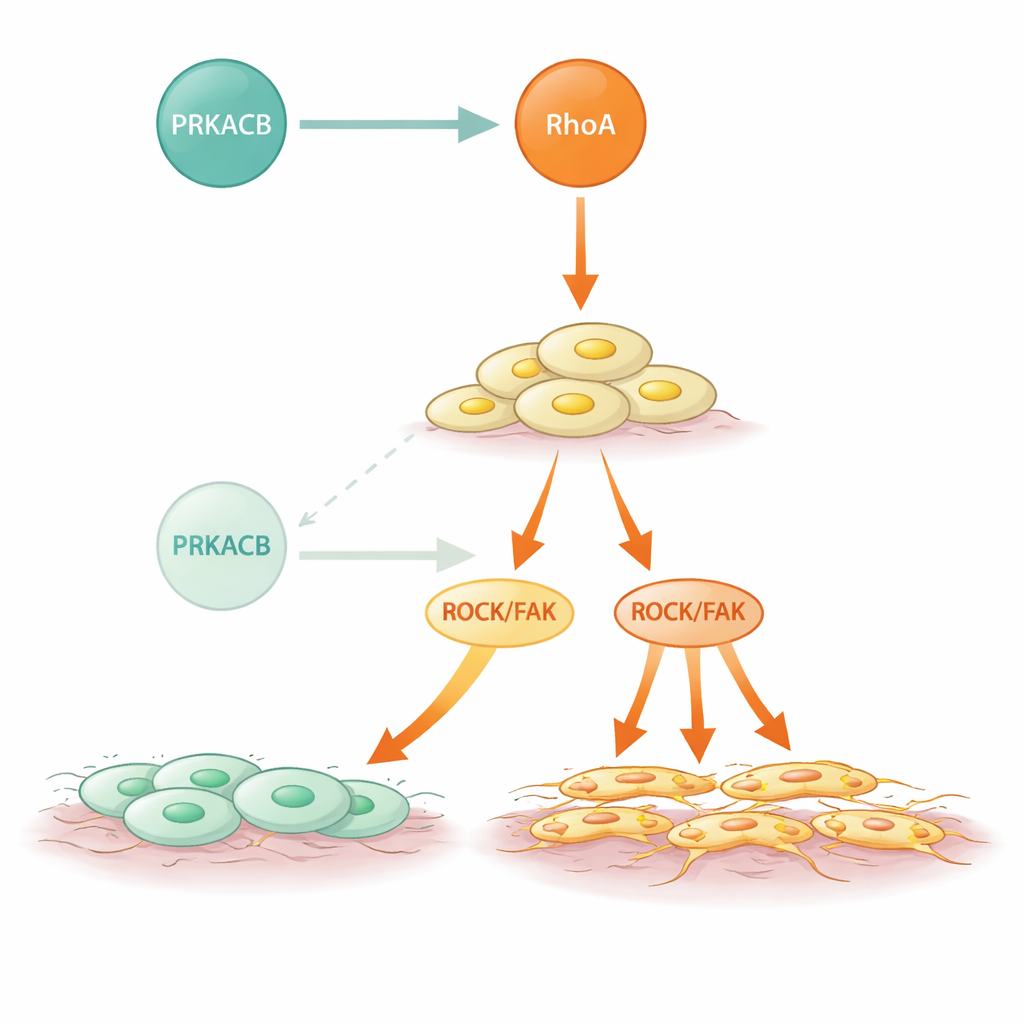
Мутантная сигнализация и возможный путь вмешательства
Диффузные раки желудка часто содержат мутации RHOA, и это исследование показывает, как некоторые из этих изменений усугубляют проблему. Несколько распространённых при ДРЖ мутаций в RhoA ослабляли или устраняли его связывание с PRKACB, но не нарушали способность RhoA активировать своих нижестоящих партнёров. В результате эти мутантные формы избегали тормозящей фосфорилирования PRKACB и демонстрировали повышенную активность ROCK и усиленное инвазивное поведение. Поразительно, что при обработке клеток и мышей соединением, блокирующим RhoA, дополнительное метастазирование, вызванное низким PRKACB, в значительной степени устранялось. Это говорит о том, что даже в опухолях, где природный «тормоз» ослаблен или отсутствует, непосредственная блокада сверхактивного пути RhoA может ограничить распространение.
Что это означает для пациентов и будущих терапий
Проще говоря, эта работа выделяет PRKACB как ключевой элемент внутренней «анти-миграционной» цепи в диффузном раке желудка. Когда уровни PRKACB падают, или когда RhoA мутирован так, что PRKACB не может с ним связаться и модифицировать его, сигнализация RhoA усиливается, и раковые клетки становятся более способными отделяться и колонизировать брюшную полость. Измерение статуса PRKACB и RhoA в опухолях может помочь врачам оценить вероятность метастазирования и определить, кто может получить наибольшую пользу от препаратов, ингибирующих путь RhoA–ROCK–FAK. Хотя такие методы лечения потребуют дальнейшей разработки и клинической проверки, исследование прокладывает чёткую молекулярную дорогу от отсутствующего «тормоза» к смертельному распространению — и указывает на новые способы замедлить этот процесс.
Цитирование: Sun, J., Zhao, J., Yang, X. et al. Loss of PRKACB facilitates metastasis of diffuse-type gastric cancer through RhoA signaling activation. Cell Death Dis 17, 281 (2026). https://doi.org/10.1038/s41419-026-08553-z
Ключевые слова: диффузный рак желудка, метастазирование, PRKACB, сигнализация RhoA, путь ROCK FAK