Clear Sky Science · ru
PD-1 защищает пролиферирующие человеческие Т-клетки от преждевременной гибели при повторной стимуляции, модулируя сигналы через TCR и CD28
Почему важно предотвращать «дружественный огонь» в иммунной системе
Наша иммунная система опирается на армии Т-клеток, которые быстро размножаются для борьбы с инфекциями и опухолями. Но это взрывное расширение опасно: если слишком много Т‑клеток остаются активными слишком долго, они могут повредить здоровые ткани или способствовать развитию аутоиммунных заболеваний. В этом исследовании рассматривается, как хорошо известный «тормоз» Т‑клеток — молекула PD‑1 — помогает пролиферирующим человеческим Т‑клеткам избегать преждевременной гибели в результате собственной чрезмерной активации. Понимание этого баланса важно для более безопасных иммунотерапий рака и для предотвращения вредных иммунных гиперреакций.
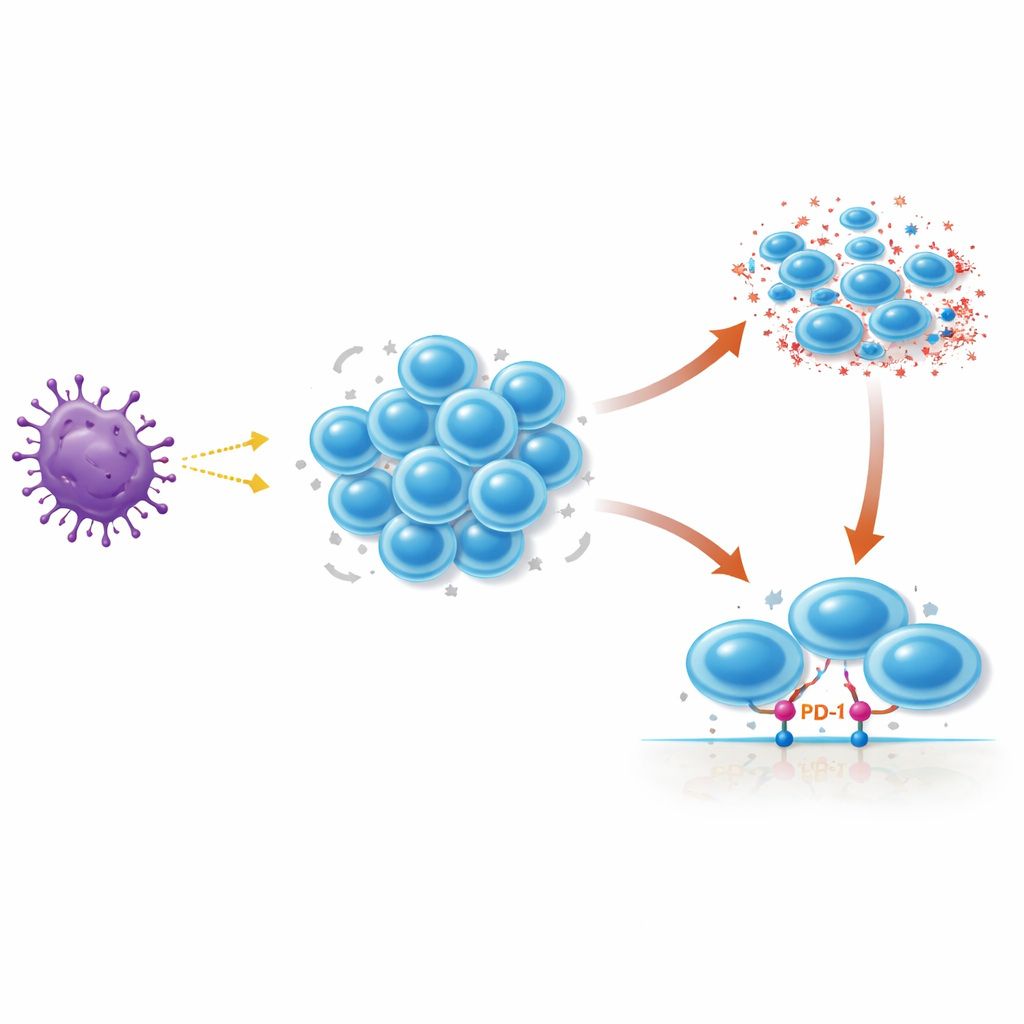
Встроенная программа самоуничтожения, требующая точного тайминга
Когда Т‑клетки распознают угрозу, они делятся, давая начало крупным клональным популяциям идентичных бойцов. Чтобы этот ответ не вышел из-под контроля, у Т‑клеток есть встроенная программа самоуничтожения — гибель, вызванная повторной стимуляцией (RICD). Если уже активированная Т‑клетка снова сильно стимулируется через свой основной сенсор — Т‑клеточный рецептор, — может включиться RICD и убить эту клетку. Это помогает сократить армию после устранения угрозы и предотвращает опасные лимфопролиферативные заболевания с чрезмерным накоплением Т‑клеток. Однако на ранних этапах ответа Т‑клеткам нужно время на экспансию перед тем, как этот путь самоуничтожения станет доминирующим, и механизм контроля этого тайминга у людей не был полностью ясен.
Неожиданная защитная сторона иммунного тормоза
PD‑1 известен как мишень «контрольных точек» в терапии рака: его блокада может пробудить истощённые Т‑клетки в опухолях. Традиционно PD‑1 рассматривают как молекулу, ослабляющую активность Т‑клеток, но PD‑1 быстро включается при первом контакте человеческих Т‑клеток со стимулом и остается на умеренном уровне в ходе их ранней экспансии. В этом исследовании учёные выделяли человеческие CD4 и CD8 Т‑клетки у здоровых доноров, активировали их в культуре и отслеживали PD‑1 и его лиганд PD‑L1 с течением времени. Они обнаружили, что PD‑1 и PD‑L1 достигают пика в течение нескольких дней после активации — как раз в период интенсивного размножения Т‑клеток — и затем снижаются по мере созревания клеток. При блокаде PD‑1 или PD‑L1 во время повторной стимуляции большее число Т‑клеток погибало, что указывает на то, что нормальный PD‑1‑зависимый сигнал на самом деле защищает эти пролиферирующие клетки от преждевременной RICD.
Как PD‑1 перестраивает «диалог» на поверхности клетки
Чтобы точнее исследовать эту защиту, учёные создали искусственные «заместительные» антиген‑представляющие частицы, покрытые активирующими сигналами (чтобы имитировать Т‑клеточный рецептор и его основного помощника CD28) и в некоторых случаях PD‑L1. Когда пролиферирующие Т‑клетки повторно стимулировали частицами с PD‑L1, погибало значительно меньше клеток по сравнению с контролем, а стандартные маркеры раннего и позднего апоптоза снижались к базовому уровню. Этот эффект выживания зависел от количества PD‑L1 и от его расположения прямо рядом с активирующими сигналами, что отражает плотную организацию естественной иммунной синапсы. Интересно, что защитный эффект был наиболее выражен при одновременном вовлечении CD28 и Т‑клеточного рецептора, что указывает на то, что PD‑1 одновременно сдерживает оба активационных пути. При отсутствии PD‑1 участие CD28 делало клетки более подверженными RICD, но добавление PD‑L1 устраняло эту повышенную чувствительность.
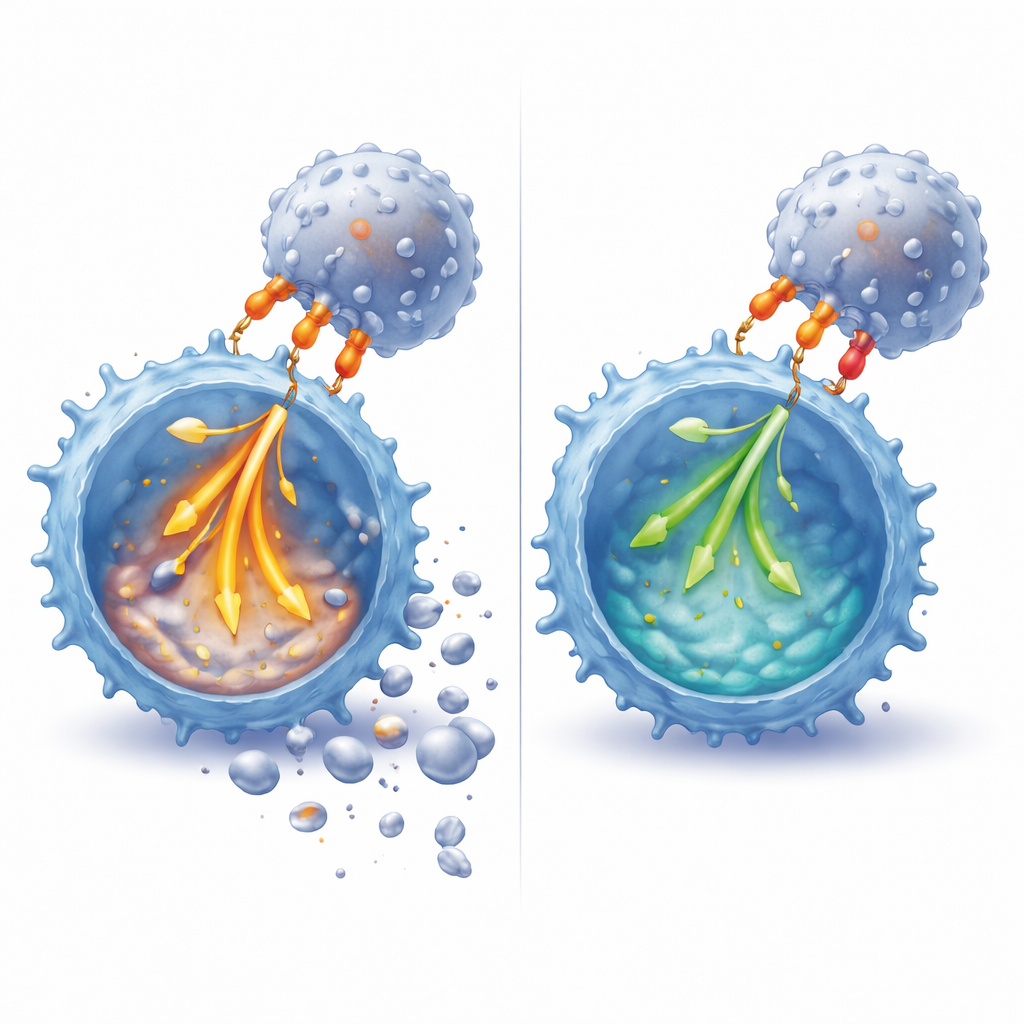
Ослабление сигналов и смещение баланса молекул выживания
Анализ внутри клетки показал, что активация PD‑1 приглушает широкий спектр ранних сигнальных событий, следующих за повторной стимуляцией Т‑клетки. Фосфатные метки на ключевых сигнальных белках — включая компоненты, непосредственно связанные с рецептором, и центральный передатчик ERK — заметно снижались в присутствии PD‑L1. Это ослабление было особенно заметно при одновременном вовлечении CD28, что коррелировало с более выраженным влиянием на RICD в этой обстановке. Сигнал через PD‑1 также смещал клеточный цикл, удерживая больше клеток в фазе контрольной точки G1, а не толкая их в активную репликацию ДНК, состояние, известное своей повышенной чувствительностью к сигналам гибели. На уровне белков PD‑1 менял соотношение между про‑смертными и про‑жизнеспособными молекулами: он ослаблял индуцирование лиганда FAS, ключевого запускающего фактора гибели Т‑клеток, и способствовал сохранению survivin — фактора, поддерживающего выживание и контролируемое деление Т‑клеток.
Значение этих результатов для терапии и иммунного здоровья
В совокупности результаты показывают, что PD‑1 — это не просто выключатель активности Т‑клеток, а тонкий регулятор, который защищает недавно активированные человеческие Т‑клетки от преждевременной гибели в ходе их экспансии. Смягчая силу повторных сигналов через Т‑клеточный рецептор и CD28 и отодвигая баланс в сторону молекул, поддерживающих выживание, PD‑1 позволяет сформироваться сильной, но контролируемой армии Т‑клеток до того, как программа самоуничтожения полностью включится. Для пациентов это означает, что препараты, блокирующие PD‑1 — мощные инструменты в онкологии — могут делать некоторые Т‑клетки более уязвимыми к RICD, что потенциально изменяет нормальный иммунный баланс или способствует побочным эффектам. Будущие терапии и клеточные подходы, такие как CAR‑T‑клетки, могут выиграть от целенаправленной модуляции PD‑1 и родственных путей, чтобы сохранить достаточное число долгоживущих эффективных Т‑клеток, одновременно предотвращая вредную иммунную гиперактивность.
Цитирование: Lee, K.P., Elster, S., Epstein, B. et al. PD-1 protects expanding human T cells from premature restimulation-induced cell death by modulating TCR and CD28 signaling. Cell Death Dis 17, 272 (2026). https://doi.org/10.1038/s41419-026-08530-6
Ключевые слова: Сигнальное пути PD-1, Выживание Т-клеток, Иммунные контрольные точки, Гибель, вызванная активацией, Иммунотерапия рака