Clear Sky Science · ru
Сигнализация лептина‑LEPR в костном мозге перенастраивает митохондриальный окислительный метаболизм и обеспечивает химиорезистентность при остром миелоидном лейкозе
Почему жир в костном мозге важен для лечения лейкоза
Многие знают, что жировая ткань влияет на такие заболевания, как диабет и болезни сердца, но немногие представляют, что жир, скрытый внутри костей, также может влиять на ответ крови на лечение. В этом исследовании изучают, как гормон, вырабатываемый адипоцитами — лептин — защищает клетки острого миелоидного лейкоза (ОМЛ) от стандартной химиотерапии. Понимание этой скрытой системы защиты может указать пути для повышения эффективности уже существующих препаратов для пациентов.
Гормон, который меняет шансы в пользу устойчивости к химиотерапии
Исследователи начали с анализа образцов костного мозга у взрослых с недавно установленным диагнозом ОМЛ. Они измеряли уровень лептина в мозге и оценивали, насколько эффективно пациенты избавлялись от лейкозных клеток после лечения распространённым химиопрепаратом цитарабином. Пациенты с более высоким уровнем лептина в мозге и с повышенной экспрессией его рецептора на лейкозных клетках реже отвечали на лечение и имели более короткую выживаемость. Даже с учётом других факторов риска лептин оставался сильным предиктором плохого ответа на химиотерапию. Это наводило на мысль, что гормон из жировой ткани — не просто маркер тяжести болезни, а активно связан с устойчивостью к лечению.
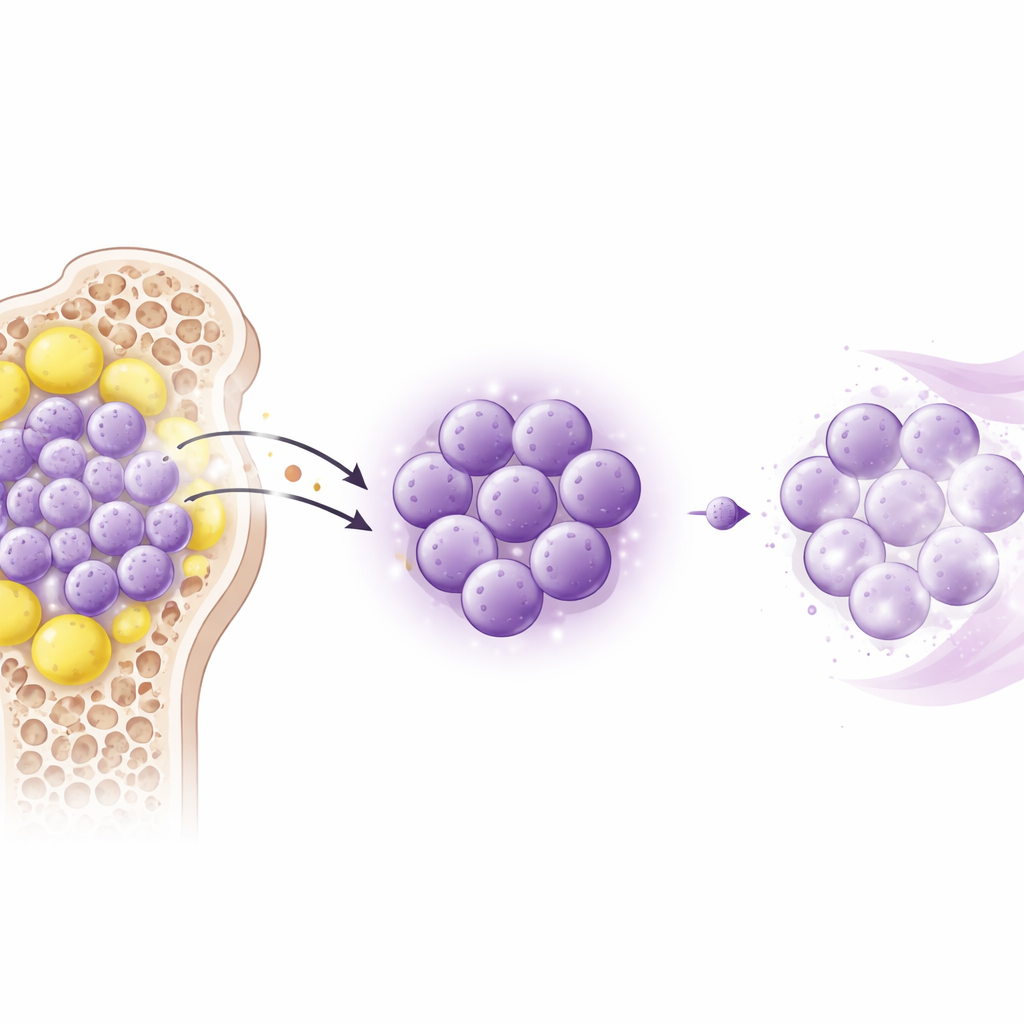
Эксперименты на животных показывают скрытый щит
Чтобы проверить, действительно ли лептин вызывает лекарственную устойчивость, команда использовала две мышиные модели ОМЛ, хорошо воспроизводящие человеческое заболевание. Мышам вводили либо только цитарабин, либо цитарабин вместе с дополнительным лептином, либо цитарабин и небольшой пептид, блокирующий рецептор лептина. Добавление лептина сокращало выживаемость, увеличивало селезёнку и печень и позволяло лейкозным клеткам заполнять эти органы несмотря на химиотерапию. Напротив, блокирование рецептора само по себе не замедляло рост лейкоза, но значительно усиливало эффект цитарабина: уменьшались размеры поражённых органов и снижалась нагрузка лейкоза. Эти данные показывают, что основной эффект лептина — не прямое ускорение роста рака, а повышение устойчивости лейкозных клеток к уничтожению химиотерапией.
Включение энергетических центров клетки
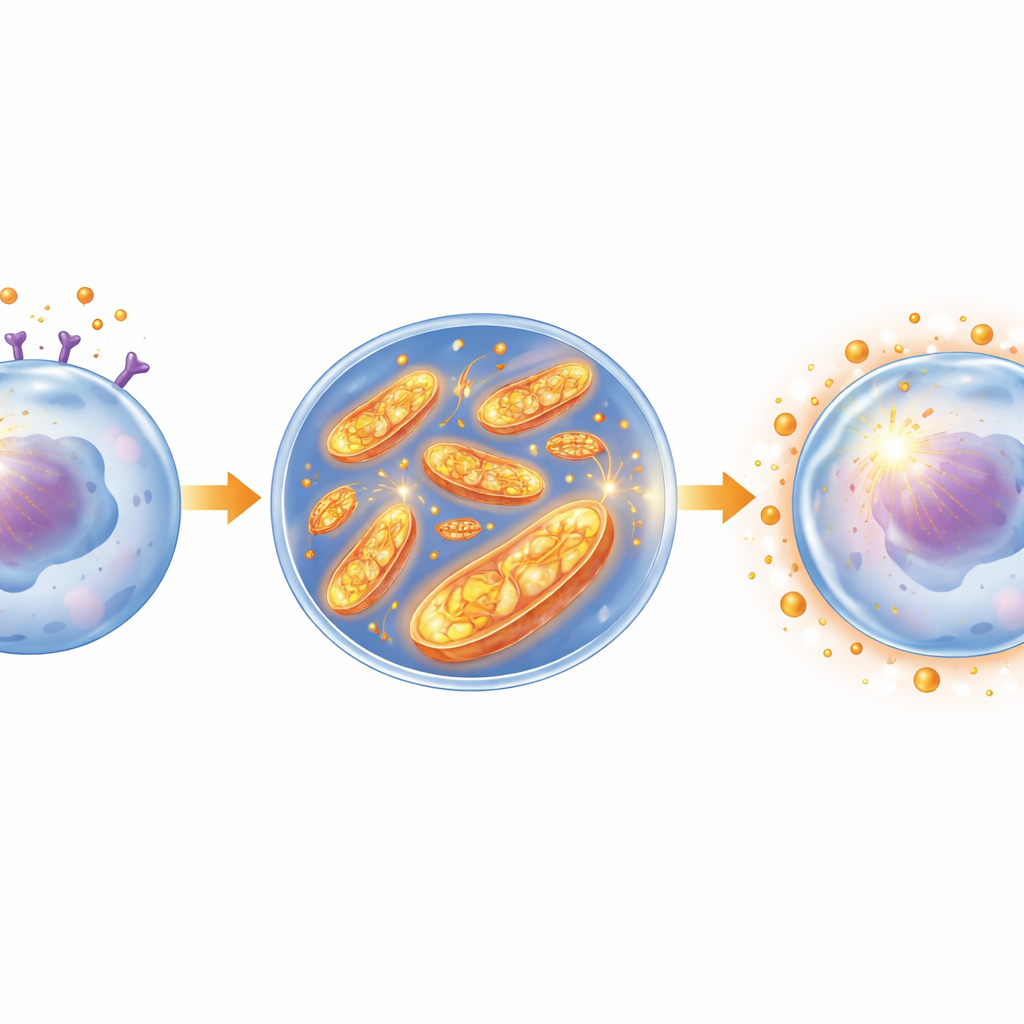
Углубившись, учёные изучили, как лептин меняет метаболизм лейкозных клеток. Они обнаружили, что лептин активирует внутриклеточную сигнальную цепочку JAK2/STAT3, которая, в свою очередь, усиливает работу митохондрий — крошечных энергетических станций клетки. И в мышиных лейкозных клетках, и в человеческих линиях ОМЛ лептин увеличивал активность одного ключевого митохондриального компонента, комплекса I, и повышал общий окислительный метаболизм. Этот сдвиг приводил к увеличению образования реактивных кислородных видов внутри митохондрий. Парадоксально, вместо того чтобы напрямую убивать клетки, постепенное повышение этих реактивных молекул запускало адаптационный ответ: лейкозные клетки наращивали свои антиоксидантные механизмы, такие как глутатион и детоксикационные ферменты, формируя мощный внутренний щит.
Когда стресс превращается в броню
Команда показала, что этот щит лежит в основе химиорезистентности. Клетки, обработанные лептином, демонстрировали более высокую общую антиоксидантную способность и были менее чувствительны к цитарабину и другому препарату, даунорубицину. Удаление рецептора лептина с помощью генетического редактирования ослабляло эту антиоксидантную сеть, снижало уровни защитных молекул и делало клетки значительно более чувствительными к лечению даже при отсутствии лептина. Дополнительные эксперименты подтвердили, что резкий всплеск митохондриального стресса может вызвать подобную защитную программу, тогда как нейтрализация этих реактивных молекул разрушает щит и восстанавливает чувствительность к препаратам. Важно, что блокирование сигнального пути JAK2/STAT3 или самого рецептора лептина предотвращало активацию комплекса I, снижало митохондриальные сигналы стресса, разрушало антиоксидантный барьер и снова делало химиотерапию эффективной.
Преобразование слабости в новый терапевтический подход
Для пациентов суть исследования в том, что лейкозные клетки могут пользоваться гормоном, вырабатываемым соседними жировыми клетками, чтобы пережить химиотерапию. Лептин из костномозгового жира связывается с рецептором на лейкозных клетках, перенастраивает их митохондрии на повышенную выработку энергии и использует возникающий низкоуровневый стресс для включения антиоксидантной «страховочной» сети. Эта сеть защищает клетки от более сильного повреждения, вызванного противораковыми препаратами. Блокируя рецептор лептина или его нижележащую сигнальную каскаду, в будущем можно будет снять эту защиту и позволить существующим химиотерапиям действовать так, как задумано, без необходимости повышения доз. Таким образом, лучшее понимание того, как жир костного мозга «общается» с лейкозными клетками, может напрямую привести к более стойким ремиссиям у людей с ОМЛ.
Цитирование: Liao, X., Dai, W., Xu, X. et al. Marrow leptin-LEPR signaling rewires mitochondrial oxidative metabolism to confer chemoresistance in acute myeloid leukemia. Cell Death Dis 17, 249 (2026). https://doi.org/10.1038/s41419-026-08528-0
Ключевые слова: острый миелоидный лейкоз, лептин, химиорезистентность, митохондрии, окислительный стресс