Clear Sky Science · ru
Ядерный миозин 1 связывает архитектуру генома с ремоделированием жировой ткани, метаболическим воспалением и ожирением у мышей
Почему «скелет» клетки важен для жировой ткани
Ожирение часто объясняют тем, что и сколько мы едим и насколько много двигаемся, но глубоко внутри клеток способ упаковки и считывания ДНК тоже может изменить весы. В этом исследовании показано, что крошечный моторный белок — ядерный миозин 1 (NM1), который помогает организовывать ДНК в ядре клетки — играет неожиданную роль в том, как образуются жировые клетки, запасают энергию и запускают воспаление. Изучая мышей, лишённых этого белка, исследователи обнаружили прямую связь между физической архитектурой наших генов и развитием нездорового висцерального жира и метаболических нарушений.
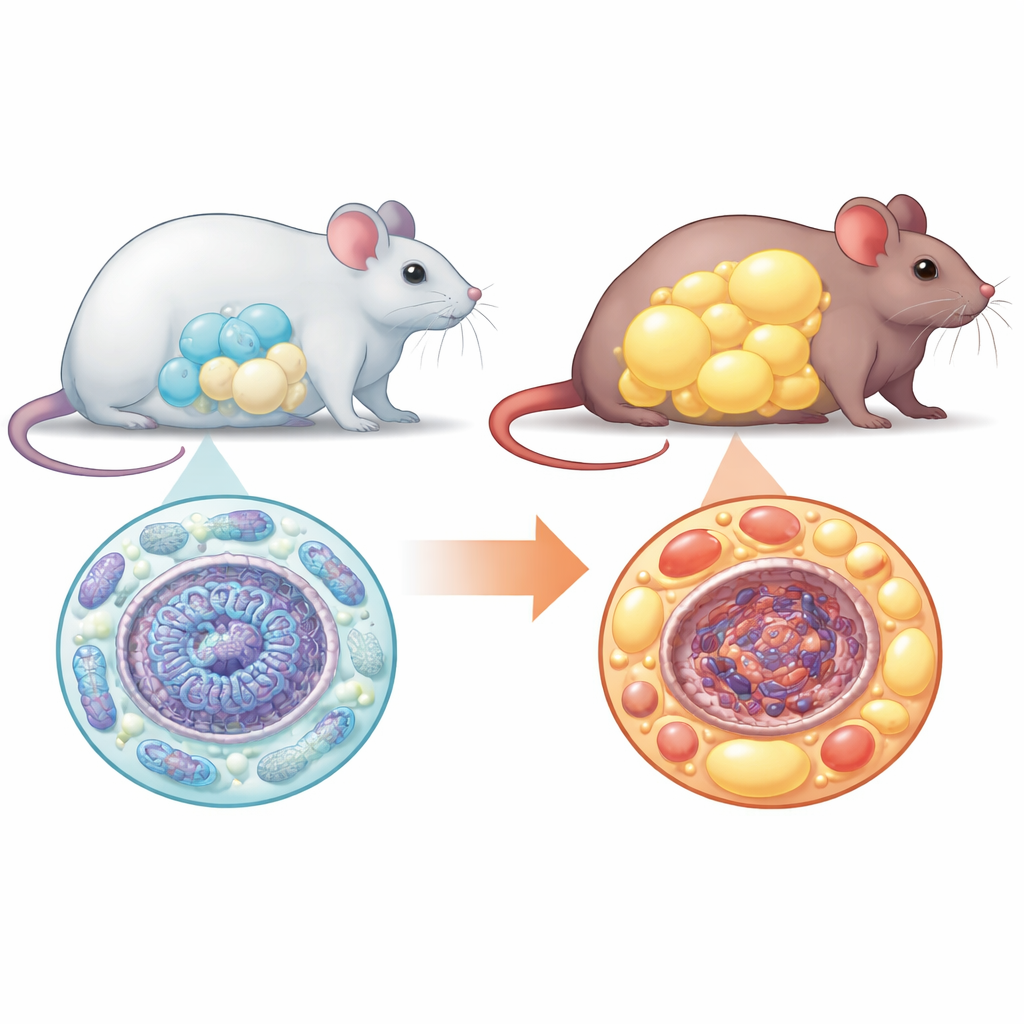
От стволовых клеток к адипоцитам
Жировые клетки развиваются из универсальных предшественников, называемых мезенхимальными стволовыми клетками. В норме эти предшественники размножаются, переключают способы использования энергии и созревают в многочисленные небольшие, нормально функционирующие жировые клетки, которые безопасно хранят избыточные калории. Команда обнаружила, что при отсутствии NM1 этот упорядоченный процесс нарушается. Когда они выращивали стволовые клетки от нормальных и NM1-дефицитных мышей в лаборатории и стимулировали их превращение в жировые клетки, в отсутствие NM1 значительно меньше клеток завершили переход. Те клетки, которые дозревали, были заметно больше обычных: наполненные липидами, но лишённые типичных маркёров здоровых адипоцитов на уровне генов и белков. Эта картина — меньше клеток, но каждая из них увеличена — является характеристикой нездоровой жировой ткани.
Как упаковка генов формирует поведение жировых клеток
NM1 действует в ядре, помогая сохранять участки ДНК доступными, чтобы важные гены можно было включать. Чтобы понять, как его потеря меняет поведение клеток, исследователи совместили карты открытых участков ДНК с измерениями активности генов в клетках с NM1 и без него. Они увидели, что многие гены, необходимые для формирования жировых клеток, обращения с жировыми каплями и поддержания митохондрий, теряли как доступность, так и активность при отсутствии NM1. В то же время другие гены, связанные с ростом и сигнальными путями, становились более открытыми и активными. Это указывает на NM1 как на ключевого регулятора трафика: он помогает поддерживать сбалансированный ландшафт открытых и закрытых участков ДНК, чтобы нужные сети генов обеспечивали здоровое развитие адипоцитов и метаболизм.
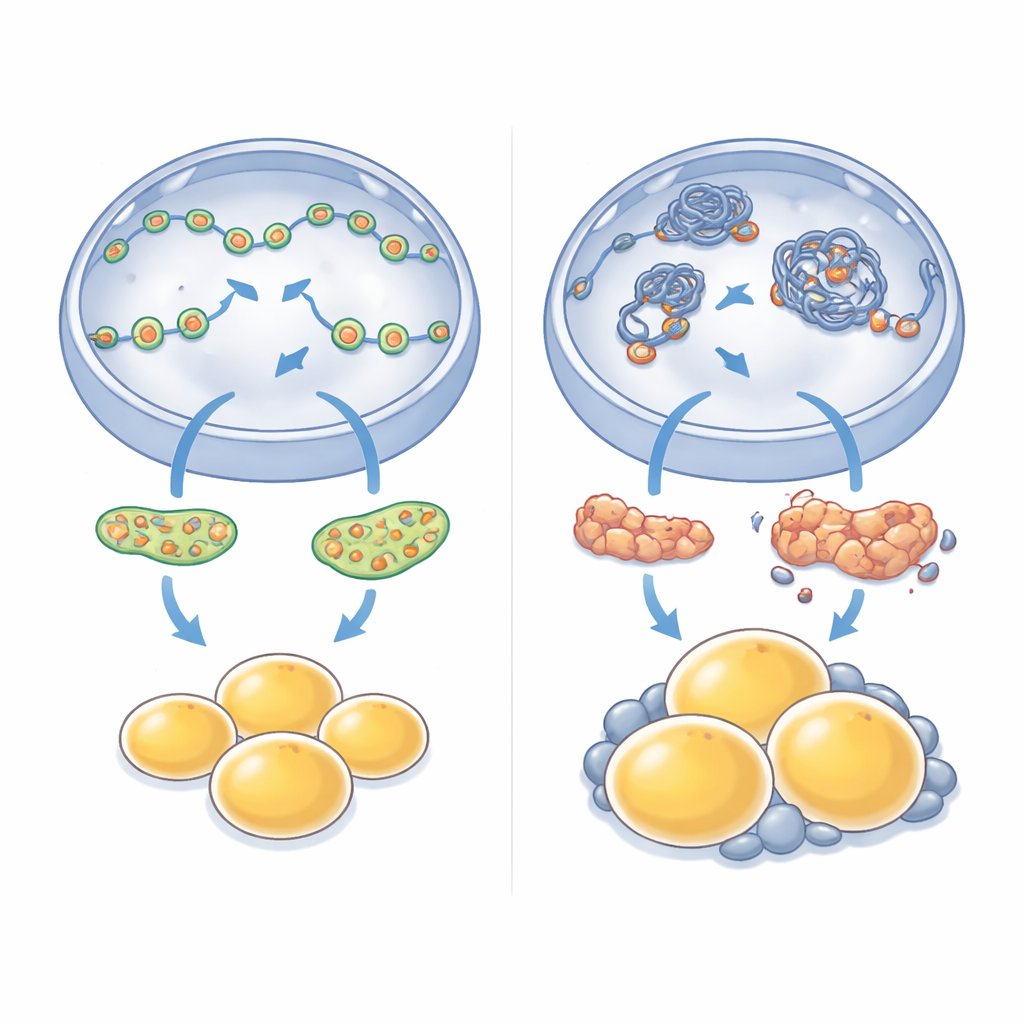
Когда локальные изменения превращаются в набор тела
Последствия потери этого единственного ядерного мотора не остались ограниченными клетками в чашке Петри. Мыши, лишённые NM1, со временем становились тяжелее своих нормальных сибсов, хотя не потребляли больше пищи. Сканирование и анализ тканей показали явное накопление жира, особенно вокруг внутренних органов в брюшной полости, а отдельные жировые клетки в этих областях были заметно увеличены. Когда исследователи измеряли, какие гены повышены или понижены в этом висцеральном жире, они обнаружили широкие изменения: пути, связанные с энергопользованием, инсулиновой сигнализацией и ремоделированием тканей, были перепрограммированы. Гены, ассоциированные с ростом и расширением жировых клеток, часто усиливались, в то время как несколько ключевых контролирующих факторов здорового формирования адипоцитов угнетались, что отражало дефекты, наблюдаемые в культурах стволовых клеток.
Воспалённый жир и нарушённые энергетические «двигатели»
Помимо увеличения размера, жировая ткань у NM1-дефицитных мышей демонстрировала признаки воспаления и метаболического стресса. Детальный анализ путей выявил сильную активацию иммунных сигналов, опосредованных такими молекулами, как интерферон-γ и фактор некроза опухоли, которые известны своим вкладом в инсулинорезистентность и метаболические заболевания. Одновременно регуляторы, поддерживающие спокойную и энергоэффективную жировую ткань, были подавлены. Исследование также связало потерю NM1 с нарушениями митохондрий — энергетических двигателей клетки. Гены, которые обычно контролируют качество митохондрий и переключение между эффективной аэробной выработкой энергии и быстрыми гликолитическими путями, были неправильно отрегулированы, что указывает на то, что при отсутствии NM1 адипоциты переходят к менее эффективной, более склонной к стрессу энергетической стратегии.
Общие сигналы у мышей и людей
Чтобы выяснить, имеет ли значение этот путь ядерного мотора у людей, авторы проанализировали большие генетические наборы данных из человеческого висцерального жира. Они сосредоточились на человеческом аналоге NM1 — MYO1C — и изучили сети вариантов, которые настраивают активность соседних генов. Они обнаружили, что многие из тех же тем, что наблюдались у мышей — контроль цитоскелета, иммунная сигнализация и метаболическая регуляция — проявлялись и в человеческих генетических сетях, связанных с MYO1C. Несколько генов, изменённых в висцеральном жире NM1-дефицитных мышей, также входили в эти человеческие сети и ранее связывались с ремоделированием жировой ткани и метаболизмом. Это перекрёстное соответствие между видами свидетельствует о том, что схожие ядерные механизмы могут влиять на риск ожирения у людей.
Что это значит для ожирения и метаболического здоровья
В целом работа показывает, что NM1 — это не просто ядерная «помощь», а центральный узел, связывающий организацию ДНК с тем, как адипоциты растут, хранят энергию и общаются с иммунной системой. При отсутствии NM1 переключатели генов в предшественниках жира смещаются, митохондрии функционируют хуже, клетки жира увеличиваются вместо размножения, а висцеральный жир воспаляется — сочетание, напоминающее нездоровую жировую ткань при ожирении и инсулинорезистентности. Для непрофессионального читателя главная мысль такова: физическое расположение ДНК и её вспомогательных белков внутри ядра может предрасполагать ткани к здоровому или вредному разрастанию жира. Белки вроде NM1 и его человеческого аналога MYO1C могут однажды стать мишенями терапии, направленной на перестройку жировой ткани изнутри, предлагая более точный подход к лечению заболеваний, связанных с ожирением.
Цитирование: Khalaji, S., Venit, T., Lukáčová, Z. et al. Nuclear Myosin 1 links genomic architecture to adipose tissue remodeling, metabolic inflammation and obesity in mice. Cell Death Dis 17, 270 (2026). https://doi.org/10.1038/s41419-026-08525-3
Ключевые слова: адипогенез, хроматин, митохондрии, висцеральный жир, метаболическое воспаление