Clear Sky Science · ru
Триметилирование лизина 36 гистона H3 ферментом SETD2 формирует эпигенетический ландшафт в кишечных стволовых клетках, чтобы координировать липидный метаболизм и ослаблять клеточное старение
Почему кишечные стволовые клетки важны по мере старения
Глубоко в стенке кишечника крошечные стволовые клетки непрерывно работают, чтобы обновлять ткань, которая помогает нам переваривать пищу и усваивать питательные вещества. С возрастом эти клетки устают, из-за чего кишечник становится более уязвимым к заболеваниям и медленнее заживает. В этом исследовании изучают, как тонкие химические метки на белках, упаковывающих ДНК, помогают сохранять молодость кишечных стволовых клеток, как их утрата нарушает внутриклеточное сжигание жиров и как правильно подобранные препараты могут однажды замедлить это ухудшение.
Стареющие клетки в требовательной среде
Внутренняя поверхность кишечника — одна из самых быстро обновляющихся тканей в организме. Стволовые клетки, расположенные у основания небольших углублений — крипт, делятся, чтобы заменять миллиарды клеток каждые несколько дней. Эта постоянная работа требует стабильного источника энергии, значительная часть которой обеспечивается расщеплением жиров. Одновременно этими стволовыми клетками управляет «эпигенетический» код — химические метки на гистонах, которые помогают определять, какие гены активны, а какие — подавлены. Авторы сосредоточились на одной такой метке, известной как триметилирование H3K36, создаваемой ферментом SETD2, и задали вопрос, могут ли изменения этой метки объяснить, почему кишечные стволовые клетки теряют свою жизнеспособность с возрастом.
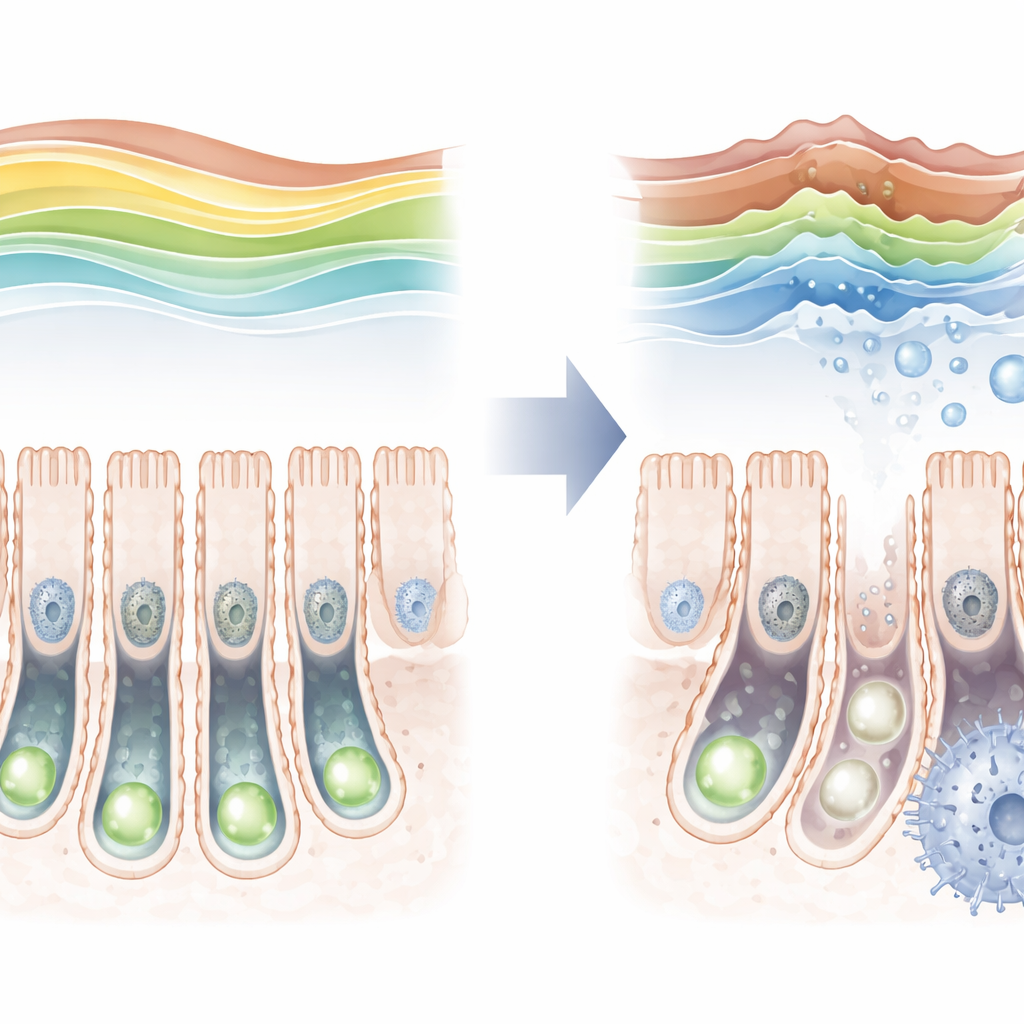
Защитная метка, которая бледнеет с возрастом
Изучая кишечник мышей на разных этапах жизни, исследователи обнаружили, что триметильная метка H3K36 не статична. Она относительно низкая сразу после рождения, затем растёт и достигает пика у молодых взрослых, после чего снова снижается в старости. По мере падения этой метки у старых животных в стволовых клетках возрастали маркеры клеточного старения, что указывает на связь между ними. Чтобы проверить это напрямую, команда создала мышей, у которых SETD2 можно было удалить только в кишечных стволовых клетках. При удалении этого фермента защитная метка почти исчезала, стволовые клетки реже делились и испытывали трудности с производством полного набора специализированных клеточных типов кишечника.
Как эпигенетические изменения нарушают сжигание жиров
Потеря этой одной метки гистона запустила каскад изменений внутри стволовых клеток. Измерения активности генов показали, что многие гены, вовлечённые в клеточный цикл и репликацию ДНК, были ослаблены, тогда как гены, связанные со стрессом и старением, усиленно экспрессировались. Поразительно, что самым сильным сигналом оказались нарушения в обращении с липидами: гены, обычно поддерживающие окисление жирных кислот — контролируемое сжигание жиров для получения энергии — были подавлены, и жиры начали накапливаться в криптах. Профилирование метаболитов подтвердило накопление длинноцепочечных жирных кислот, что свидетельствует о сбое обычных путей переработки жиров. Одновременно изменилась упаковка ДНК в ядре: многие области стали либо более доступными, либо более плотно закрытыми, меняя набор генов, которые клетка может быстро включать.
Ремоделирующие хроматин факторы и марш к сенесценции
Чтобы понять, как возникают эти изменения упаковки ДНК, авторы картировали как открытые области хроматина, так и набор других меток гистонов по всему геному. При потере триметилирования H3K36 большие участки ДНК приобретали «активные» метки и становились более доступными, особенно вблизи генов, связанных с метаболизмом и старением. Ключевым участником этого перехода оказался комплекс ремоделирования хроматина SWI/SNF, работающий при участии основного субъединичного белка SMARCA4. У стволовых клеток без SETD2 уровень SMARCA4 повышался, и комплекс, по-видимому, помогал открывать области, запускающие программы сенесценции. Когда исследователи снижали активность SMARCA4 генетически или с помощью таргетного ингибитора, стволовые клетки частично восстанавливали способность формировать здоровые мини-кишечники в культуре, а маркеры старения снижались — это свидетельствует о том, что чрезмерное ремоделирование толкает эти клетки в утомлённое, сенесцентное состояние.
Пробуждение энергетических путей для спасения стволовых клеток
Поскольку нарушение сжигания жиров оказалось ключевой проблемой, команда проверила, можно ли усиление этого пути противодействовать старению стволовых клеток. Они использовали препарат, активирующий PPARα, главный регулятор окисления жирных кислот. В органоидах, выращенных из стволовых клеток с дефицитом SETD2, это лечение усиливало рост, восстанавливало отпочковывающиеся структуры, характерные для активных стволовых клеток, и снижало накопление жира. У живых мышей та же интервенция частично восполняла пул стволовых клеток, снижала маркеры сенесценции и нормализовала накопление липидов в кишечных криптах. Эти результаты выводят окисление жирных кислот как ключевую связь между эпигенетическим контролем и здоровьем стволовых клеток.
Что это значит для здорового старения
В целом работа показывает, что специфическая метка гистона, наносимая SETD2, помогает поддерживать сбалансированный эпигенетический ландшафт в кишечных стволовых клетках. Когда эта метка исчезает, хроматин аномально ремоделируется, пути сжигания жиров дают сбой, липиды накапливаются, и клетки скатываются в сенесценцию, ослабляя восстановительную систему кишечника. Путём либо ослабления чрезмерно активного ремоделирующего комплекса, либо восстановления жирового метаболизма с помощью таргетных препаратов возможно сохранить функцию стволовых клеток и здоровье кишечника в пожилом возрасте. Хотя эти результаты получены на мышах, они перекликаются с паттернами, наблюдаемыми при человеческих заболеваниях кишечника, что даёт надежду: тщательно подобранные метаболические терапии однажды могут помочь противостоять возрастному упадку и в наших собственных кишечных стволовых клетках.
Цитирование: Xu, Y., Wang, Z., Feng, W. et al. Histone 3 lysine 36 trimethylation by SETD2 shapes an epigenetic landscape in intestinal stem cells to orchestrate lipid metabolism and attenuate cell senescence. Cell Death Dis 17, 273 (2026). https://doi.org/10.1038/s41419-026-08518-2
Ключевые слова: кишечные стволовые клетки, эпигенетика, окисление жирных кислот, клеточное старение, SETD2