Clear Sky Science · ru
РНК, связанная с Lamp2a и секретируемая АДСК, предотвращает петлю ENO1–лактиляция–гликолиз и злокачественное поведение клеток при тройном-негативном раке молочной железы
Почему это важно для пациентов
Тройно-негативный рак молочной железы — одна из самых агрессивных форм рака молочной железы; он лишён гормональных или факторов роста, которые делают другие подтипы более поддающимися лечению. В этом исследовании показано, как такие опухоли перенастраивают своё энергетическое потребление, чтобы выживать при низком содержании кислорода, и описан изобретательный способ нарушить эту перенастройку. Для читателей это даёт представление о том, как понимание метаболизма рака может привести к новым высоко направленным терапиям, принципиально отличающимся от традиционной химиотерапии.
Как эти опухоли подпитывают себя
Многие раки сильно зависят от быстрого, но неэффективного пути получения энергии — гликолиза, при котором сахар превращается в побочный продукт лактат. Анализ образцов пациентов, общедоступных генетических баз данных и нескольких линий раковых клеток молочной железы показал, что тройно-негативные опухоли в ещё большей степени полагаются на гликолиз, чем другие подтипы. Ключевой фермент этого пути, ENO1, особенно высоко экспрессирован в этих опухолях и связан с худшим прогнозом. При снижении уровней ENO1 в культивируемых тройно-негативных клетках они смещались от гликолиза к более нормальному митохондриальному производству энергии, расти стали медленнее и утратили способность активно инвазировать и образовывать колонии.
Опасная петля внутри раковых клеток
Углублённый анализ показал, что сам лактат усиливает ENO1 и запирает раковые клетки в порочном цикле. Лактат может химически модифицировать белки в процессе, называемом лактиляцией. В тройно-негативных клетках избыток лактата увеличивал лактиляцию ENO1, что, в свою очередь, повышало активность и стабильность фермента, ещё сильнее ускоряя гликолиз и порождая ещё больше лактата. В условиях низкого содержания кислорода — характерных для солидных опухолей — эта петля становилась сильнее, помогая клеткам противостоять гибели и продолжать пролиферацию. Блокирование активности ENO1 малым молекулярным ингибитором или снижение производства лактата ослабляло эту петлю, сокращало гликолиз и замедляло рост опухолей у мышей.
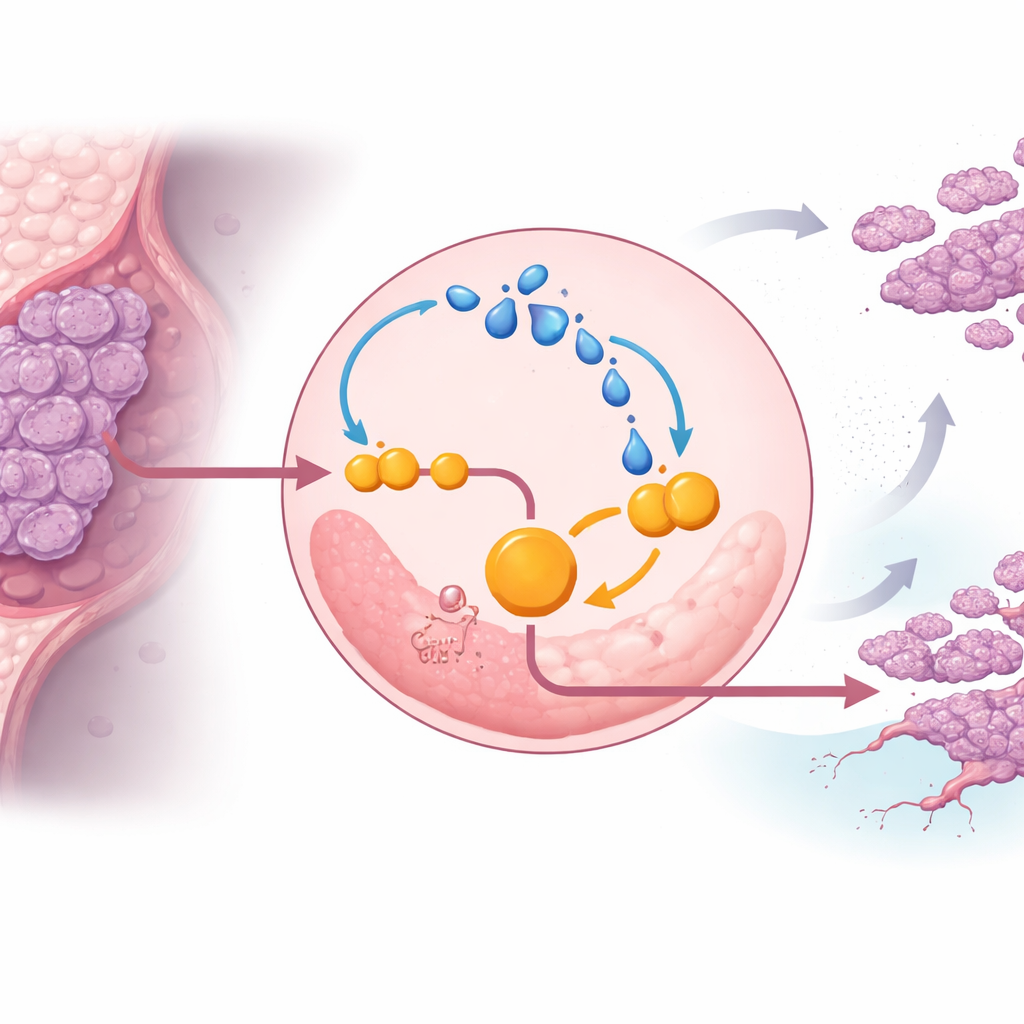
Молекулярный переключатель, который защищает ENO1
В исследовании выявлен конкретный контрольный пункт в ENO1, благодаря которому возможна эта петля. Белок EP300 добавляет лактат-обусловленные метки на несколько лизиновых остатков ENO1, и один из них, обозначенный как K262, оказался ключевым. Когда этот сайт был мутирован так, что его больше нельзя было лактиллировать, ENO1 быстро направлялся в клеточные перерабатывающие структуры — лизосомы — и разрушался. Без этой защитной метки тройно-негативные клетки утратили большую часть своего гликолитического потенциала и способности образовывать опухоли и метастазы в модельных животных. Это выделяет лактиляцию ENO1 на K262 как молекулярный переключатель, который защищает фермент от разрушения и поддерживает изменённый метаболизм рака.
Новый способ пометить ENO1 для уничтожения
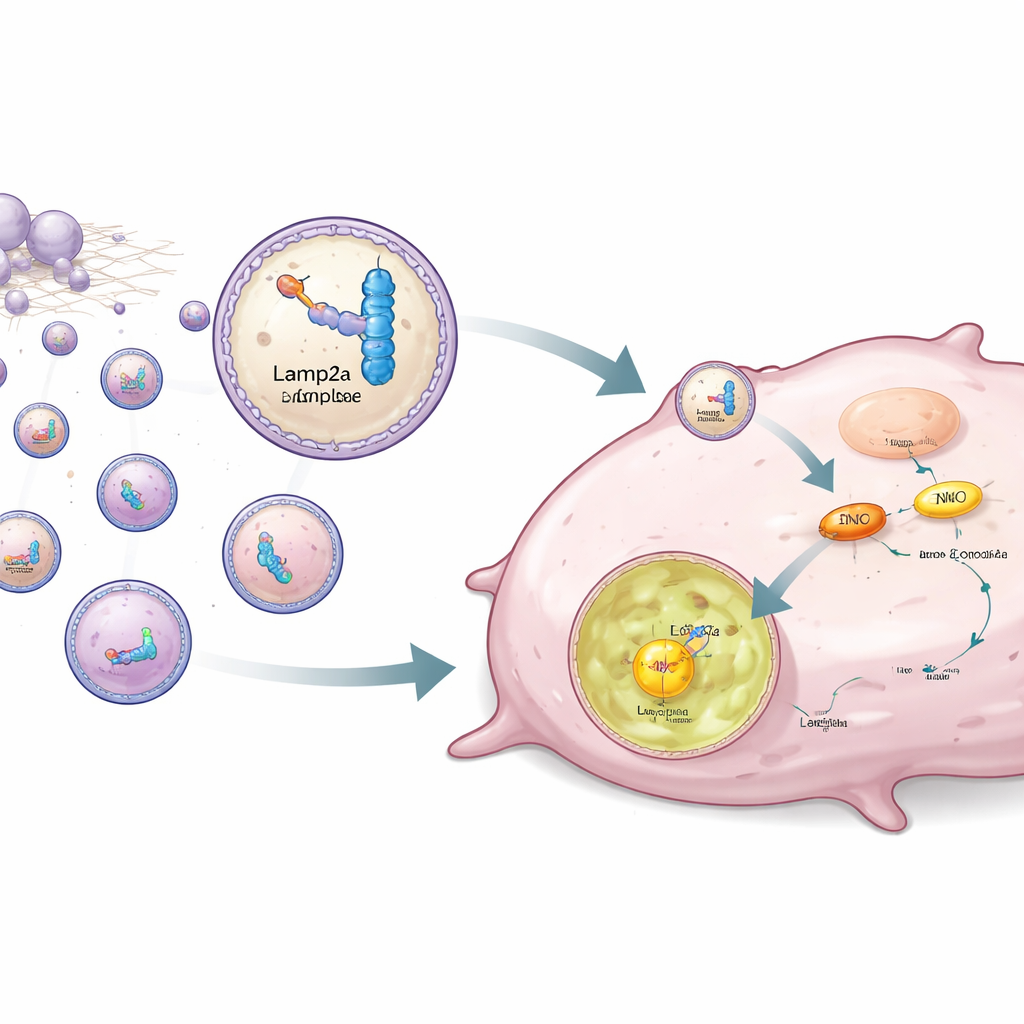
Вместо простого блока ENO1 авторы разработали стратегию избирательного удаления этого белка из раковых клеток. ENO1 также действует как РНК-связывающий белок, распознавая короткие специфические последовательности РНК. Команда сконструировала синтетические фрагменты РНК, которые сильно связывают ENO1, и затем связала их с Lamp2a — белком мембраны лизосомы, участвующим в целенаправленной деградации белков. Стволовые клетки человека, полученные из жировой ткани, генетически модифицировали так, чтобы они производили эту пару РНК–Lamp2a и паковали её в маленькие везикулы — экзосомы. Когда эти инженерные экзосомы добавляли к тройно-негативным клеткам, РНК-член прочно прикреплялся к ENO1, а часть Lamp2a направляла весь комплекс в лизосомы, где ENO1 разрушался даже при наличии стабилизирующей лактиляции.
Испытание подхода направленной деградации в животных
Чтобы приблизить эту идею к практической терапии, исследователи выращивали модифицированные стволовые клетки на биоразлагаемом каркасе и имплантировали этот конструкт подкожно у мышей рядом с тройно-негативными опухолями. Из этого местоположения стволовые клетки непрерывно выпускали экзосомы, несущие комплексы, нацеленные на ENO1. У животных с таким лечением в опухолях отмечались значительно более низкие уровни белка ENO1, сниженный гликолиз, меньше делящихся клеток и больше признаков гибели по сравнению с контрольной группой. Опухоли росли медленнее, и их злокачественное поведение было заметно подавлено, что демонстрирует: направление ENO1 в лизосомы может эффективно лишить рак его предпочитаемого энергетического пути.
Что это может значить для будущего лечения
Для неспециалистов главный вывод в том, что работа выявляет как уязвимость, так и потенциальный новый лечебный подход для тройно-негативного рака молочной железы. Уязвимость — зависимость опухоли от самоподдерживающейся энергетической петли вокруг ENO1 и лактата, особенно в зонах с низким кислородом. Направление лечения — система селективной деградации белка, использующая настраиваемую РНК и экзосомы, полученные от стволовых клеток, чтобы направлять ENO1 в клеточную систему утилизации. Хоть до клинического применения ещё далеко, этот подход иллюстрирует, как глубокое понимание метаболических приёмов рака может вдохновить на создание точных терапий, целью которых является обезвреживание, а не просто отравление злокачественных клеток.
Цитирование: Cheng, S., Xia, B., Li, L. et al. A Lamp2a-linked RNA secreted by ADSCs prevents ENO1–lactylation–glycolysis feedback and cell malignant behavior in triple-negative breast cancer. Cell Death Dis 17, 288 (2026). https://doi.org/10.1038/s41419-026-08517-3
Ключевые слова: тройно-негативный рак молочной железы, метаболизм рака, лактатный сигналинг, селективный деградационный путь белков, фермент ENO1