Clear Sky Science · ru
Фосфатаза Shp1 регулирует стабильность белка CXCR2 и инвазивность, опосредованную IL8, при раке молочной железы
Почему это исследование важно для рака молочной железы
Рак молочной железы по-прежнему остается одной из ведущих причин смерти от рака у женщин, во многом потому, что некоторые опухоли становятся инвазивными и метастазируют в отдаленные органы. В этом исследовании подробно рассматривается, как распространенный воспалительный сигнал в опухоли — IL8 — взаимодействует с раковыми клетками молочной железы и как молекулярный «тормоз» под названием Shp1 помогает решить, останутся ли эти клетки на месте или станут более агрессивными. Понимание этой молекулярной борьбы может открыть новые пути для замедления или предотвращения распространения трудно поддающихся лечению форм рака молочной железы, особенно тройной-негативной болезни.
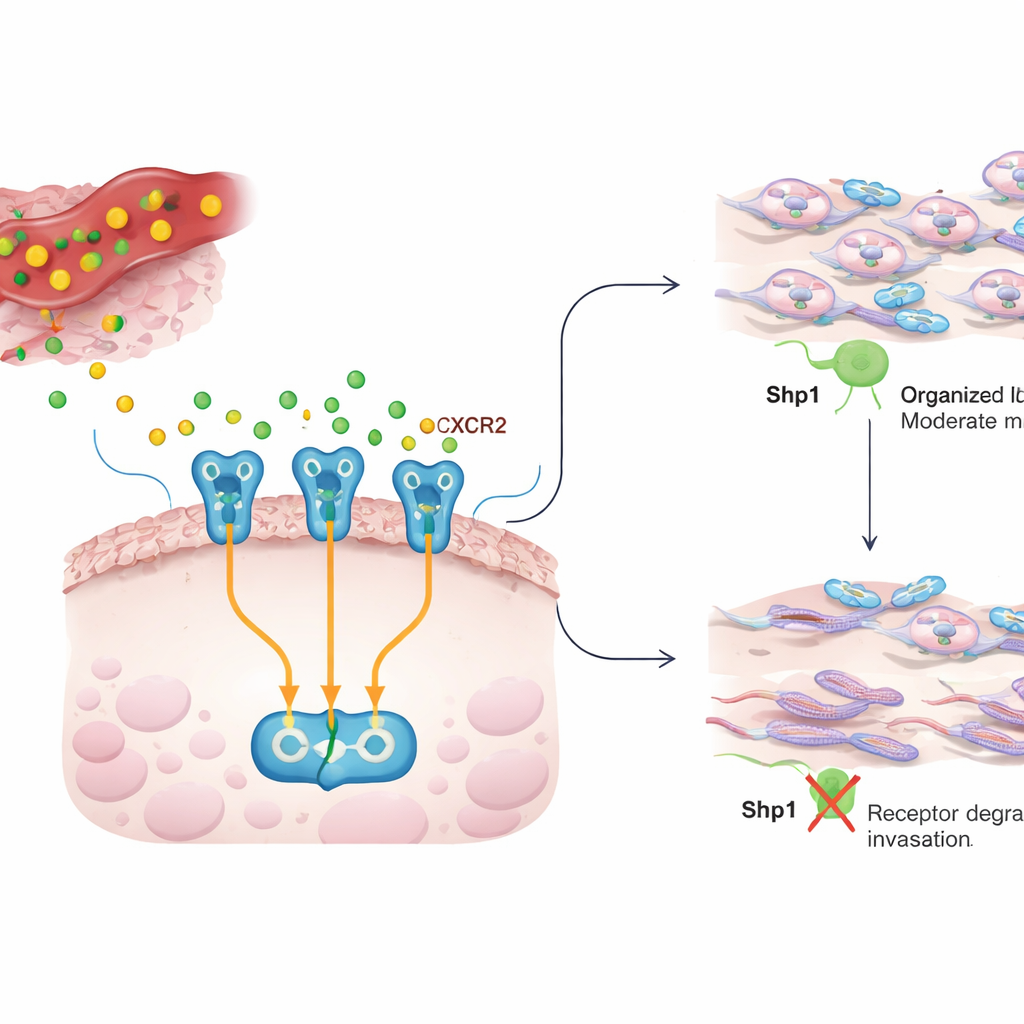
Разговор между воспалением и раковыми клетками
Внутри опухоли раковые клетки окружены иммунными и поддерживающими клетками, которые выделяют химические мессенджеры — цитокины. IL8 — один из таких мессенджеров и часто обнаруживается в высоких концентрациях во многих видах рака, где он стимулирует рост, образование кровеносных сосудов и способность клеток перемещаться и инвазиовать. IL8 действует через рецептор на поверхности раковой клетки, называемый CXCR2. Когда IL8 связывается с CXCR2, запускаются несколько внутренних цепей, которые реорганизуют цитоскелет клетки, помогая ей ползти через ткань и распространяться. В данной работе исследуют, как этот диалог IL8–CXCR2 удерживается под контролем и влияет ли Shp1 — фермент, обычно рассматриваемый как тормоз опухолевого роста — на инвазивное поведение.
Скрытая роль Shp1 в движении клеток
Сначала исследователи удалили или химически заблокировали Shp1 в широко используемой люминальной линии клеток рака молочной железы (MCF7) и измерили способность клеток мигрировать и вторгаться через гель, имитирующий ткань. Без Shp1 клетки закрывали «раны» быстрее и проходили через гель в два–три раза эффективнее, что показывает: Shp1 обычно сдерживает движение. Анализ данных пациентов также показал, что у женщин с опухолями, экспрессирующими меньшие уровни Shp1, выживаемость хуже, а время до рецидива короче. В совокупности эти результаты указывают, что Shp1 ограничивает агрессивное поведение клеток рака молочной железы, и потеря этого «тормоза» связана с худшим прогнозом.
Как IL8 выключает Shp1 и перепрограммирует ключевой рецептор
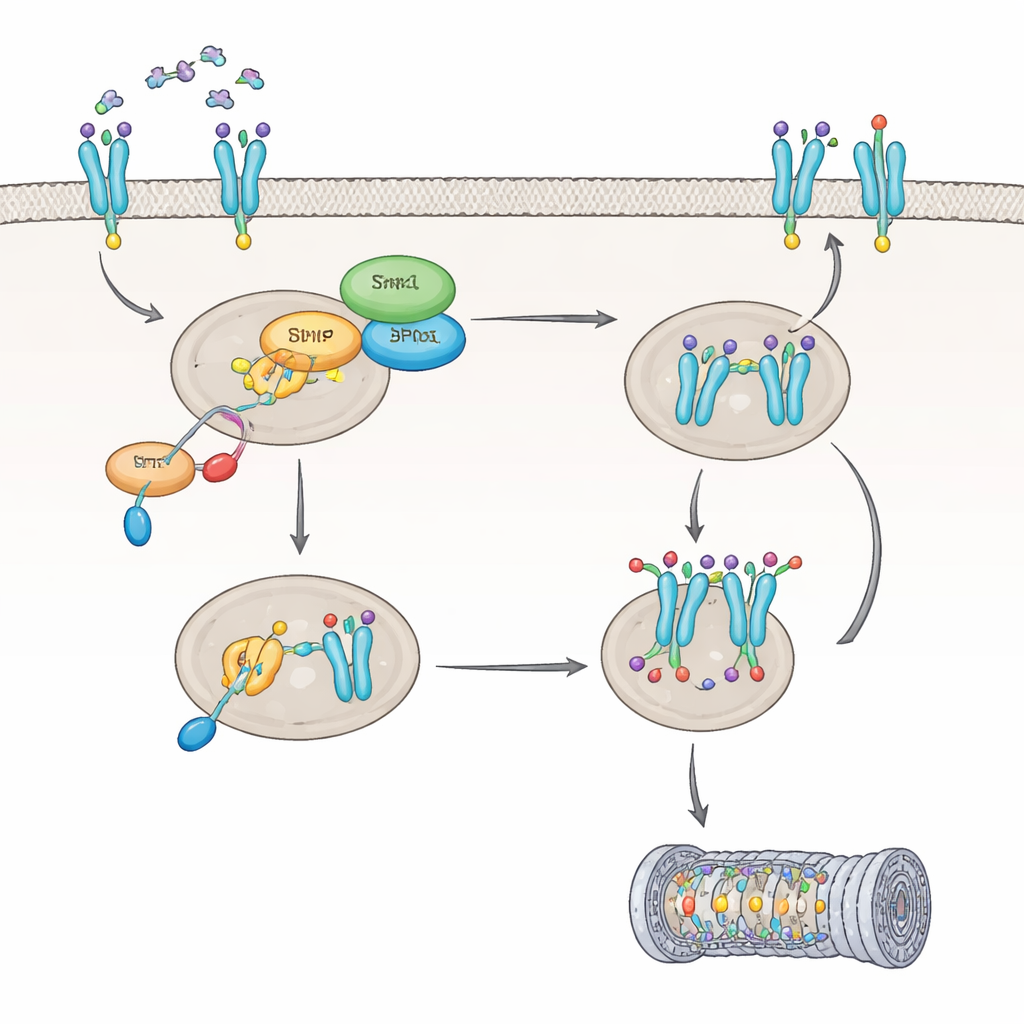
Далее команда изучала, как IL8 влияет на сам Shp1. Они обнаружили, что IL8 активирует белок PKC, который метит Shp1 в определенном участке, снижая его ферментативную активность примерно на 60 процентов. При таком подавлении Shp1 другой фермент, PP2A, становится менее активным, и рецептор CXCR2 сохраняется в сильно модифицированном состоянии, что меняет его судьбу внутри клетки. Вместо того чтобы быть очищенным и рециклированным обратно на поверхность клетки, CXCR2 помечается для разрушения, главным образом через протеасомную систему. Особая модификация на CXCR2, в аминокислоте Ser347, оказалась ключевой для присоединения этих меток на деградацию. В клетках, лишенных Shp1, CXCR2 помечался сильнее и разрушался быстрее, что приводило к меньшему числу рецепторов на поверхности клетки и ослабленной реакции на IL8 с течением времени.
Разные типы рака молочной железы — разные связи
Рак молочной железы — это не единая болезнь; опухоли классифицируют как люминальные, HER2-положительные и тройной-негативные по профилю рецепторов. Исследователи протестировали цепочку IL8–CXCR2–Shp1 в нескольких линиях клеток, представляющих каждый подтип. В люминальных и тройной-негативных клетках IL8 активировал каскад Shp1–PP2A–CXCR2, а блокада Shp1 как повышала базовую инвазивность, так и устраняла обычный проинвазивный эффект IL8. Напротив, в HER2-положительных клетках ответ на IL8 сохранялся, но блокада Shp1 почти не меняла их поведения, что предполагает: в этих опухолях Shp1 вовлечен в другие сигналы, такие как HER2, и менее доступен для регуляции CXCR2. Крупномасштабный анализ экспрессии генов подтвердил эту картину: тройной-негативные линии, как правило, имели более низкий уровень Shp1, измененную сигнализацию, связанную с GPCR, и более высокий IL8, что согласуется с более агрессивным, опосредованным воспалением профилем.
Что это означает для будущего лечения
Для неспециалиста основная идея такова: фермент Shp1 действует как регулятор движения для рецептора IL8, CXCR2, определяя, будет ли рецептор перенаправлен на повторное использование или уничтожен, а значит — насколько сильно клетки рака молочной железы будут реагировать на воспалительные сигналы. В люминальных и тройной-негативных раках молочной железы этот контрольный узел особенно важен: при низком уровне Shp1 или его блокаде клетки становятся более инвазивными, а прогноз пациентов ухудшается. Поскольку активность Shp1 можно повысить или модулировать с помощью некоторых существующих препаратов, нацеливание на ось Shp1–CXCR2, возможно в сочетании с блокаторами IL8 или CXCR2, может стать новой стратегией ограничения инвазии и метастазирования в агрессивных подтипах рака молочной железы.
Цитирование: Monti, M., Amendola, P.G., Filograna, A. et al. Shp1 phosphatase regulates CXCR2 protein stability and IL8-mediated invasiveness in breast cancer. Cell Death Dis 17, 297 (2026). https://doi.org/10.1038/s41419-026-08516-4
Ключевые слова: инвазия рака молочной железы, сигнализация IL8, рецептор CXCR2, фосфатаза Shp1, тройной-негативный рак молочной железы