Clear Sky Science · ru
CRMP2 ингибирует формирование метастазов, нарушая ILF3-зависимую стабилизацию мРНК CXCL10 при раке молочной железы
Почему важно остановить распространение рака
Большинство смертей от рака молочной железы происходит не из‑за первичной опухоли, а потому что раковые клетки мигрируют в жизненно важные органы, например в легкие, и образуют там новые очаги. В этом исследовании выявлен встроенный защитный белок внутри раковых клеток молочной железы, который может замедлять или даже блокировать это распространение, изменяя «приветственный коврик», который отдаленные органы расстилают для блуждающих раковых клеток. Понимание этого скрытого предохранителя может открыть путь к новым методам лечения, которые препятствуют закреплению рака в других частях тела.
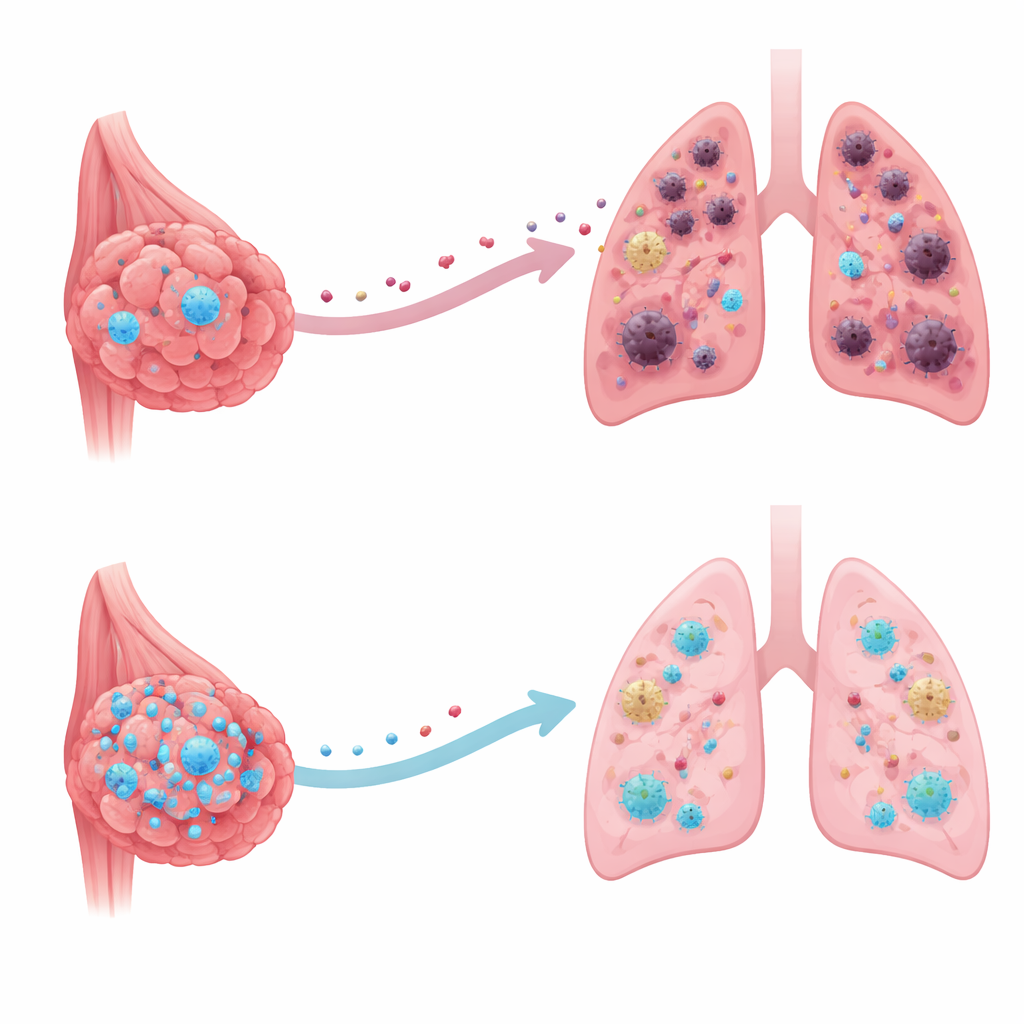
Тихий защитник внутри раковых клеток
Исследователи сосредоточились на белке под названием CRMP2, наиболее известном своей ролью в росте нейронов и поддержании их цитоскелета. При анализе крупных общедоступных баз данных по раку и образцов опухолей пациентов они обнаружили, что уровни CRMP2 существенно понижены в опухолях молочной железы, особенно в тех, что уже дали метастазы. У пациентов, у которых в опухолях сохранялись более высокие уровни CRMP2, наблюдалась лучшая выживаемость и меньшая вероятность развития отдаленных метастазов. Эта закономерность указывала на то, что CRMP2 скорее выполняет роль тормоза, чем ускорителя при раке молочной железы — действует как внутренний защитник, а не драйвер болезни.
Как легкие подготавливают к инвазии
Раковые клетки редко попадают в отдаленный орган внезапно. Задолго до их прибытия первичная опухоль выделяет молекулы, которые перестраивают этот орган в так называемую «предметастатическую нишу» — микроокружение, благоприятствующее выживанию рака. С помощью хорошо зарекомендовавшей себя модели на мышах, которая близко имитирует человеческий рак молочной железы, команда показала, что при искусственном усилении продукции CRMP2 в опухолевых клетках первичные опухоли росли с той же скоростью, но легкие становились гораздо менее гостеприимными. Маркеры воспаления и ремоделирования тканей в легких снижались, и в меньшем количестве привлекались иммунные клетки, обычно подавляющие противоопухолевую защиту. В результате после удаления основной опухоли в легких образовывалось значительно меньше метастатических узелков.
Сигнальная цепочка, вызывающая проблемы
Углубляясь, ученые выясняли, какие секретируемые опухолью сигналы подготавливают легкие. Они сосредоточились на CXCL10 — небольшом сигнальном белке (хемокине), известном способностью привлекать определенные иммунные клетки и пробуждать дремлющие раковые клетки. В клеточных линиях человека и мыши, выращенных в лаборатории, повышение CRMP2 резко сокращало синтез и секрецию CXCL10. У мышей легкие, подвергшиеся воздействию опухолевого материала с высоким содержанием CRMP2, имели значительно меньше CXCL10 и меньше входящих иммунных клеток, которые обычно ослабляют активность Т‑клеток. Когда исследователи блокировали CXCL10 антителом, колонизация легких раковыми клетками уменьшалась; обратное добавление CXCL10 устраняло защитный эффект CRMP2. Это поместило CXCL10 непосредственно ниже по цепочке от CRMP2 как ключевого инициатора образования метастазо‑благоприятной ниши.
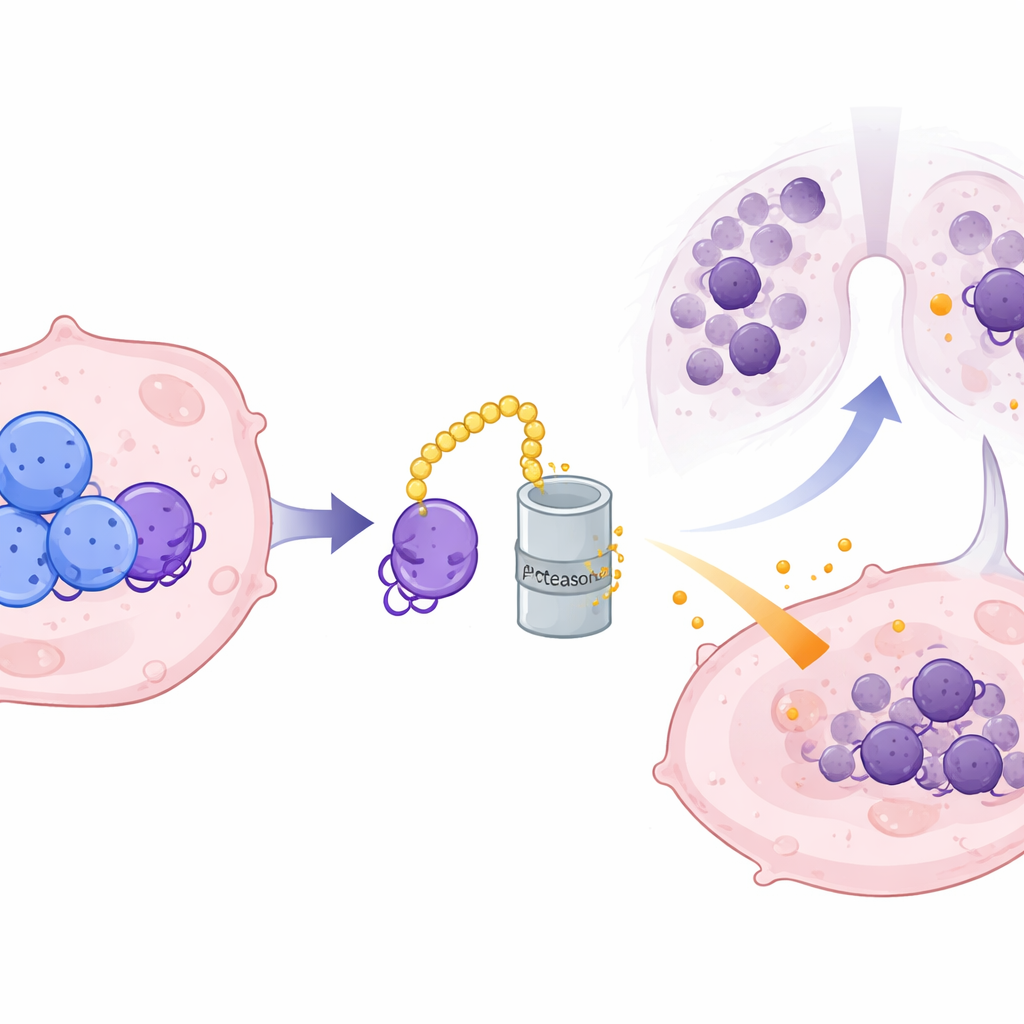
Скрытый посредник, стабилизирующий вредоносные сигналы
Поскольку CRMP2 находится внутри клетки, а CXCL10 секретируется, команда заподозрила молекулярного посредника. Они идентифицировали ILF3, РНК‑связывающий белок, как прямого партнера CRMP2. ILF3 прикрепляется к молекуле РНК, кодирующей CXCL10, и обычно защищает её от разрушения, позволяя синтезироваться большему количеству белка CXCL10. CRMP2 связывается с ILF3 в определённых контактных точках и помечает его для уничтожения через систему утилизации белков клетки, сокращая жизненный цикл ILF3 и нарушая его влияние на РНК CXCL10. При высоких уровнях CRMP2 ILF3 деградирует быстрее, РНК CXCL10 становится нестабильной, и секреция провоспалительного хемокина уменьшается. Искусственное восстановление ILF3 отменяло подавление CXCL10 со стороны CRMP2, подтверждая роль ILF3 как ключевого звена в этой цепочке.
Преобразование растительного соединения в потенциального союзника
Чтобы проверить, можно ли использовать этот путь в терапевтических целях, исследователи просcreenировали библиотеку естественных соединений и обнаружили, что псорален — растительная молекула, давно применяющаяся в дерматологии — связывается прямо с CRMP2 и делает его более стабильным. В клеточных экспериментах псорален повышал уровни CRMP2, снижал ILF3 и CXCL10 и уменьшал инвазивное поведение клеток рака молочной железы, не влияя на их общую жизнеспособность. В нескольких моделях на мышах псорален не уменьшал размеры первичных опухолей молочной железы, но значительно снижал число метастазов в легких и ослаблял формирование предметастатической ниши — опять же в зависимости от CRMP2. Хотя сам псорален может вызывать печёночную токсичность и требует доработки, эти результаты показывают, что небольшие молекулы способны усилить защитную роль CRMP2.
Что это значит для пациентов
В целом это исследование выявляет защитную ось внутри клеток рака молочной железы, где CRMP2 дестабилизирует ILF3, что в свою очередь снижает CXCL10 и не позволяет легким стать благоприятной средой для метастазов. Вместо прямой атаки на раковые клетки такая стратегия нацелена на обезвреживание отдалённых ниш, от которых те зависят, переключая баланс в пользу собственных защитных механизмов организма. Хотя до клинического применения ещё далеко, нацеленность на путь CRMP2–ILF3–CXCL10 — возможно, с помощью более безопасных соединений, подобных псоралену — предлагает перспективный новый подход к предотвращению распространения рака молочной железы.
Цитирование: Lin, B., Luo, M., Zhou, Y. et al. CRMP2 inhibits metastasis formation by impairing ILF3-dependent stabilization of CXCL10 mRNA in breast cancer. Cell Death Dis 17, 255 (2026). https://doi.org/10.1038/s41419-026-08515-5
Ключевые слова: метастазы рака молочной железы, предметастатическая ниша, хемокиновая сигнализация, РНК‑связывающие белки, терапевтические натуральные соединения