Clear Sky Science · ru
CCL11 способствует рецидиву гепатоцеллюлярной карциномы после операции, усиливая иммуноподавляющие CCR5 + CD206 + M2-подобные макрофаги и повышая инвазивность опухоли
Почему рак печени может вернуться после операции
Хирургическое вмешательство по поводу рака печени часто является наилучшим шансом для пациентов на ранних стадиях заболевания, но у многих опухоль возвращается в течение нескольких лет. В этом исследовании поставлен простой, но важный вопрос: не помогает ли собственный воспалительный ответ организма на операцию случайно выжившим раковым клеткам выживать и распространяться? Авторы фокусируются на сигнальной молекуле CCL11 и показывают, как всплеск этой молекулы после операции может одновременно ослаблять противоопухолевый иммунитет и делать оставшиеся опухолевые клетки более агрессивными.
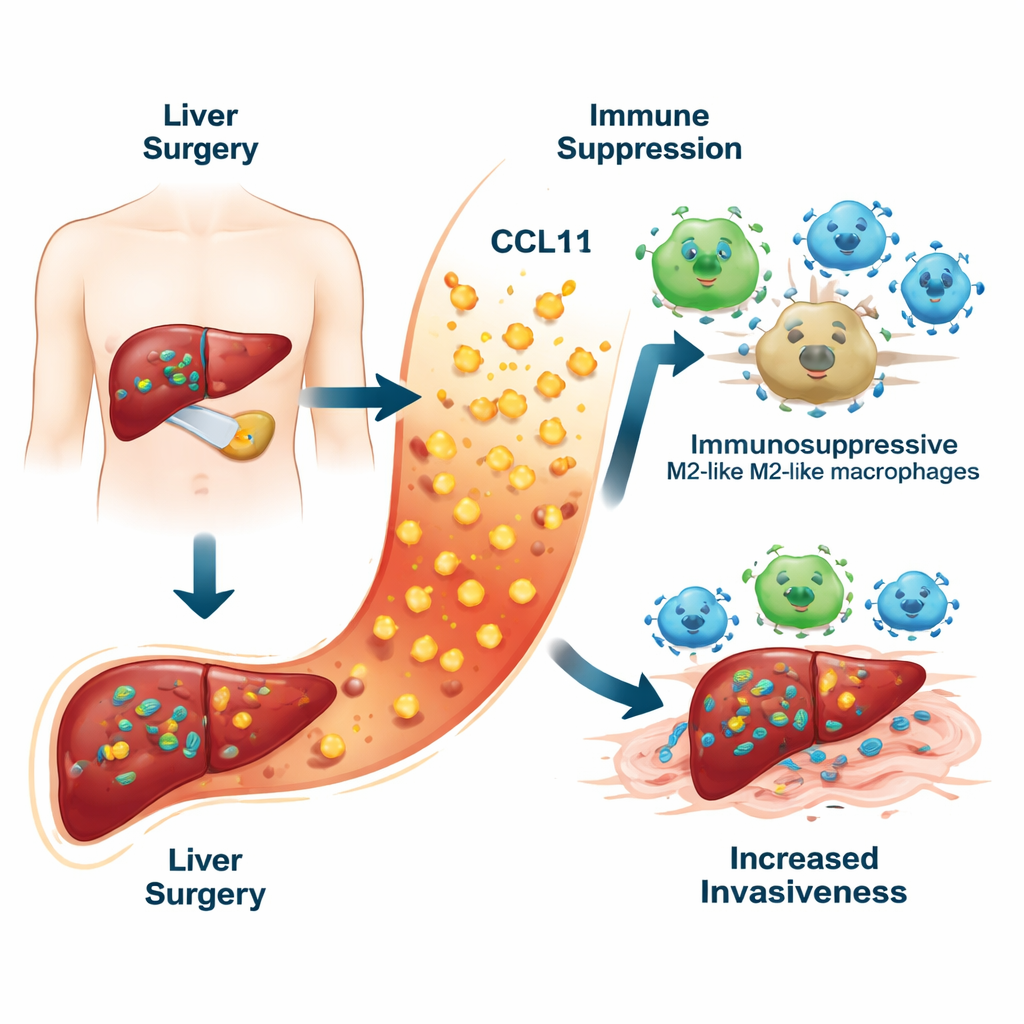
Скрытая опасность в процессе заживления
Когда хирурги удаляют опухоль печени, им приходится пережимать сосуды и повреждать окружающие ткани. Это повреждение вызывает волну воспаления, которая помогает печени восстановиться. Измерив десять разных воспалительных молекул в крови пациентов через неделю после операции, команда обнаружила, что один хемокин, CCL11, выделялся особенно ярко. У пациентов, у которых впоследствии наблюдался рецидив рака печени, уровни CCL11 были значительно выше, чем у тех, кто оставался свободным от болезни. Высокие уровни CCL11 также ассоциировались с худшей выживаемостью. Комбинируя CCL11 с рутинными клиническими данными — такими как анализы крови и характеристики опухоли — исследователи создали «оценочную карту» риска, которая точнее предсказывала пятилетний рецидив по сравнению с традиционными моделями.
Даже ткань печени, выглядящая нормально, имеет значение
Большинство исследований сосредоточены на самой опухоли, но это исследование показывает, что окружающая «нормальная» печеночная ткань может быть не менее важной. В образцах более чем 100 пациентов CCL11 оказался фактически выше в нетуморной ткани печени, чем в раковых узлах или в печени доноров. У пациентов, у которых окружающая печень вырабатывала больше CCL11, чаще встречались прогрессирующее заболевание, отдаленные метастазы и рецидив после операции. В мышиных моделях, имитирующих кратковременную потерю и восстановление кровотока во время операции, повреждение печени быстро повышало уровни CCL11. В условиях низкого содержания кислорода в лаборатории клетки, поддерживающие печень — такие как миофибробласты и эндотелиальные клетки сосудов — также увеличивали продукцию CCL11, что позволяет предположить, что хирургический стресс подготавливает остаток печени к приобретению проопухолевого фенотипа.
Как CCL11 превращает защитников иммунитета в наблюдателей
Чтобы понять, как CCL11 формирует иммунитет, авторы сосредоточились на макрофагах — универсальных лейкоцитах, которые могут либо атаковать опухоль, либо защищать её. Они обнаружили, что в нетуморной ткани печени более высокие уровни CCL11 коррелировали с увеличением подтипа макрофагов, несущих маркер CCR5 и проявляющих так называемый M2-подобный, опухоле-дружественный профиль. У пациентов печень, богатая этими CCR5+ M2-подобными макрофагами, была связана с худшей выживаемостью. В культурах клеток добавление CCL11 направляло моноциты в этот иммуноподавляющий макрофагальный тип, усиливая молекулы, такие как PD‑L1 и IL‑10, и выделяя другие сигналы, привлекающие и переориентирующие дополнительные иммунные клетки. Эти макрофаги, кондиционированные CCL11, затем способствовали превращению наивных хелперных Т-клеток в регуляторные Т-клетки — популяцию, известную подавлением противоопухолевых ответов. Механистические эксперименты показали, что CCL11 активирует каскад сигналов внутри макрофагов, который завершается активацией пути NF‑κB и повышенным производством PD‑L1, помогая защищать раковые клетки от иммунного нападения.
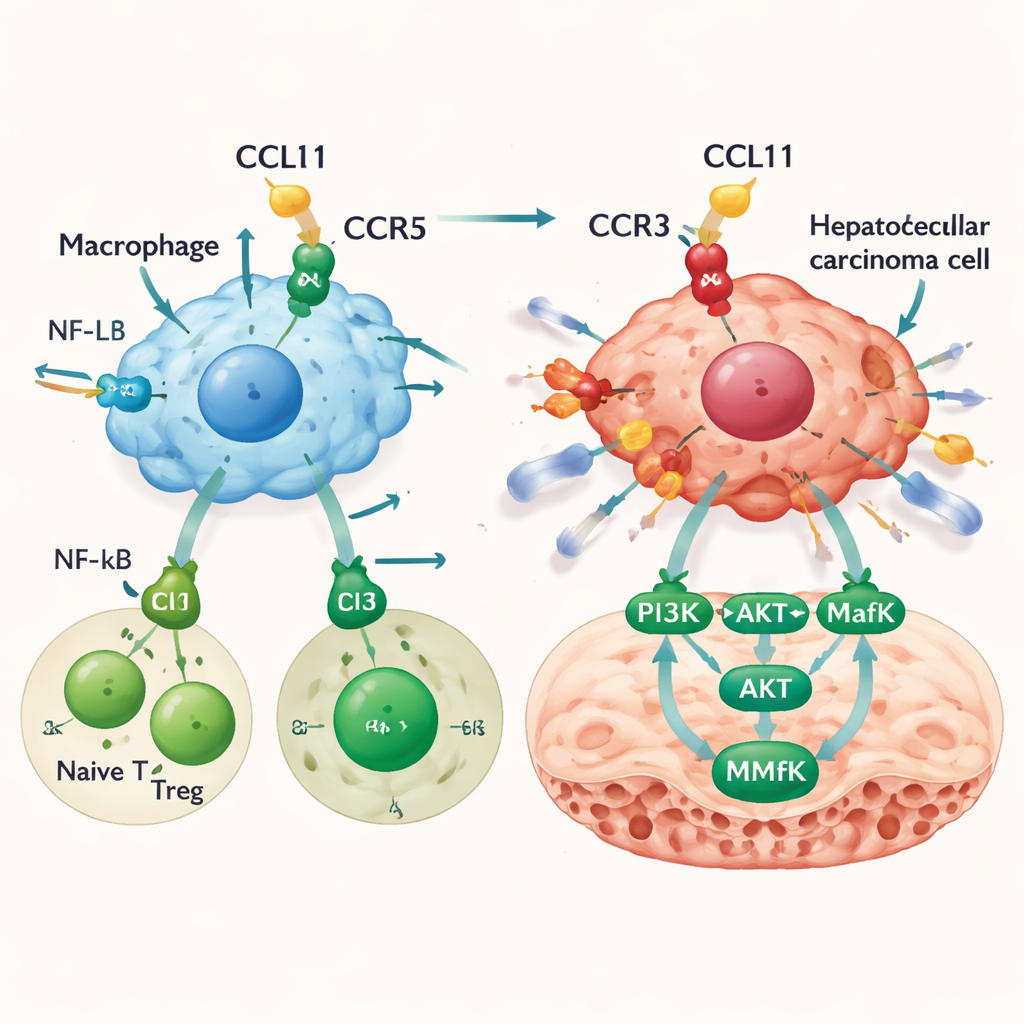
Как CCL11 делает оставшиеся раковые клетки более инвазивными
CCL11 не только перестраивает иммунную среду; она также действует непосредственно на раковые клетки печени. Хотя сами раковые клетки производят мало CCL11, у них имеется один из её рецепторов — CCR3. В лабораторных тестах CCL11 не ускорял пролиферацию клеток рака печени, но делал их более подвижными и проникающими через барьеры — признак повышенного метастатического потенциала. Блокирование рецептора CCR3 во многом устраняло этот эффект. Генные анализы указывали на путь, в котором сигнализация CCL11–CCR3 включает PI3K и AKT, что затем активирует транскрипционный фактор MafK. MafK, в свою очередь, усиливает экспрессию MMP13 — фермента, разрушающего окружительную матрицу и открывающего пути для распространения рака. В мышиных моделях инфузия CCL11 в печень увеличивала опухолевую нагрузку и приводила к большему числу метастазов, параллельно с повышением активности пути PI3K–AKT–MafK–MMP13 в опухолях.
Преобразование рискованного сигнала в терапевтическую возможность
Поскольку CCL11, по-видимому, одновременно подавляет иммунную защиту и укрепляет остаточные раковые клетки, исследователи проверили, может ли её блокада после операции изменить исход. У мышей с опухолями печени, которым была выполнена хирургическая резекция, лечение антителом, нейтрализующим CCL11, заметно снизило частоту рецидивов в печени и улучшило выживаемость, без очевидных побочных эффектов, таких как потеря веса. В совокупности результаты представляют CCL11 как ключевой переключатель, связывающий хирургическое повреждение с иммуноподавляющей и инвазионно-способствующей средой в оставшейся печени. Для пациентов это исследование подразумевает, что измерение уровней CCL11 после операции могло бы помочь выявить наиболее подверженных рецидиву, а лекарства, нацеленные на ось CCL11–CCR5/CCR3, возможно, однажды станут частью стратегий предотвращения возврата рака печени.
Цитирование: Wang, J., Yeung, O.WH., Qiu, W. et al. CCL11 promotes hepatocellular carcinoma recurrence after surgery by potentiating immunosuppressive CCR5 + CD206 + M2-like macrophages and promoting tumor invasiveness. Cell Death Dis 17, 236 (2026). https://doi.org/10.1038/s41419-026-08508-4
Ключевые слова: рецидив рака печени, хемокин CCL11, опухолевая микроокружение, иммунная супрессия, метастазирование рака