Clear Sky Science · ru
Фибробласты, ассоциированные с раком, способствуют резистентности к осимертинибу в клетках немелкоклеточного рака легкого через m7G-модификацию NET1, опосредованную METTL1
Почему некоторые раки легкого перестают реагировать на «умный» препарат
Таргетные препараты, такие как осимертиниб, изменили подход к лечению многих пациентов с распространенным типом рака легкого, предоставив более длительную выживаемость и меньше побочных эффектов по сравнению с традиционной химиотерапией. Однако у большинства пациентов эти преимущества носят временный характер: опухоли рано или поздно находят способы обойти действие препарата. В этом исследовании поставлен на первый взгляд простой, но важный вопрос: не помогает ли поддерживающая ткань опухоли — в частности клетки, называемые фибробластами, ассоциированными с раком — незаметно раковым клеткам уклоняться от воздействия осимертиниба?
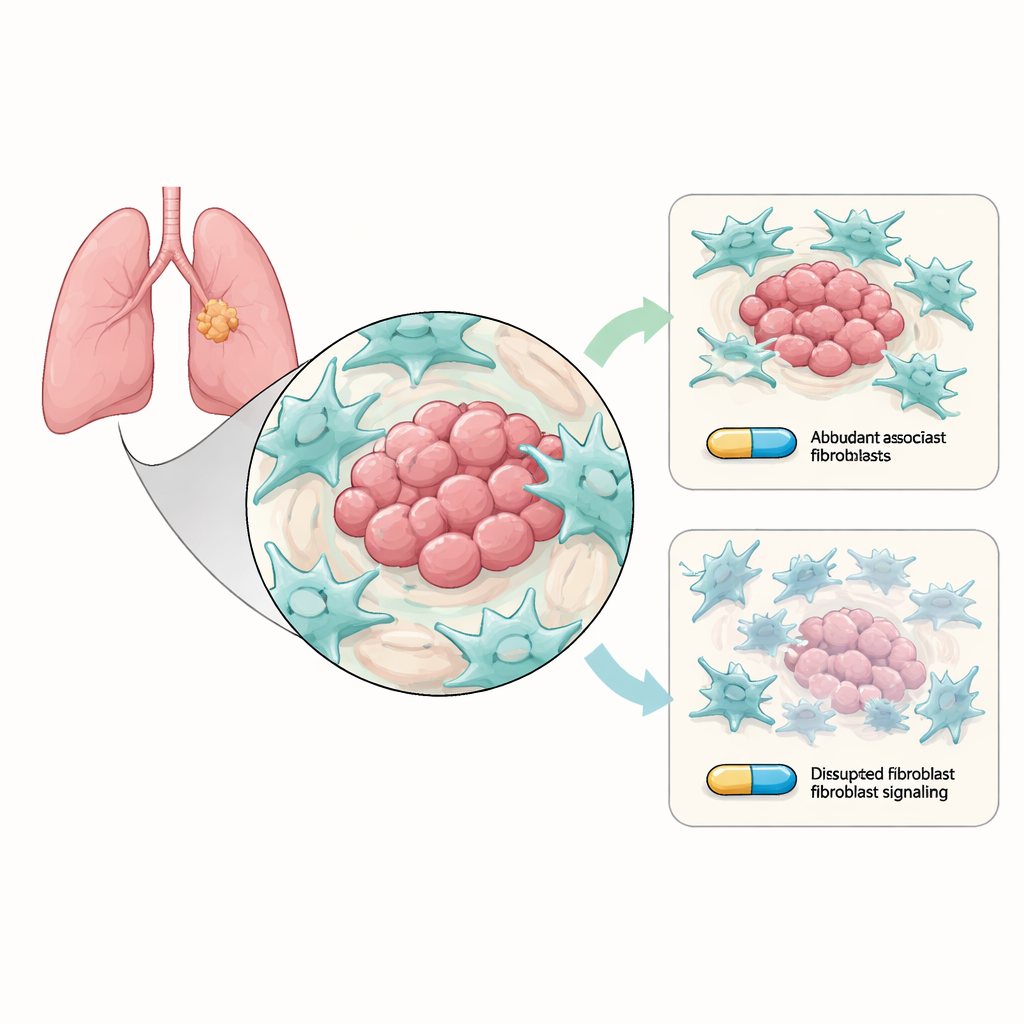
Помощники, которые тайно защищают опухоль
Немелкоклеточный рак легкого развивается в окружении многочисленных нераковых клеток, известном как опухолевый микроокружение. Одними из наиболее многочисленных жителей являются фибробласты, ассоциированные с раком (CAF), клетки соединительной ткани, перестраивающие пространство вокруг опухоли. Исследователи выращивали в лаборатории раковые клетки легкого с обычными чувствительными к осимертинибу мутациями EGFR совместно с CAF. Они обнаружили, что в присутствии CAF раковые клетки труднее убить осимертинибом: они образовывали больше колоний, реже подвергались апоптозу и демонстрировали усиленные «стволоподобные» признаки, связанные с долгосрочным выживанием и рецидивом. Другими словами, хотя препарат продолжал нацеливаться на раковые клетки, окружающие фибробласты тихо помогали им выживать.
Химическая метка на РНК, которая меняет правила
Дальше команда посмотрела не только на сами гены, но и на химические метки, украшающие РНК — рабочие копии генетической информации внутри клеток. Одна из таких меток, называемая m7G, может влиять на стабильность молекулы РНК и на то, насколько эффективно она трансляционируется в белок. С помощью биохимических тестов и картирования в масштабе генома исследователи показали, что CAF увеличивают общий уровень м7G-модификаций на РНК внутри раковых клеток легкого. Это усиление в основном обеспечивалось метилтрансферазой METTL1, которая наносит m7G-метки на мРНК. Уровни METTL1 были выше в опухолях легкого по сравнению с прилежащей нормальной тканью и коррелировали с более поздними стадиями болезни и худшей выживаемостью пациентов, что указывает на то, что этот фермент делает нечто большее, чем просто тонкую настройку рутинных клеточных функций.
Секретный сигнал и уязвимая молекулярная цепочка
Как CAF повышают METTL1 в раковых клетках? Исследование указывает на белок HMGB1, который CAF выделяют в окружающую среду. По сравнению с раковыми клетками CAF секретировали значительно больше HMGB1. Когда исследователи добавляли HMGB1 к раковым клеткам легкого, уровни METTL1 и отметок m7G повышались; когда они блокировали HMGB1 в среде, кондиционированной CAF, этот эффект ослабевал. При более тщательном рассмотрении они выделили ключевую РНК-мишень для METTL1: NET1, ген, способствующий росту и подвижности клеток. CAF увеличивали и m7G-метки, и количество РНК и белка NET1, а METTL1 физически связывался с РНК NET1, стабилизируя ее. Снижение METTL1 приводило к уменьшению модифицированного NET1, ослаблению сигнальных путей выживания раковых клеток и повышению чувствительности к осимертинибу.
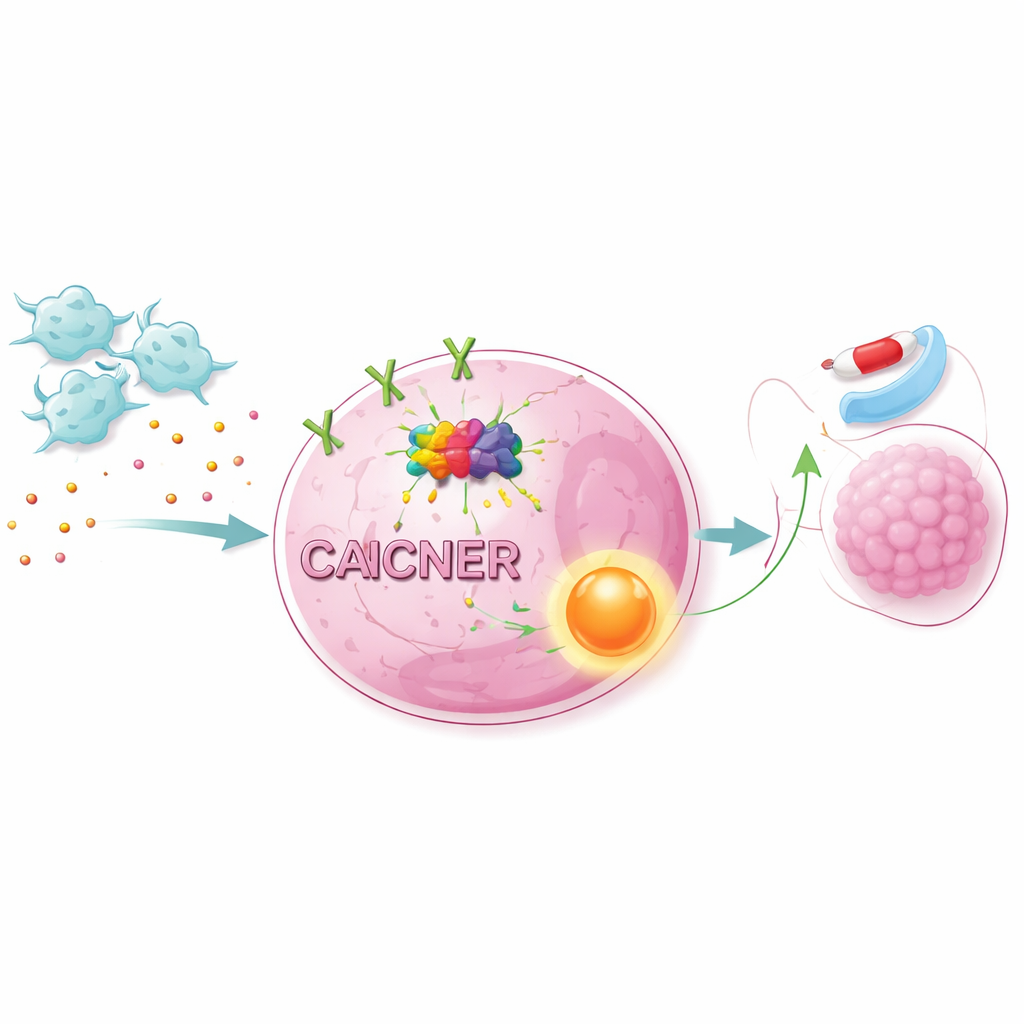
Включение путей выживания внутри раковых клеток
Усиленный сигнал NET1 не действовал в одиночку. Объединив данные по масштабному профилю РНК с анализом путей, ученые показали, что CAF активируют важный путь роста и выживания внутри клеток, известный как путь AKT/NF-κB. Блокирование AKT или NF-κB с помощью специфических ингибиторов делало раковые клетки легкого более уязвимыми к осимертинибу, даже в присутствии CAF. Изменение уровней NET1 давало похожие эффекты: снижение NET1 ослабляло защиту, обеспечиваемую CAF, тогда как повышение NET1 усиливало резистентность. У мышей, трансплантированных человеческими раковыми клетками легкого, добавление CAF приводило к более быстрому росту опухолей и меньшей чувствительности к осимертинибу. Подавление METTL1 в раковых клетках снижало m7G-метки, уменьшало уровни NET1 и активацию путей и заметно сокращало рост опухолей, индуцированный CAF.
Что это значит для будущего лечения рака легкого
Для пациентов с EGFR-мутационным раком легкого эта работа предлагает новый взгляд на то, почему мощные препараты вроде осимертиниба в конце концов перестают действовать. Вместо того чтобы винить только новые мутации в самих раковых клетках, исследование выделяет молекулярную цепочку, которая начинается вне опухолевой клетки — с выделения HMGB1 фибробластами — и проходит через METTL1, m7G-метки на NET1 и активацию путей выживания, смягчающих эффект препарата. Прерывание этой цепочки в любой ее точке, теоретически, могло бы восстановить или продлить чувствительность к лечению. Хотя препараты, которые прямо нацелены на METTL1, HMGB1 или специфические m7G-модифицированные РНК, пока находятся на ранних стадиях разработки, исследование предполагает, что комбинация осимертиниба с терапиями, направленными на поддерживающие клетки опухоли или их сигналы модификации РНК, может помочь дольше контролировать этот вид рака легкого.
Цитирование: Qian, Y., Gong, Z., Jia, Y. et al. Cancer-associated fibroblasts promote osimertinib resistance in non-small cell lung cancer cells via METTL1-mediated NET1 m7G modification. Cell Death Dis 17, 248 (2026). https://doi.org/10.1038/s41419-026-08505-7
Ключевые слова: резистентность к осимертинибу, немелкоклеточный рак легкого, фибробласты, ассоциированные с раком, метилирование РНК, путь METTL1–NET1