Clear Sky Science · ru
miR-424(322)~503 нарушает прогрессирование рака ободочной кишки, вызванное дефицитом PTEN
Почему это исследование важно для рака толстой кишки
Рак ободочной кишки остаётся одним из самых распространённых и смертельных видов рака в мире: у многих пациентов заболевание прогрессирует до поздних стадий, несмотря на операцию, химиотерапию и таргетные препараты. В этом исследовании изучается небольшая группа генетических «диммеров» — микроРНК, которые могут замедлять или ускорять рост опухоли. Раскрывая, как один конкретный кластер микроРНК взаимодействует с хорошо изученным геном-супрессором опухолей PTEN, работа помогает объяснить, почему некоторые раки ободочной кишки становятся более агрессивными, и указывает на новые подходы к прогнозированию риска и разработке терапий.
Крошечные РНК-переключатели с большим эффектом
МикроРНК — это короткие молекулы РНК, которые не кодируют белки, но тонко регулируют экспрессию сотен генов в клетке. Кластер miR-424(322)~503, состоящий из двух родственных микроРНК, озадачивал учёных тем, что в разных типах рака он может действовать либо как тормоз, либо как ускоритель. В раке ободочной кишки его роль оставалась неясной. Авторы сосредоточили внимание на опухолях, развивающихся при утрате PTEN — гена, который обычно контролирует сигналы роста и часто нарушается при колоректальных опухолях. Они задали простой, но важный вопрос: что происходит с развитием рака ободочной кишки, когда оба компонента — PTEN и этот кластер микроРНК — отсутствуют?
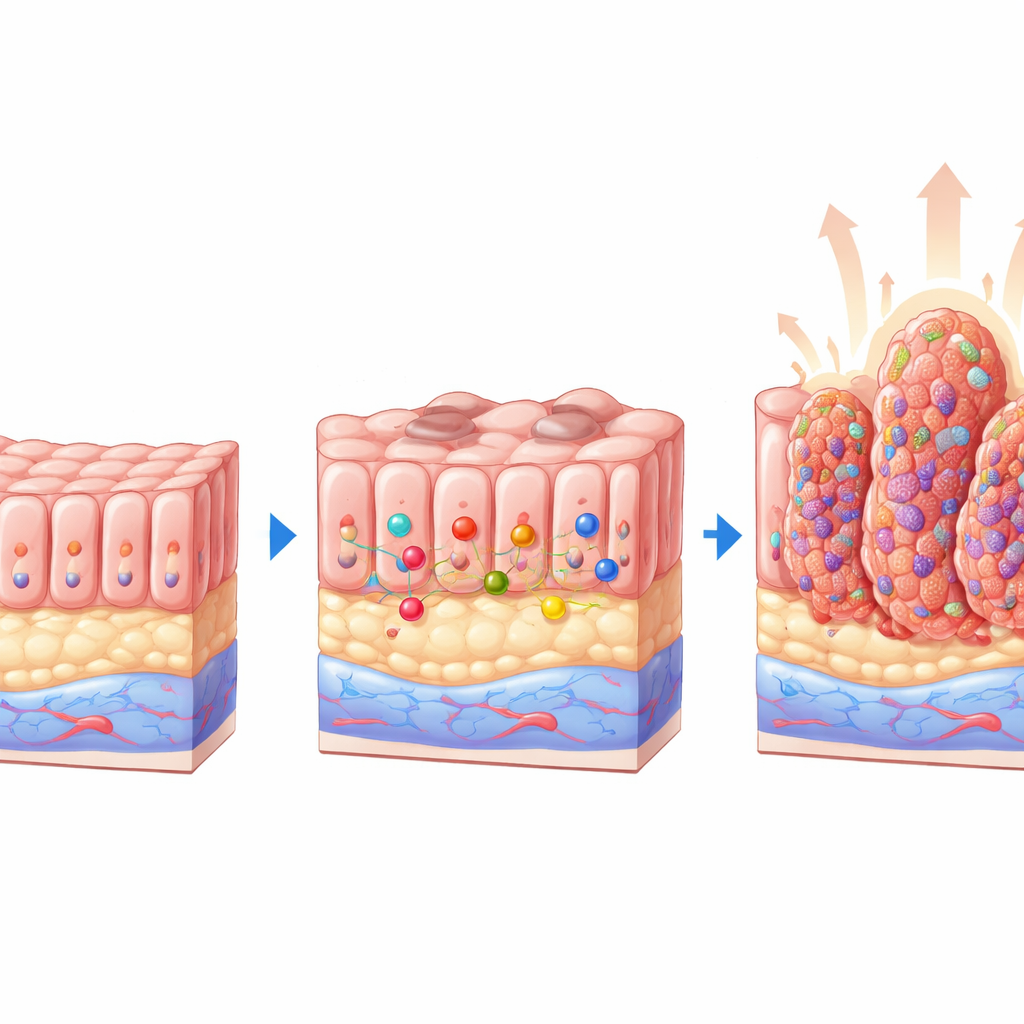
Мышиные модели показывают защитную роль
Чтобы ответить на этот вопрос, команда использовала генетически модифицированных мышей, у которых PTEN можно выключать в слизистой оболочке кишечника, и скрещивала их с мышами, лишёнными кластера miR-424(322)~503. Получили четыре группы: нормальные животные, мыши, лишённые только микроРНК, мыши с дефицитом только PTEN и двойные нокауты, лишённые обоих компонентов. После индукции потери PTEN исследователи внимательно осмотрели ободочные кишки. Животные с удалённым только PTEN развивали множество мелких полипов, многие из которых содержали ранние атипические изменения. В резком контрасте у мышей, лишённых и PTEN, и кластера микроРНК, было гораздо больше поражений, полипы были крупнее, а доля продвинутых изменений, включая высокодифференцированную дисплазию и явную аденокарциному, была выше. Сам кластер микроРНК не вызывал заболевания, что показывает: его утрата особенно вредна на фоне уже отсутствующего PTEN.
Классический путь не изменился, но включились новые виновники
Часто рост рака толстой кишки обусловлен переактивацией пути Wnt/β-катенин, ключевого маршрута, контролирующего стволовые клетки в кишечнике. Поскольку этот кластер микроРНК может влиять на этот путь в грудной ткани, авторы проверили, так ли это и здесь. Удивительно, но уровни и локализация β-катенина и его корецептора LRP6 в ободочной кишке не изменялись при удалении кластера микроРНК, даже в двойных нокаутах. Вместо этого масштабный анализ экспрессии генов указал в другую сторону: опухоли, лишённые и PTEN, и микроРНК, демонстрировали сильные сигнатуры ремоделирования ткани, ответа на повреждение и эпителиально-мезенхимального перехода — программы, связанной с инвазивностью и метастазированием. Особенно обогащёнными оказались сигнальные маршруты, запускаемые MAP-киназами (ERK1/2 и p38) и фактором роста TGFβ.
Как сигналы роста выходят из-под контроля
Глубже исследуя белковый уровень в ткани ободочной кишки, учёные обнаружили, что при одной только потере PTEN усиливается путь PI3K/AKT, а при дополнительной утрате кластера микроРНК наблюдается дальнейший всплеск активности MAPK: увеличивается количество активированных JNK, p38, MKK4 и особенно ERK1/2. Эти сильно активированные сигналы совпадали с повышением уровня циклина D1, ключевого фактора, стимулирующего деление клеток. Одновременно компоненты пути TGFβ, усиливающие его активность (SMAD3 и SMAD4), возрастали, тогда как внутренний тормоз (SMAD7) снижался, а раковые клетки демонстрировали более выраженную ядерную окраску SMAD2/3 — признак активации пути. Сопоставляя гены мышиных опухолей с предполагаемыми целями микроРНК, команда идентифицировала IGF1 — мощный фактор роста, вовлечённый в MAPK-каскады — как прямую цель кластера miR-424(322)~503. При отсутствии этих микроРНК IGF1 освобождался от репрессии, дополнительно усиливая сигнализацию MAPK. Анализы данных человеческих колоректальных опухолей подтверждали эти наблюдения: IGF1 был выше в опухолях с низким уровнем miR-424 или miR-503, а длинная некодирующая РНК-хост MIR503HG и сами микроРНК координированно изменялись в образцах пациентов.
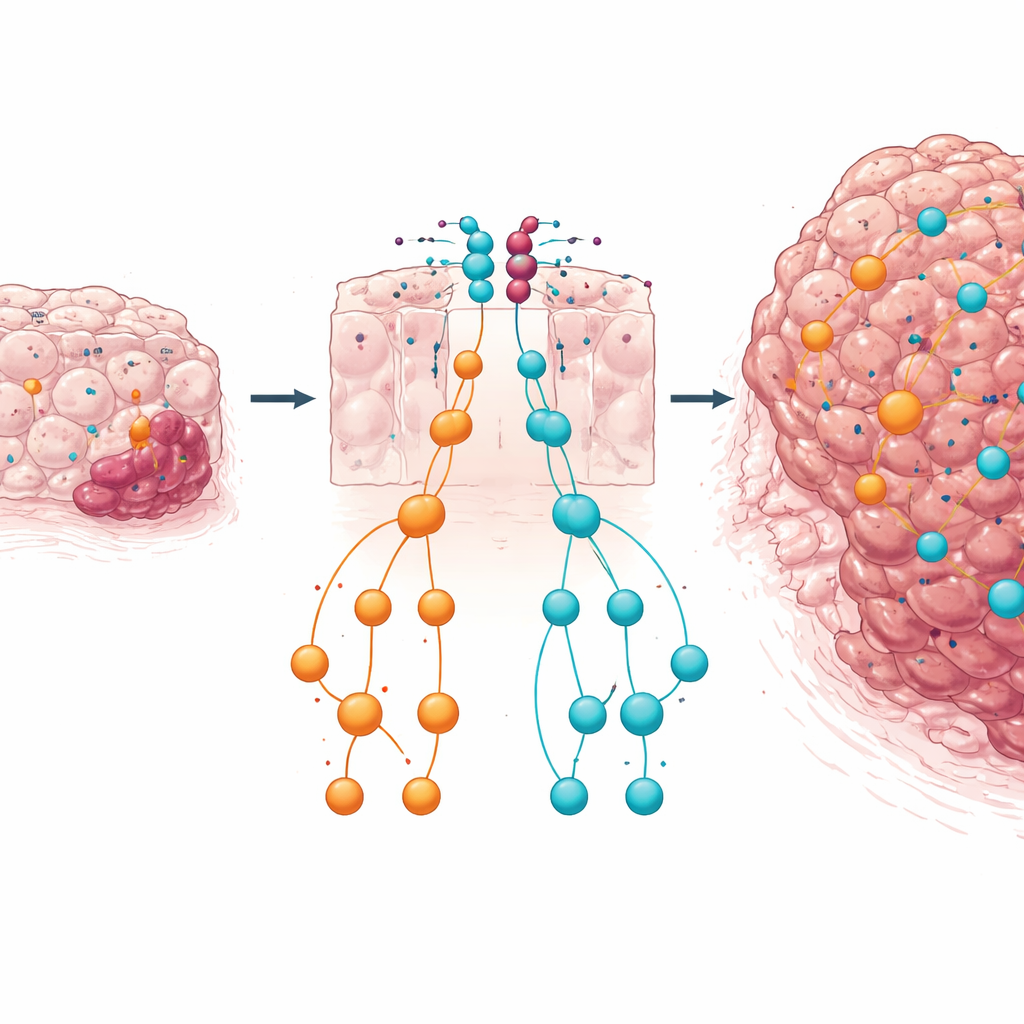
Двойная страховка и что это значит для пациентов
В целом результаты указывают на то, что в ткани ободочной кишки с дефектом PTEN кластер miR-424(322)~503 функционирует как второе защитное звено. При потере PTEN эти микроРНК повышают свою активность, отчасти через сигналы, такие как TGFβ, и сдерживают мощные пути роста, например IGF1–MAPK и TGFβ–SMAD. Если этот микроРНК-тормоз устраняется, сигналы роста и ремоделирования тканей выходят из-под контроля, ускоряя переход от доброкачественных полипов к инвазивному раку. Для непрофессионального читателя ключевое сообщение таково: не все генетические изменения в опухоли действуют в одном направлении — некоторые выполняют роль встроенных защит. Понимание того, как PTEN и этот кластер микроРНК взаимодействуют для поддержания баланса клеточного роста, может помочь выявлять пациентов с высоким риском и вдохновить на комбинированные подходы к лечению, направленные одновременно на оси PI3K/AKT и MAPK/TGFβ при колоректальном раке.
Цитирование: Vidal-Sabanés, M., Bonifaci, N., Navaridas, R. et al. miR-424(322)~503 impairs colon cancer progression driven by PTEN deficiency. Cell Death Dis 17, 254 (2026). https://doi.org/10.1038/s41419-026-08504-8
Ключевые слова: колоректальный рак, PTEN, микроРНК, сигнализация MAPK, TGF-бета