Clear Sky Science · ru
Подавление аутофагии, обусловленное mTOR, определяет метаболическую уязвимость при резистентности к ингибиторам CDK4/6 у HR+/HER2− рака молочной железы
Почему это важно для пациенток с раком молочной железы
Многие женщины с распространённым раком молочной железы теперь живут дольше благодаря препаратам, называемым ингибиторами CDK4/6, которые замедляют скорость деления опухолевых клеток. К сожалению, большинство опухолей со временем научается обходить действие этих лекарств. В этом исследовании ставится обнадёживающий вопрос: когда рак молочной железы становится резистентным к ингибиторам CDK4/6, не приобретает ли он новую уязвимость, которой врачи могли бы воспользоваться с помощью уже существующих и относительно простых метаболических препаратов, таких как метформин или дихлороацетат (DCA)?
Когда препараты, блокирующие клеточный цикл, перестают работать
Врачи часто лечат наиболее распространённый тип рака молочной железы — гормонально-рецептор‑положительный, HER2‑отрицательный — комбинацией гормональной терапии и ингибиторов CDK4/6, например палбоциклиба или рибоциклиба. Эти препараты нацелены на белки, которые продвигают клетки через цикл деления. Со временем, однако, некоторые раковые клетки адаптируются и становятся сильно резистентными, продолжая расти даже при высоких дозах препаратов. Исследователи воссоздали эту проблему в лаборатории, подвергая линии клеток рака молочной железы (T47D и MCF7) постепенному увеличению концентраций ингибиторов CDK4/6. В результате появились два типа выживших: частично резистентные клетки и меньшая популяция высокорезистентных клонов, которые уже не отвечали на лечение.
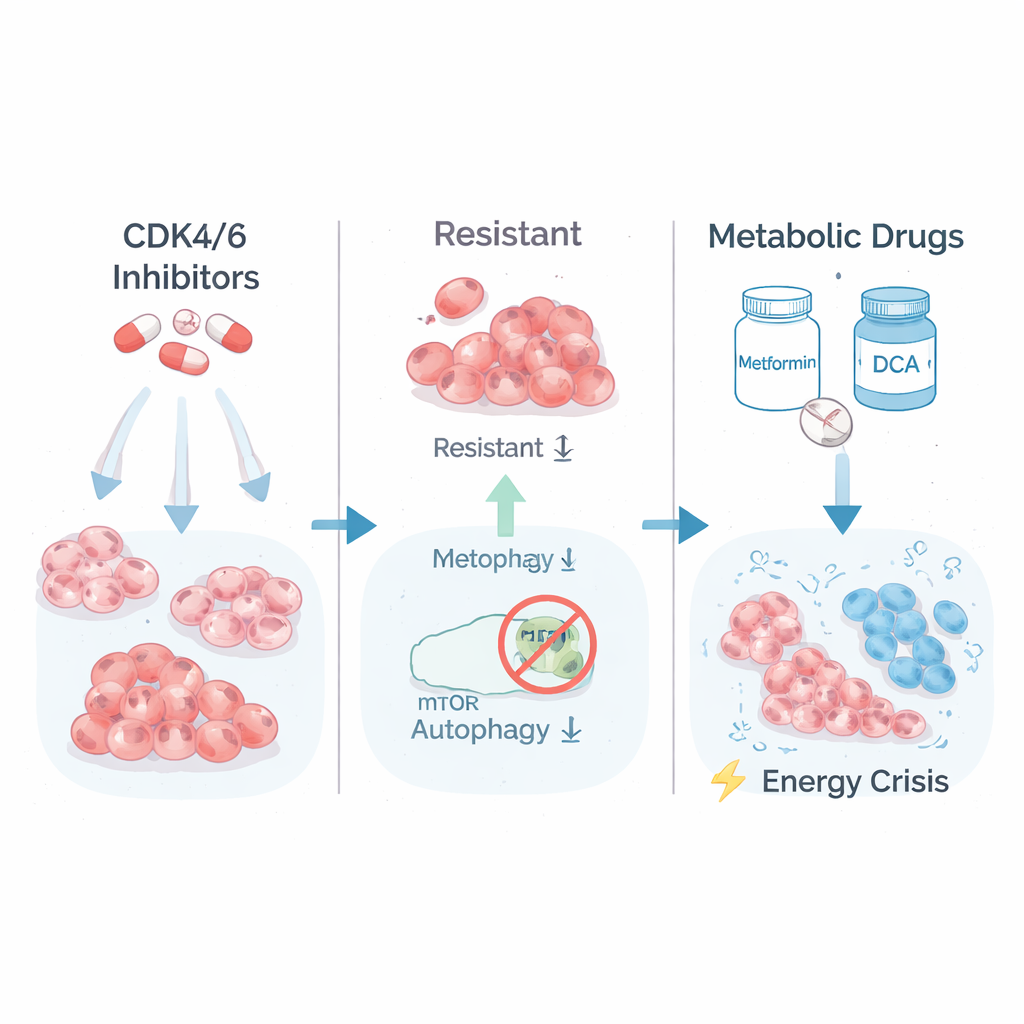
Скрытая уязвимость в использовании энергии опухолью
Чтобы понять, что отличало высокорезистентные клетки, команда изучила, какие гены были включены или выключены. Они обнаружили, что самые резистентные клетки усилили пути, связанные с расщеплением сахара (гликолизом), и сигнальными каскадами роста, контролируемыми белковым комплексом mTORC1. Иными словами, эти клетки работали в высоких оборотах, быстро сжигая топливо, чтобы продолжать рост. Ученые затем проверили, можно ли обратить эту «высокую передачу» метаболизма против самих клеток. Они обработали резистентные и исходные клетки метформином, широко применяемым при диабете препаратом, который нагружает энергетические станции клетки, и DCA, который заставляет клетки более эффективно перерабатывать топливо. Поразительно, самые лекарственно‑устойчивые клоны оказались наиболее уязвимыми: их долгосрочный рост в культурах почти прекратился под действием метаболического лечения, тогда как родительские и только частично резистентные клетки пострадали значительно меньше.
Блокированная «самоочистка» и энергетический крах
Почему эти ушедшие от лечения клетки оказались такими чувствительными к энергетическому стрессу? Ответ лежит в другом базовом процессе выживания: аутофагии, встроенной системы клетки по переработке и очистке материалов. Обычно при дефиците энергии клетки разрушают и повторно используют собственные компоненты, чтобы выжить. Исследователи показали, что в высокорезистентных клонах mTORC1 был сверхактивен и наложил химический тормоз на ULK1, ключевой инициатор аутофагии. С помощью чувствительного репортерного анализа они продемонстрировали, что эти клетки уже не могли должным образом включать или усиливать аутофагию, даже при нагрузке метаболическими препаратами. В результате метформин и DCA вызвали тяжёлый энергетический кризис: включились датчики низкой энергии, синтез жиров был подавлен и появились маркеры необратимой гибели клеток — причём исключительно в сильно резистентных клетках.
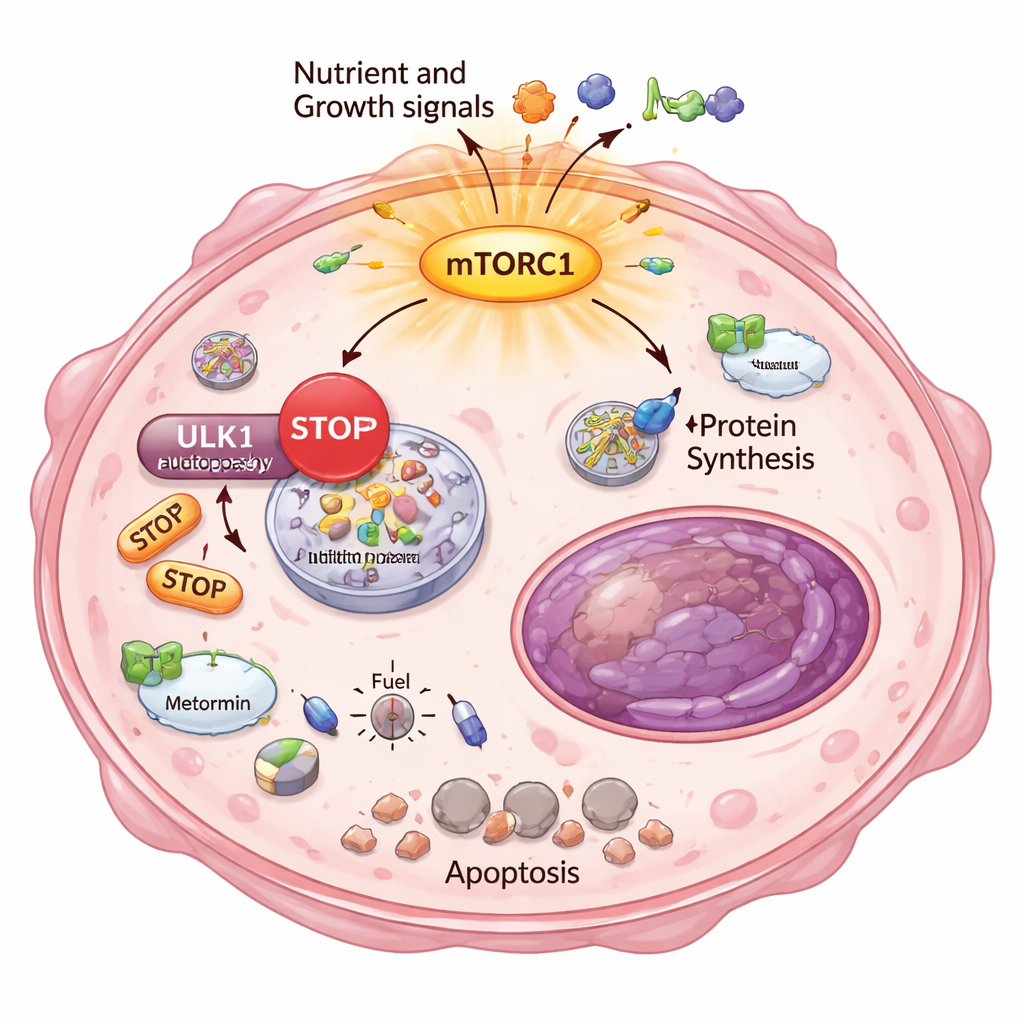
Доказательства из опухолей реальных пациенток
Лабораторные модели не всегда отражают то, что происходит у людей, поэтому исследователи обратились к образцам человеческих опухолей молочной железы. Они окрасили более сотни образцов на маркер активности mTORC1 (фосфорилированный 4E‑BP1) и на p62 — белок, который накапливается при блокированной аутофагии. Опухоли с высокой активностью mTORC1, как правило, имели больше p62, что поддерживает идею о том, что сочетание «перегруженного сигнала роста и плохой переработки» существует в реальных опухолях молочной железы, а не только в клеточных линиях. Это указывает на то, что у подмножества пациенток могут быть опухоли с той же метаболической уязвимостью, что и в лаборатории.
Что это может означать для будущих способов лечения
Для неспециалиста ключевая мысль такова: когда раковые опухоли молочной железы эволюционно уходят от воздействия мощных ингибиторов CDK4/6, они одновременно могут загнать себя в метаболический угол. Постоянно включая сигналы роста и отключая клеточную переработку, такие опухоли становятся сильно зависимыми от непрерывного поступления энергии. Исследование показывает, что эту уязвимость можно использовать с помощью метаболических препаратов, таких как метформин и DCA, которые уже хорошо известны при других заболеваниях. Важно, что авторы предлагают простые тканевые тесты на активность mTORC1 и маркеры аутофагии, которые могли бы помочь выявить пациенток, чьи резистентные опухоли подготовлены к такому метаболическому атакующему подходу, открывая путь к более персонализированным «спасательным» лечениям после неудачи ингибиторов CDK4/6.
Цитирование: von Wichert, L., Stroh, A., Witt, M. et al. mTOR-driven autophagy suppression defines metabolic vulnerability in CDK4/6 inhibitor-resistant HR+/HER2− breast cancer. Cell Death Dis 17, 235 (2026). https://doi.org/10.1038/s41419-026-08496-5
Ключевые слова: рак молочной железы, резистентность к ингибиторам CDK4/6, mTOR, аутофагия, метаболическая терапия