Clear Sky Science · ru
Переключение сплайсинга онкогенного изоформы BCS1L подавляет прогрессию рака яичников путем нарушения функции митохондрий
Электростанции внутри раковых клеток
Каждая клетка нашего организма зависит от крошечных электростанций — митохондрий. Раковые клетки, которые быстро растут и метастазируют, особенно нуждаются в энергии. В этом исследовании показано, как рак яичников перенастраивает одного из ключевых митохондриальных помощников, и что аккуратное переключение молекулярного «переключателя» на этом помощнике может лишить опухоли энергии, по большей части не затронув здоровые ткани.
Почему опухоли полагаются на свои «двигатели»
Клетки рака яичников, как и многие другие опухоли, гибко используют разные источники энергии. Просмотрев большие базы данных пациентов и данные одиночных клеток, исследователи обнаружили, что многие опухоли яичников работают на высоких оборотах митохондрий — в режиме окислительного фосфорилирования (OXPHOS). Опухоли с повышенной митохондриальной активностью были более агрессивными и чаще встречались на поздних стадиях болезни. Среди множества белков, собирающих митохондриальную энергетическую систему, выделялся один: BCS1L, шаперон, который помогает собирать Комплекс III — центральный узел в энергетической цепи клетки. В опухолях с высоким OXPHOS и в отдельных подтипах опухолевых клеток активность BCS1L была особенно высокой, что указывает на сильную зависимость раковых клеток от этого помощника для поддержания работы «двигателей».
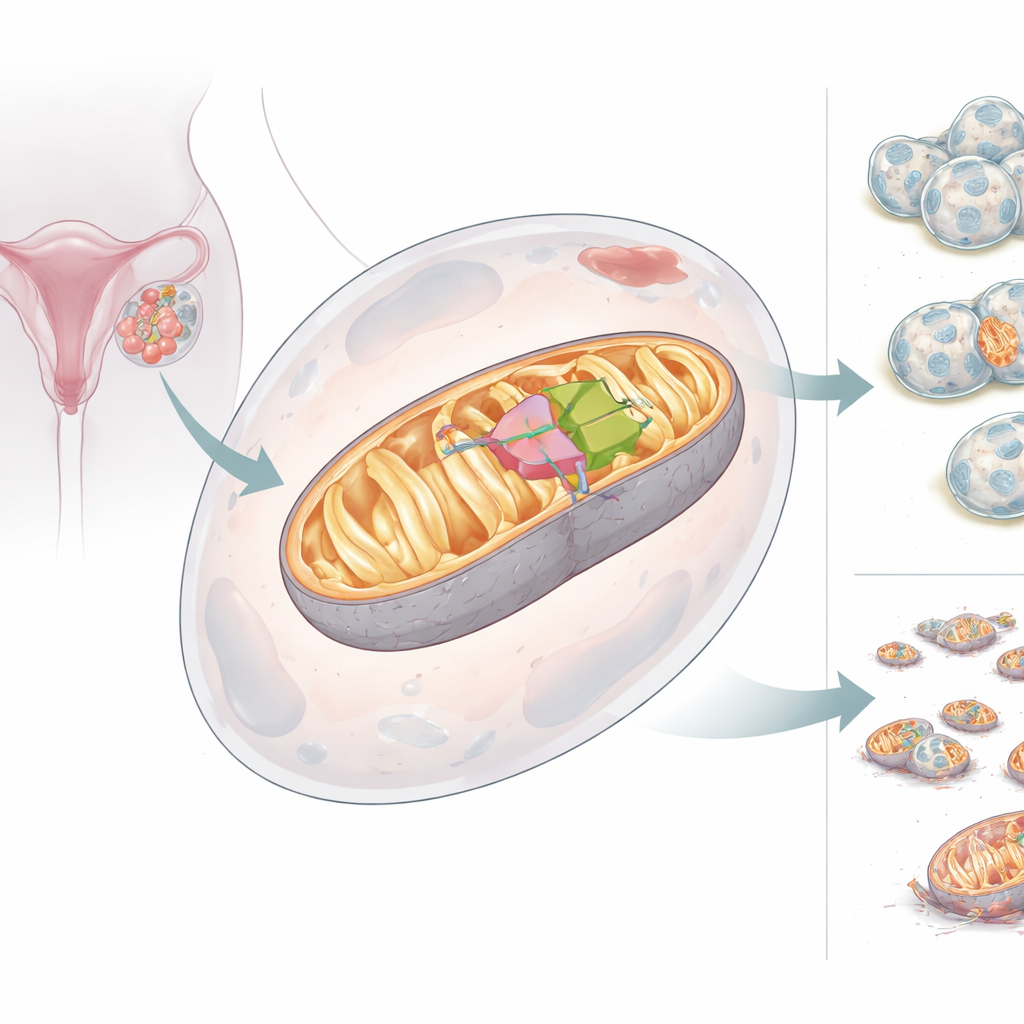
Две стороны митохондриального помощника
Команда обнаружила, что ген BCS1L может давать две версии — изоформы — своего белка. Полноразмерная форма, BCS1L-L, несет встроенный адресный фрагмент, направляющий ее в митохондрии, где она поддерживает правильную сборку Комплекса III и высокую выработку энергии. Более короткая форма, BCS1L-S, лишена ключевого сегмента и не попадает в митохондрии; вместо этого она находится в цитоплазме и ядре клетки и не поддерживает выработку энергии. В здоровых тканях короткая версия распространена, но в раке яичников баланс меняется: доминирует длинная митохондриально-направленная форма. При вынужденной экспрессии BCS1L-L митохондрии клеток вырабатывали больше энергии, поддерживали более высокий мембранный потенциал, производили меньше вредных побочных продуктов кислорода и были более устойчивы к гибели. При снижении уровня BCS1L митохондрии фрагментировались, производство энергии падало, уровень вредных кислородных молекул возрастал, и раковые клетки чаще погибали.
Как рак перенастраивает сообщение
Производство длинной или короткой версии BCS1L зависит от того, как клетка обрабатывает свою РНК — процесса, называемого сплайсингом. Исследователи искали белки, которые связываются с РНК BCS1L и влияют на этот выбор. Они сосредоточились на USP39, факторе сплайсинга, уже связанном с несколькими типами рака. В клетках рака яичников USP39 связывается рядом с сегментом РНК, который становится экзоном 2 BCS1L, и способствует включению этого экзона, тем самым отбирая в пользу длинной, направляемой в митохондрии формы. Когда USP39 выключали, клетки чаще пропускали этот сегмент, смещаясь в сторону короткой формы BCS1L-S. Это ослабляло Комплекс III, снижало митохондриальное дыхание и выработку АТФ, повышало окислительный стресс и вызывало гибель раковых клеток. Восстановление BCS1L-L в этих клетках возвращало большую часть митохондриальной функции и выживания, что демонстрирует: USP39 управляет критическим митохондриальным переключателем во многом через BCS1L.
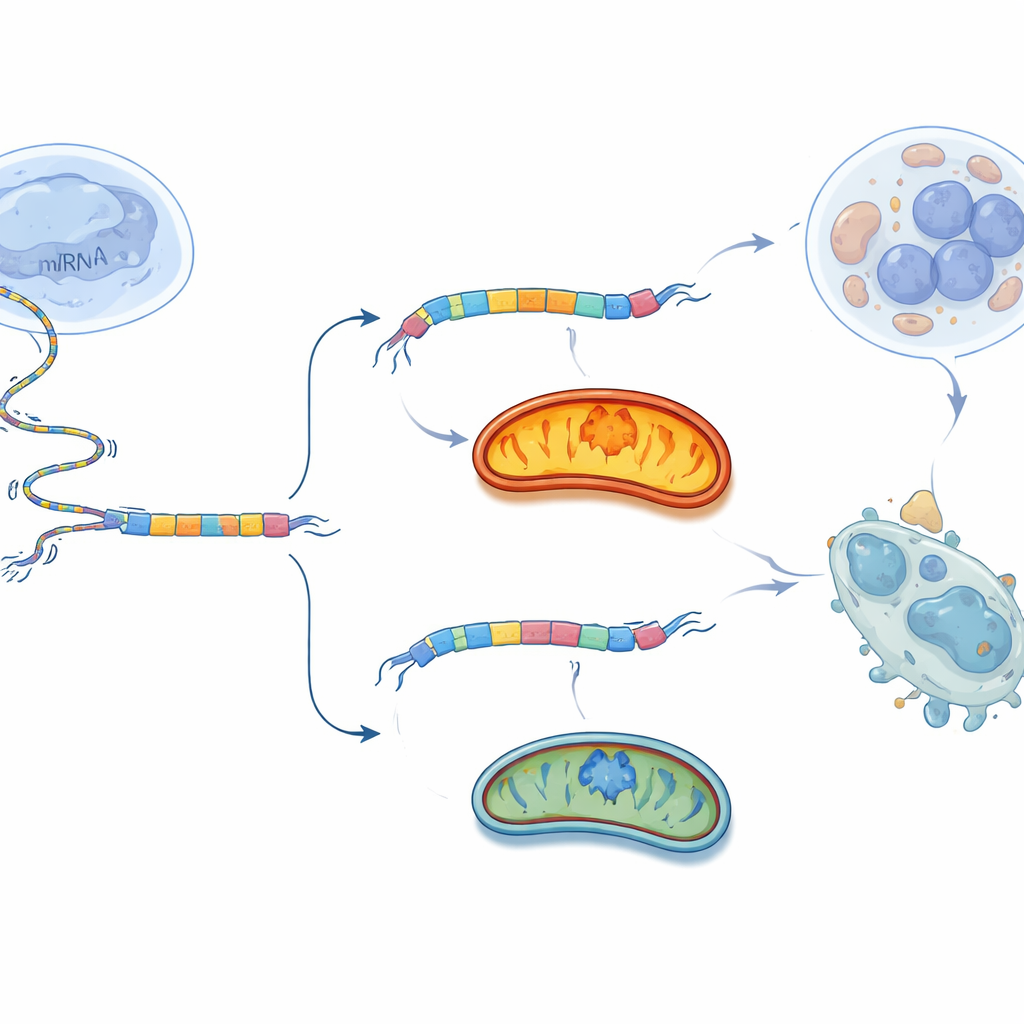
Переключение против опухоли
Вместо того чтобы блокировать митохондрии глобально — что могло бы повредить многие ткани — команда применила более прицельный подход: сместить выбор сплайсинга самого BCS1L. Они спроектировали короткие фрагменты генетического материала — антисмысловые олигонуклеотиды (ASO), которые связываются непосредственно вокруг экзона 2 РНК BCS1L. Эти ASO действуют как крошечные прищепки, меняющие чтение послания сплайсинговым аппаратом и поощряющие пропускание экзона 2. В культивируемых клетках рака яичников лучший ASO существенно уменьшал количество длинной формы BCS1L-L и увеличивал долю короткой BCS1L-S. В результате митохондриальное дыхание и синтез АТФ снижались, уровень вредных форм кислорода возрастал, и значительно больше клеток уходили по пути программируемой гибели. При введении того же ASO в опухоли яичников у мышей рост опухолей замедлялся и их масса уменьшалась, при этом эффект на раковые клетки был заметно сильнее, чем на нормальные фибробласты.
Что это может означать для пациентов
Проще говоря, работа показывает, что многие опухоли яичников зависят от «турбированной» версии митохондриального шаперона для подпитки роста. Фактор сплайсинга USP39 смещает аппаратуру редактирования РНК так, чтобы производилось больше этой турбированной формы, поддерживая митохондрии опухоли в оптимальном состоянии. Используя точно спроектированные ASO для обратного переключения сплайсинга в сторону более слабой формы, исследователи могут избирательно подорвать митохондрии раковых клеток, вызвав их гибель и оставив большинство нормальных клеток относительно невредимыми. Хотя доставка таких ASO в опухоли по‑прежнему остается серьезной проблемой, это исследование указывает на переключатель сплайсинга BCS1L как перспективную и высокоспецифичную мишень для лечения рака яичников.
Цитирование: Xu, M., Wang, Z., Yang, S. et al. Splice-switching of the oncogenic BCS1L isoform suppresses ovarian cancer progression by disrupting mitochondrial function. Cell Death Dis 17, 293 (2026). https://doi.org/10.1038/s41419-026-08495-6
Ключевые слова: рак яичников, митохондрии, сплайсинг РНК, BCS1L, антисмысловые олигонуклеотиды