Clear Sky Science · ru
PGC-1α защищает от MASH посредством Tim23-зависимого подавления DRP1-опосредованной ферроптозы
Почему это важно для повседневного здоровья
У многих людей с ожирением или сахарным диабетом 2-го типа в скрытой форме развивается серьёзная проблема печени — метаболически ассоциированный стеатогепатит (MASH). При этом состоянии клетки печени, насыщенные жиром, воспаляются и начинают гибнуть, что открывает путь к образованию рубцовой ткани, циррозу и раку печени. В этом исследовании обнаружена внутренняя система самозащиты в печёночных клетках — в центре внимания находятся крошечные энергетические центры, митохондрии — которая может либо защищать печень от повреждений, либо, при её срыве, ускорять развитие болезни. Понимание этого внутреннего предохранителя может открыть новые подходы к лечению одной из самых распространённых угроз для печени во всём мире.
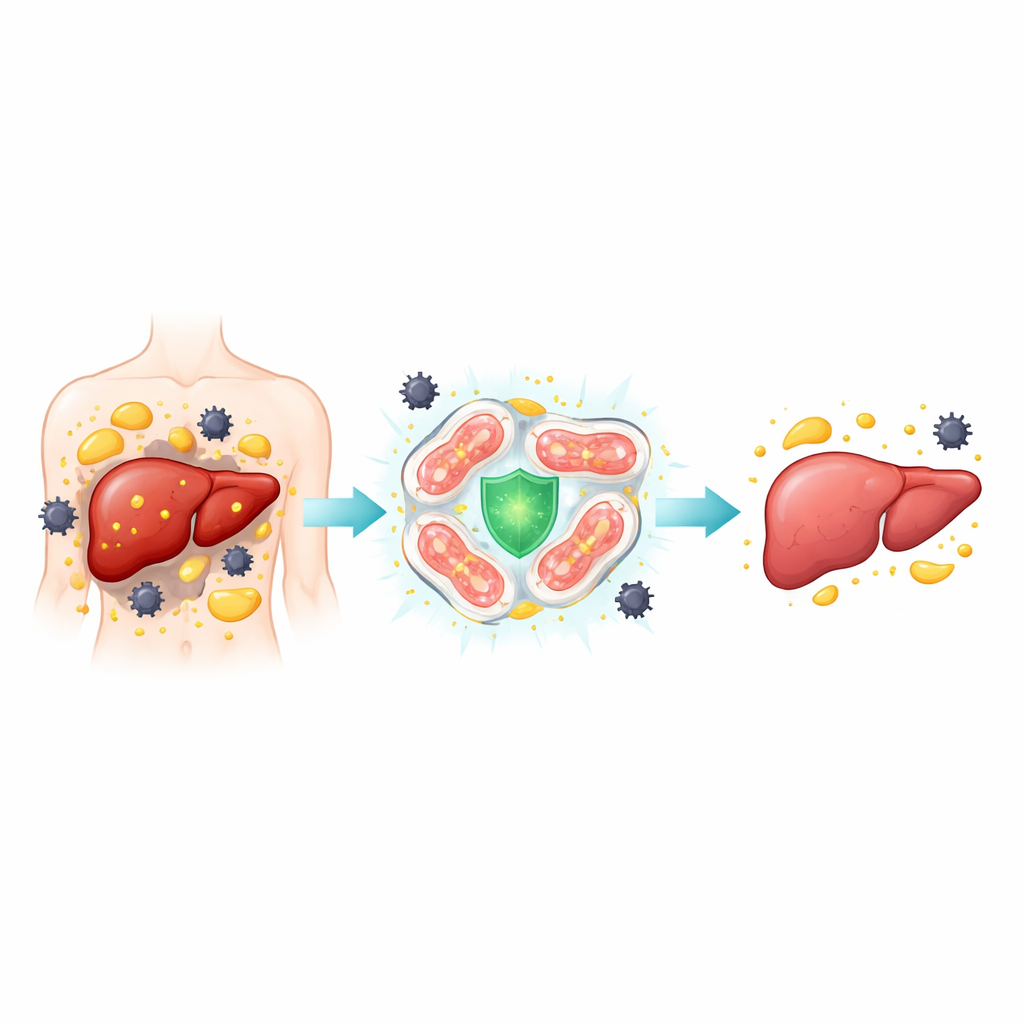
Внимательнее о «тихой» болезни печени
MASH развивается, когда простая жировая печень переходит в более опасное состояние, отмеченное набухшими, повреждёнными печёночными клетками, воспалением и в конечном счёте рубцеванием. Авторы изучали образцы печени пациентов с MASH и образцы из мышиных моделей, которым давали диеты с высоким содержанием жиров, сахара или дефицитными по питательным веществам рационами, имитирующими человеческое состояние. Они сосредоточили внимание на особом виде гибели клеток — ферроптозе, при котором железо и повреждённые липиды взаимодействуют, создавая токсичные молекулы, нарушающие целостность мембран клеток. Как у людей, так и у мышей с MASH печёночные клетки демонстрировали признаки этой железо- и липид-обусловленной гибели: избыток отложений железа, деформированные митохондрии и повышенные уровни белков, способствующих повреждению липидов, наряду с пониженным содержанием белков, которые обычно детоксифицируют вредные побочные продукты.
Доказательства, что блокирование железозависимой гибели помогает
Чтобы проверить, является ли ферроптоз лишь сопутствующим явлением или драйвером болезни, исследователи лечили мышей на высокожировой диете ферростатином-1, соединением, которое специфически блокирует ферроптоз. У мышей, получавших блокатор, наблюдалось меньше накопления жира, меньше перегрузки железом и меньше признаков воспаления и рубцевания в печени. Анализы крови показали улучшение функции печени и общую метаболическую картину: сниженный холестерин и улучшенную чувствительность к инсулину. В изолированных печёночных клетках мышей, подвергнутых воздействию пальмитиновой кислоты — жира, имитирующего перегрузку при MASH — тот же препарат уменьшал накопление жира, загрузку железом, окислительное повреждение и воспалительные сигналы. В совокупности эти результаты свидетельствуют, что ферроптоз является ключевым механизмом повреждения при MASH и что прерывание этого процесса может существенно смягчить течение болезни.
Встроенный страж печени внутри митохондрий
Далее команда сосредоточилась на PGC-1α, ключевом регуляторе, помогающем митохондриям производить энергию и справляться со стрессом. В печени людей с MASH, а также у больных мышей и в стрессированных печёночных клетках уровни PGC-1α были заметно снижены, в то время как белок митохондриального фиссии DRP1 и фермент, активирующий липиды, ACSL4, были повышены. На генетически модифицированных мышах, у которых PGC-1α отсутствовал только в печёночных клетках, авторы показали, что утрата этого «защитника» делает высокожировые диеты значительно более вредными: печень становилась более жировой, более воспалённой, с большей загрузкой железом и с усиленными признаками ферроптоза. На клеточном уровне дефицит PGC-1α усиливал активность DRP1, повышал уровни ACSL4 и белков, импортирующих железо, и ослаблял антиоксидантные механизмы, которые обычно сдерживают ферроптоз.
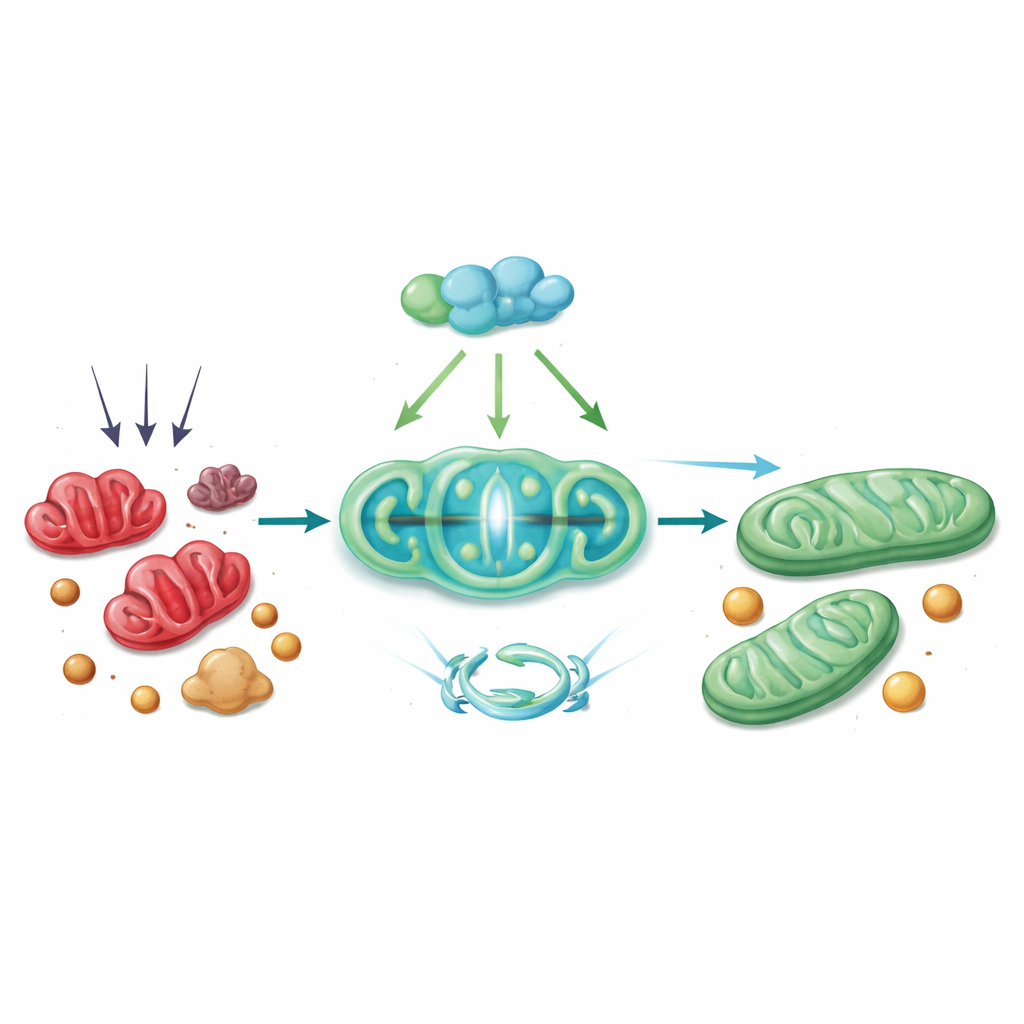
Защитная цепочка реакций внутри клетки
Механистически PGC-1α действует через цепочку взаимодействующих звеньев. Он работает с транскрипционным фактором Nrf1, чтобы увеличить продукцию Tim23 — канала во внутренней митохондриальной мембране, необходимого для импорта белков и поддержания здоровой структуры органеллы. Когда уровни Tim23 падают, нарушается мембранный потенциал митохондрий, что запускает DRP1 и приводит к фрагментации органеллы. Исследование показывает, что при снижении Tim23 DRP1 становится более активным и чаще взаимодействует с ACSL4 на поверхности митохондрий, привлекая этот липид-модифицирующий фермент в митохондрии. Там ACSL4 способствует тем изменениям липидов, которые делают клетки уязвимыми к ферроптозу. Восстановление PGC-1α — либо у мышей с помощью вирусного вектора доставки гена, либо в культивируемых гепатоцитах с помощью активатора на базе CRISPR — обращало многие из этих процессов: уровни Tim23 повышались, активность DRP1 и ACSL4 снижалась, митохондрии выглядели более здоровыми, а маркеры ферроптоза и повреждения печени уменьшались.
Как это открытие может направить будущую терапию
Для неспециалиста главный вывод заключается в том, что печень обладает внутренним «тормозом» против железо- и липид-индуцированной гибели клеток, и что этот тормоз заложен в митохондриях. Цепочка PGC-1α–Tim23–DRP1–ACSL4 функционирует как предохранительная схема: при высоких уровнях PGC-1α Tim23 удерживает митохондрии стабильными, DRP1 и ACSL4 сдержаны, и печёночные клетки менее склонны к самоуничтожению. Когда эта схема даёт сбой, ферроптоз ускоряется и MASH прогрессирует. Идентификация этого пути в образцах человеческой ткани и моделях животных подчёркивает два взаимодополняющих терапевтических подхода для будущего — прямое блокирование ферроптоза и повышение активности PGC-1α или Tim23 для стабилизации митохондрий — что даёт надежду на ранние и более эффективные вмешательства до наступления необратимого рубцевания печени.
Цитирование: Zhao, Y., Zhang, L., Li, B. et al. PGC-1α protects against MASH via Tim23-dependent inhibition of DRP1-mediated ferroptosis. Cell Death Dis 17, 246 (2026). https://doi.org/10.1038/s41419-026-08493-8
Ключевые слова: жировая болезнь печени, митохондрии, гибель клеток, обмен железа, воспаление печени