Clear Sky Science · ru
NSD2 подавляет экспрессию PD-L1 посредством окислительного фосфорилирования, контролируя иммунный надзор при гепатоцеллюлярной карциноме
Почему эта история о раке печени важна
Гепатоцеллюлярная карцинома, самая распространённая форма рака печени, часто диагностируется поздно и устойчива ко многим видам лечения. Иммунотерапевтические препараты, блокирующие «плащ-невидимку» PD-L1 на опухолевых клетках, помогают некоторым пациентам, но не большинству. В этом исследовании выявлен неожиданный участник — белок NSD2, связывающий способ, которым клетки рака печени производят энергию, и их видимость для иммунной системы. Понимание этой связи может указывать на новые подходы к усилению существующих терапий и на способы определить, какие пациенты с наибольшей вероятностью получат от них выгоду.
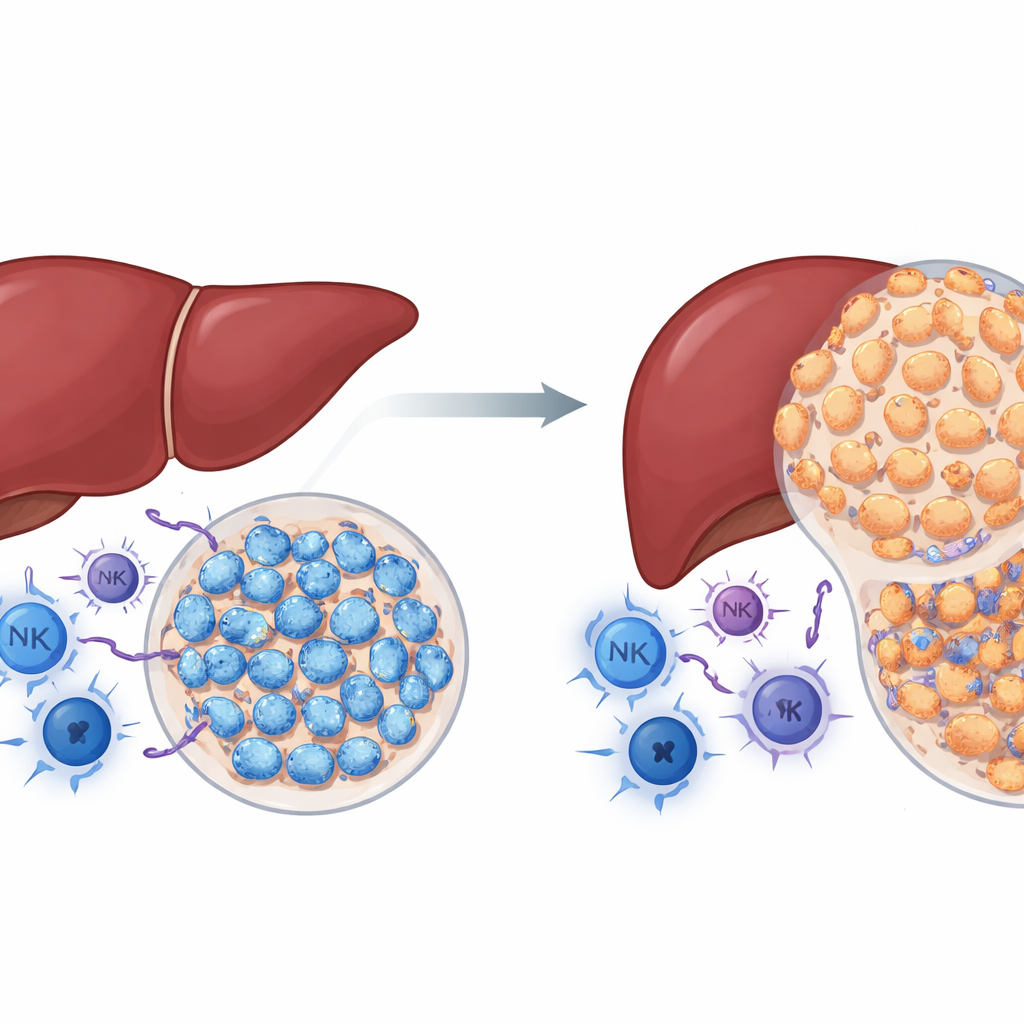
Неожиданная роль знакомого онкологического белка
NSD2 — фермент, модифицирующий гистоны, белки, вокруг которых упакована ДНК. Во многих типах рака NSD2 рассматривали как фактор, стимулирующий рост опухоли. Авторы поставили вопрос, распространяется ли это и на рак печени. Используя генетически модифицированных мышей, в которых NSD2 включён специально в печёночных клетках, они обработали животных химическим веществом, надёжно индуцирующим печёночные опухоли. Вопреки ожиданиям, у мышей с повышенным уровнем NSD2 развивалось значительно меньше и меньшего размера опухолей, чем у нормальных животных; их печень также демонстрировала меньше повреждений, рубцевания и клеточной пролиферации. При этом опухоли из печёнок с сверхэкспрессией NSD2 содержали больше противоопухолевых иммунных клеток, включая хелперные и цитотоксические Т‑лимфоциты, а также натуральные киллеры. Эти результаты говорят о том, что при наличии неизменённой иммунной системы NSD2 ведёт себя скорее как тормоз, а не как ускоритель рака печени.
Энергетические фабрики и использование топлива в опухолевых клетках
Чтобы понять, как NSD2 сдерживает опухоль, команда проанализировала активность генов в печёночной ткани. Они обнаружили, что сверхэкспрессия NSD2 значительно подавляет гены, связанные с окислительным фосфорилированием — процессом, при котором митохондрии, «электростанции» клетки, вырабатывают энергию с использованием кислорода. Последующие эксперименты на клеточных линиях рака печени мыши и человека показали, что повышение NSD2 снижает экспрессию многих генов окислительного фосфорилирования, уменьшает потребление кислорода и производство АТФ, а также снижает потенциал мембраны митохондрий, что является признаком ослабленной митохондриальной активности. Одновременно эти клетки потребляли меньше глюкозы, но не переключались в пользу гликолиза, что указывает на общее снижение энергетического выхода. Потеря NSD2 давала противоположный эффект, усиливая митохондриальную мощность и использование топлива.
Как NSD2 перенастраивает энергетику и иммунную видимость
Углубляясь в механизм, исследователи совместили масштабное картирование хроматина с данными экспрессии генов и выделили набор генов, непосредственно активируемых при наличии NSD2. Два из них, Camk2d и Prkce, известны как тормоза митохондриальной активности. NSD2 усиливал определённую метку на гистонах (H3K36me2) в их промоторах, повышая их экспрессию. Восстановление экспрессии этих генов в клетках рака печени, лишённых NSD2, уменьшало потребление кислорода митохондриями и выработку АТФ, подтверждая, что они служат нисходящими тормозами NSD2 на окислительное фосфорилирование. Важно, что предыдущие работы указывали: высокоактивные митохондрии способствуют повышенному уровню PD-L1 на опухолевых клетках. В согласии с этим авторы обнаружили, что сверхэкспрессия NSD2 снижает уровни PD-L1, тогда как потеря NSD2 повышает PD-L1 в клетках рака печени и в опухолевой ткани.
Ослабление щита и пробуждение иммунной атаки
Функциональные последствия этих молекулярных сдвигов проверяли на мышах, получавших внутрипечёночные инъекции клеток рака, запрограммированных на приобретение или потерю NSD2. Клетки без NSD2 быстро формировали более крупные опухоли, экспрессировали больше PD-L1 и были инфильтрированы меньшим числом Т‑клеток и натуральных киллеров, особенно активированных цитотоксичных Т‑клеток. Когда исследователи химически блокировали митохондриальный комплекс V, ключевой компонент окислительного фосфорилирования, уровни PD-L1 в клетках, лишённых NSD2, снижались к норме, и иммунные клетки лучше индуцировали гибель опухолевых клеток. Аналогично, сверхэкспрессия Camk2d или Prkce в клетках без NSD2, или лечение опухолей антигеном-блокирующим антителом к PD-L1, уменьшали размер опухоли и восстанавливали инфильтрацию иммунных клеток. В данных пациентов низкая экспрессия NSD2 ассоциировалась с худшей выживаемостью, но, что примечательно, с лучшим ответом на терапию, нацеленную на PD-L1, что предполагает возможность использования статуса NSD2 для прогнозирования выгоды от таких препаратов.
Что это значит для будущего лечения рака печени
Для широкого читателя ключевая мысль такова: это исследование переопределяет роль NSD2 как фактора, подавляющего опухолеобразование в раке печени, по крайней мере при наличии работающей иммунной системы. Снижая кислородозависимое энергетическое производство клетки, NSD2 косвенно уменьшает PD-L1 на опухолевых клетках, снимая часть их «плаща-невидимки» и позволяя иммунным клеткам распознавать и атаковать их. Описанная цепочка NSD2–энергетика–PD-L1 предлагает две практические идеи: во‑первых, пациенты с опухолями, лишёнными NSD2, могут быть особенно подходящими кандидатами для препаратов, блокирующих PD-L1; во‑вторых, сочетание препаратов, ингибирующих митохондриальную энергию, с иммунотерапией может дать мощный комбинированный эффект против рака печени.
Цитирование: Zhang, W., Feng, W., Ma, C. et al. NSD2 inhibits the expression of PD-L1 via oxidative phosphorylation to control immune surveillance in hepatocellular carcinoma. Cell Death Dis 17, 284 (2026). https://doi.org/10.1038/s41419-026-08490-x
Ключевые слова: гепатоцеллюлярная карцинома, NSD2, окислительное фосфорилирование, PD-L1, опухолевая иммунотерапия