Clear Sky Science · ru
Регуляция сплайсинга DDX39B опосредованная SNRPD2 способствует прогрессированию рака эндометрия, подавляя активацию криптических экзонов CTSC
Почему скрытые сообщения в генах рака имеют значение
Рак эндометрия — распространённая опухоль матки, заболеваемость которой растёт во всём мире, однако у многих пациентов с распространённым заболеванием по-прежнему мало эффективных вариантов лечения. В этом исследовании показано, как тонкий внутриклеточный процесс — то, как клетки «вырезают» и «склеивают» генетические сообщения — может стимулировать рост и распространение опухолей эндометрия. Выявляя уязвимую «схему проводки», от которой зависят раковые клетки, работа указывает на новые подходы к подавлению опухолей с помощью прецизионных генетических препаратов.
Растущая опухоль, требующая новых ответов
Рак эндометрия сейчас является самой частой гинекологической опухолью во многих западных странах, при этом случаи и число летальных исходов стабильно растут как на Западе, так и в Китае. Применяют операцию, лучевую терапию, химиотерапию, гормональную терапию и иммунотерапию, но ни один из этих методов не идеален. Удаление матки лишает возможности иметь детей, гормональные терапии часто неэффективны, а агрессивные опухоли нередко рецидивируют. Эти трудности побуждают исследователей искать внутри раковых клеток молекулярные слабые места, которые можно было бы адресно нацелить более точными методами лечения.
Аппарат сплайсинга клетки как слабое звено
Для функционирования наши гены сначала переписываются в длинные молекулы РНК, которые затем нужно подрезать и сшивать в процессе, называемом сплайсингом. Специализированные белковые комплексы — сплайсосомы — решают, какие фрагменты сохранять, а какие выбрасывать, фактически редактируя «сценарий», по которому клетки синтезируют белки. Команда сосредоточилась на компоненте сплайсосомы SNRPD2, который относится к семейству «Sm»-белков и участвует в сборке сплайсингового аппарата. Анализируя крупные базы данных по генам и белкам в раке и изучая образцы пациентов, они обнаружили, что уровни SNRPD2 значительно выше в опухолях эндометрия по сравнению с нормальным слизистым слоем матки, а у пациентов с опухолями, содержащими больше SNRPD2, прогноз хуже.
Выключение «главного редактора» замедляет опухоли
Чтобы проверить, является ли SNRPD2 простым свидетелем или активным драйвером, исследователи подавляли его в линиях клеток рака эндометрия, выращиваемых в лаборатории. При выключении SNRPD2 клетки делились медленнее, образовывали меньше колоний и хуже мигрировали и прорастали через мембраны — поведение, связанное с метастазированием. При пересадке таких модифицированных клеток мышам полученные опухоли были существенно меньше и содержали меньше клеток в активной фазе деления. Важно, что команда разработала антисмысловые олигонуклеотиды — короткие синтетические участки ДНК, которые специфически нацелены на РНК SNRPD2. В модели ксенотрансплантата, где фрагменты опухоли человека растут в иммунодефицитных мышах, эти антисмысловые препараты резко снизили уровни SNRPD2 и размер опухоли, что указывает на потенциальную клиническую применимость таргетирования SNRPD2.
Трёхступенчатая цепочка от ошибки сплайсинга к росту рака
Изучая генетические данные, исследователи выяснили, как потеря SNRPD2 перенастраивает РНК-сообщения по всему геному. Они обнаружили, что при снижении SNRPD2 ключевой фермент обработки РНК DDX39B начинает работать с ошибками. Обычно DDX39B помогает удалить конкретный интрон — сегмент РНК, который должен быть вырезан — из собственной матричной РНК. При недостатке SNRPD2 этот интрон остаётся, что создаёт дефектную версию РНК DDX39B, которую клетка быстро разрушает. Пониженный уровень DDX39B затем вызывает эффект домино на другой ген, CTSC, кодирующий фермент-протеазу, известную поддержкой роста и распространения опухоли. В норме скрытый «криптический» экзон внутри РНК CTSC игнорируется, что позволяет синтезировать полноразмерный активный белок CTSC. При дефиците DDX39B этот криптический экзон по ошибке включается, внося преждевременные стоп‑кодоны в РНК. Искажённая РНК CTSC разрушается прежде, чем сможет дать значительный объём белка, и раковые клетки теряют часть своей агрессивности.
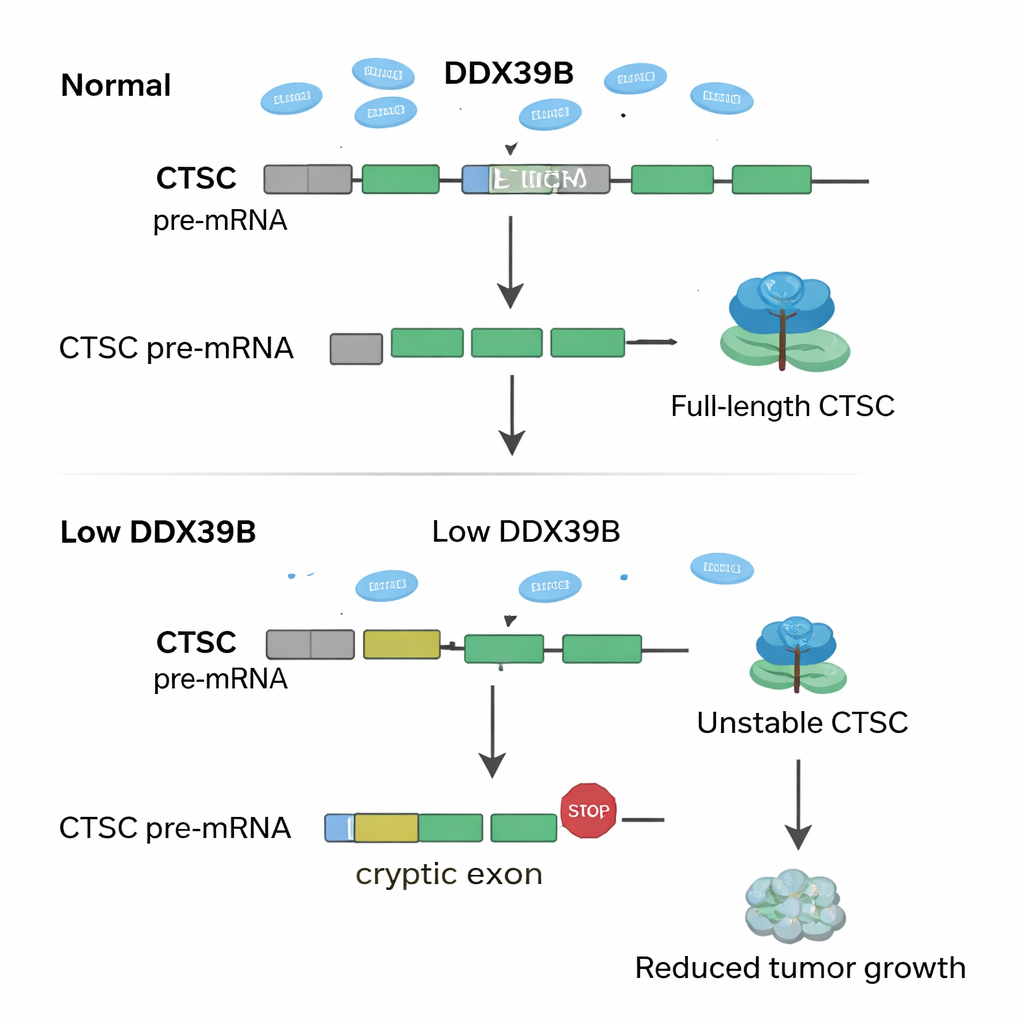
Что это означает для будущих методов лечения
Говоря проще, авторы выявляют релейную систему — SNRPD2 → DDX39B → CTSC — которую раковые клетки эндометрия эксплуатируют для собственного процветания. Высокий SNRPD2 поддерживает уровень DDX39B; DDX39B, в свою очередь, предотвращает использование CTSC повреждающих криптических экзонов, сохраняя полнофункциональный белок CTSC, который помогает опухолям расти и метастазировать. При блокаде SNRPD2 эта цепочка разрушается, уровни CTSC падают, и опухоли ослабевают. Для непрофессионалов ключевая идея в том, что раковые клетки зависят от очень точного редактирования РНК, и даже небольшие намеренные «ошибки» могут избирательно подорвать их рост. Таргетирование SNRPD2 с помощью антисмысловых препаратов или прямое принуждение к использованию криптического экзона в CTSC может предложить новые, более персонализированные терапии для пациентов с раком эндометрия.
Цитирование: Li, Y., Chen, Z., Liu, Y. et al. SNRPD2-mediated regulation of DDX39B splicing promotes endometrial cancer progression by suppressing the activation of CTSC cryptic exons. Cell Death Dis 17, 239 (2026). https://doi.org/10.1038/s41419-026-08489-4
Ключевые слова: рак эндометрия, сплайсинг РНК, SNRPD2, DDX39B, CTSC