Clear Sky Science · ru
DNMT2 тормозит прогрессирование анапластического рака щитовидной железы, понижая образование 5’tiRNAGly-GCC
Почему эта скрытая РНК-химия важна
Анапластический рак щитовидной железы — один из самых смертельных видов рака у людей: пациенты часто умирают в течение нескольких месяцев, несмотря на операцию, лучевую терапию и химиотерапию. В этом исследовании выявлена неожиданная причина, глубоко внутри клеток опухоли: крошечные химические метки на транспортных РНК, молекулах, которые участвуют в построении белков. Авторы показывают, что при утрате или снижении активности определённого фермента DNMT2 опухоли щитовидной железы растут быстрее, легче распространяются и становятся устойчивыми к обычному химиопрепарату доксорубицину. Ещё более интригующе то, что они обнаружили маленький фрагмент РНК, который накапливается при низком уровне DNMT2, и продемонстрировали, что блокирование этого фрагмента может стать новой терапевтической стратегией.
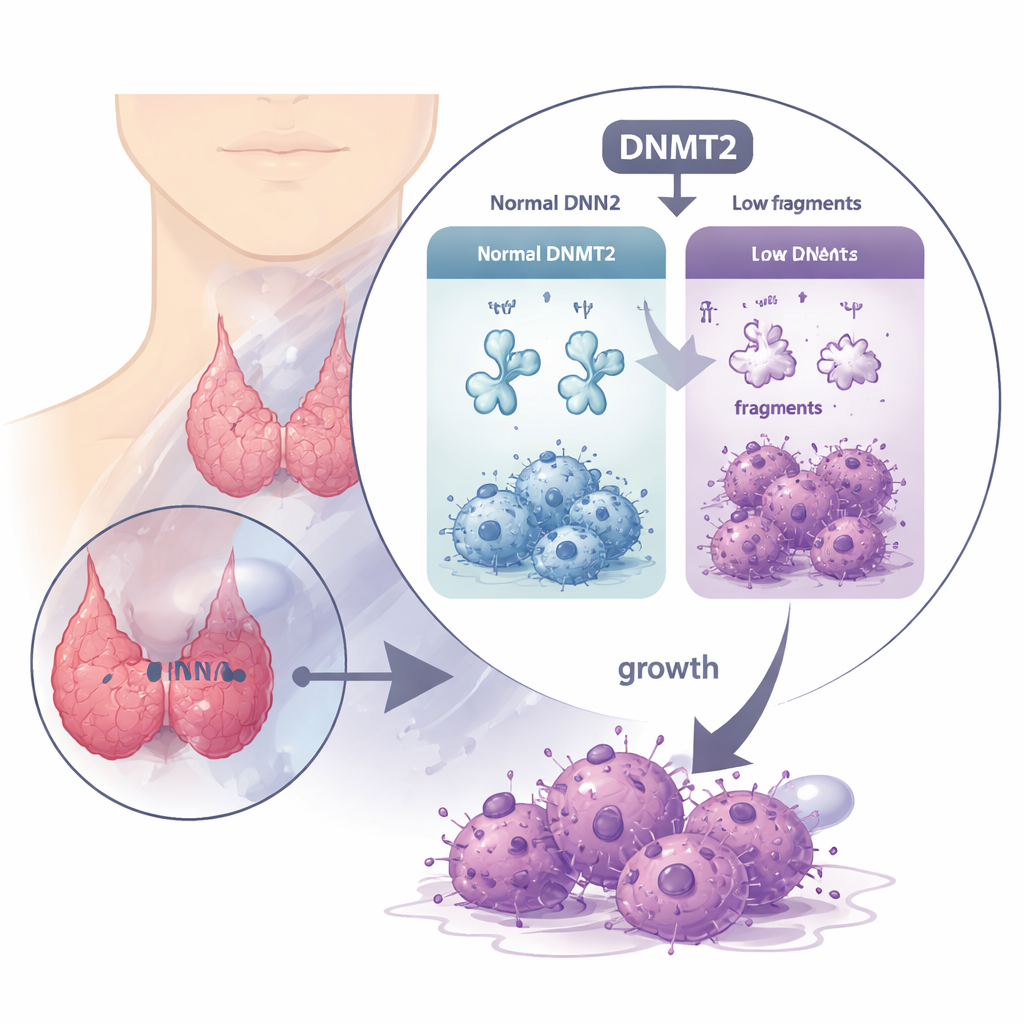
Защитный фермент, который исчезает
Транспортные РНК (тРНК) обычно доставляют аминокислоты к рибосомам, и их стабильность зависит от тонких химических модификаций. DNMT2 — фермент, добавляющий одну такую метку, метильную группу, в определённые позиции тРНК. Во многих типах рака уровень DNMT2 повышен и считается способствующим опухолям, но в данном случае картина обратная. При анализе больших наборов данных пациентов и образцов опухолей исследователи обнаружили, что уровень DNMT2 в тканях анапластического рака щитовидной железы значительно ниже, чем в нормальной щитовидной железе. У пациентов, у которых в опухолях было больше DNMT2, наблюдалась более длительная безпрогредиентная выживаемость, что указывает на то, что в этом заболевании DNMT2 действует скорее как тормоз, чем как акселератор.
Как низкий DNMT2 подпитывает агрессивность
Чтобы понять, что именно делает DNMT2 в раковых клетках, команда варьировала его уровень в линиях клеток анапластического рака щитовидной железы, выращиваемых в культурах, и в моделях на мышах. При снижении DNMT2 клетки делились быстрее, легче прорастали через мембраны и формировали больше колоний — все признаки агрессивной опухоли. Эти клетки также стали менее чувствительны к доксорубицину, стандартному препарату для этого рака. У мышей опухоли с пониженным DNMT2 росли больше и чаще метастазировали в лёгкие, тогда как повышение экспрессии DNMT2 давало обратный эффект. Исследователи отчасти связали эти изменения с активацией программы клеточной пластичности, известной как эпителиально-мезенхимальный переход, которая делает раковые клетки более подвижными и инвазивными.
От повреждённой тРНК до вредных мелких фрагментов
Глубже изучив процесс, авторы показали, что DNMT2 добавляет метильную метку в конкретную позицию (обозначаемую C38) лишь в трёх типах тРНК. Без этой защиты тРНК становятся более уязвимы к разрезанию другим ферментом — ангиогенином. Этот разрез даёт короткий фрагмент РНК, происходящий из тРНК-Gly-GCC, названный 5’tiRNAGly-GCC. С помощью секвенирования и биохимических тестов авторы обнаружили, что при низком уровне DNMT2 этот фрагмент накапливается, особенно из тРНК, несущих глицин. В экспериментах in vitro добавление метильной метки надёжно защищало тРНК от рассечения, подтверждая, что DNMT2 обычно охраняет эти молекулы от разрезания на более мелкие, потенциально вредные кусочки.
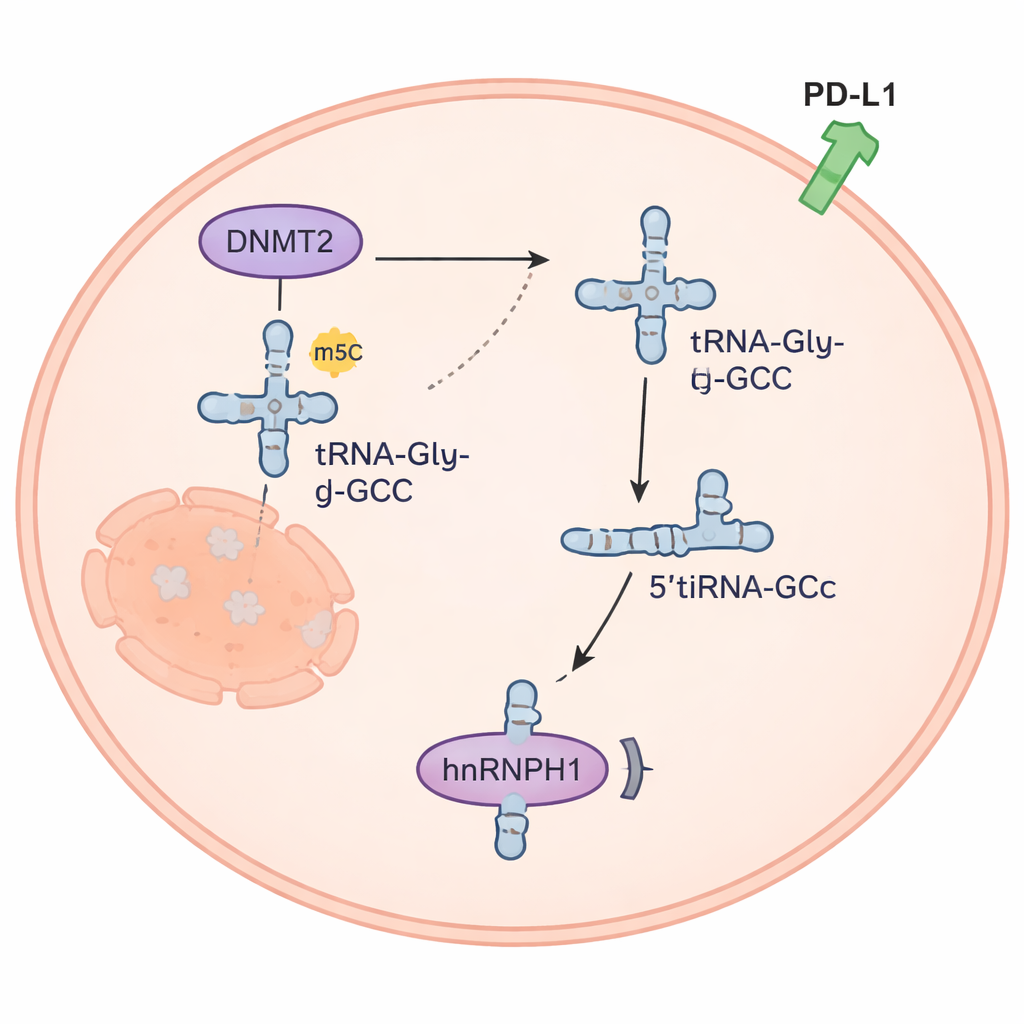
Маленький фрагмент РНК перенастраивает сигналы рака
Фрагмент 5’tiRNAGly-GCC оказался не просто молекулярным мусором. Он был обилен в клетках анапластического рака щитовидной железы и редок в нормальной ткани. Когда исследователи искусственно повышали его уровень, раковые клетки быстрее пролиферировали, становились более инвазивными и более устойчивыми к доксорубицину; снижение уровня фрагмента давало противоположный эффект. У мышей химически разработанный ингибитор 5’tiRNAGly-GCC замедлял рост опухолей, а комбинация этого ингибитора с доксорубицином работала ещё лучше, чем каждое лечение по отдельности. Команда показала, что 5’tiRNAGly-GCC связывается с белком hnRNPH1, уменьшая его количество в клетках. Поскольку hnRNPH1 обычно помогает держать под контролем уровень иммунного белка PD-L1, потеря hnRNPH1 приводит к повышению PD-L1 — изменениям, которые могут помочь опухолям избежать иммунной атаки и связаны с накоплением регуляторных T-клеток вокруг опухолей.
Что это значит для будущего лечения
Проще говоря, исследование выявляет цепную реакцию: при низком DNMT2 некоторые тРНК теряют защитную метку, расщепляются на мелкие фрагменты, и один из этих фрагментов (5’tiRNAGly-GCC) отключает белок, сдерживающий PD-L1. В результате опухоль становится более агрессивной, лекарственно-устойчивой и способной ускользать от иммунитета. Вместо попыток напрямую повышать DNMT2 — что может быть рискованно в других тканях — авторы предлагают нацелиться на вредный РНК-фрагмент. Эксперименты на мышах с ингибитором 5’tiRNAGly-GCC, особенно в сочетании с доксорубицином, дают раннее свидетельство того, что вмешательство в эту микроскопическую РНК-схему может помочь обуздать одну из самых смертоносных форм рака щитовидной железы.
Цитирование: Zhou, R., Li, B., Cao, M. et al. DNMT2 inhibits anaplastic thyroid cancer progression by downregulating 5’tiRNAGly-GCC production. Cell Death Dis 17, 240 (2026). https://doi.org/10.1038/s41419-026-08488-5
Ключевые слова: анапластический рак щитовидной железы, DNMT2, фрагменты тРНК, хеморезистентность, PD-L1