Clear Sky Science · ru
Выявление ZNF124 как нового фактора нейродегенерации: регулирование гомеостаза фоторецепторов через транскрипционный контроль MSX2
Почему это открытие важно для зрения
Ретинит пигментоза является одной из ведущих причин наследственной слепоты, но у почти 40 процентов пациентов врачи по-прежнему не могут точно определить повреждённый ген. В этом исследовании обнаружен новый генетический участник, названный ZNF124, который помогает сохранять жизнеспособность светочувствительных клеток глаза. Показав, как мутация в этом гене нарушает цепочку молекулярных «переключателей» в сетчатке, исследователи открывают новые пути для диагностики и, возможно, таргетной терапии для людей, теряющих зрение.
Скрытая причина наследственной потери зрения
Учёные изучали большую семью, в которой у нескольких детей развились классические признаки ретинита пигментоза: ранняя ночная слепота, сужение бокового поля зрения и постепенная потеря центрального зрения. Детальные офтальмологические обследования выявили истончение сетчатки и слабые электрические ответы на свет — оба признака повреждения палочковых и колбочковых фоторецепторов. Однако ни в одном из более чем 80 известных генов, связанных с ретинитом пигментоза, у этих пациентов не было очевидных дефектов, что указывало на то, что причиной их болезни может быть ещё не описанный ген.
Поиск повреждённого генетического переключателя
С помощью секвенирования всего экзома, которое считывает кодирующие белки участки ДНК, команда выявила редкую, ранее не описанную мутацию в гене ZNF124. Эта мутация изменяет сборку РНК гена, удаляя несколько оснований на критическом стыке. В результате белок ZNF124 обрывается и теряет цинк-пальцевой домен — структуру, которая обычно распознаёт и связывается с конкретными последовательностями ДНК. Поскольку цинк-пальцевые белки часто выступают в роли главных переключателей, включающих или выключающих многие другие гены, повреждённый ZNF124 может оказывать широкое действие в клетках сетчатки.
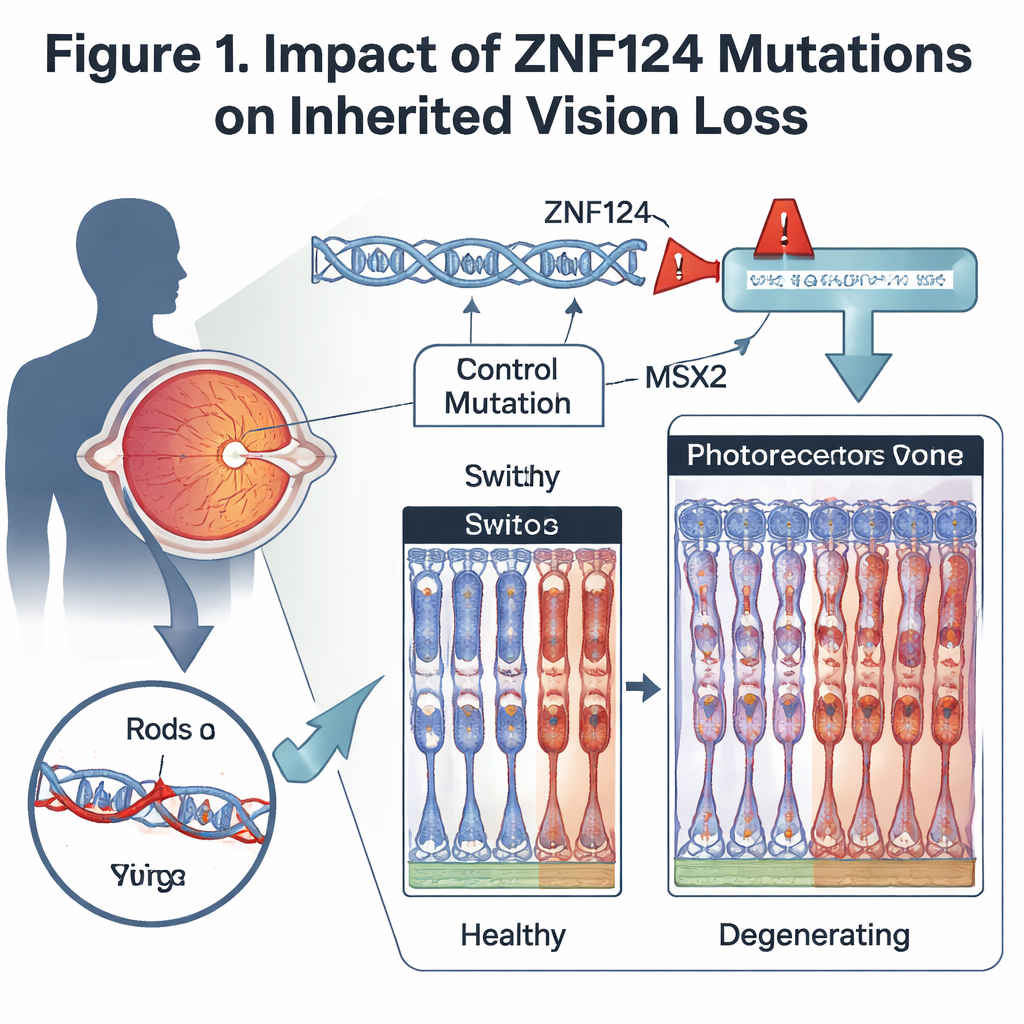
Тестирование гена на модельных животных
Чтобы выяснить, как утрата этого переключателя влияет на глаз, исследователи создали мышей, лишённых Gm20541 — ближайшего мышиного аналога ZNF124 — специально в сетчатке. У этих животных развивались возрастнозависимые проблемы со зрением: их электрические ответы на тусклый и яркий свет ослабевали, а микроскопическое исследование показало прогрессирующее истончение слоя сетчатки, содержащего фоторецепторы. И палочки, которые поддерживают ночное зрение, и колбочки, отвечающие за цветовое и дневное зрение, демонстрировали укороченные внешние сегменты и потерю ключевых визуальных белков. Также сокращалось число некоторых биполярных нейронов сетчатки, а клетки-опорники активировались — типичный ответ на хроническое повреждение сетчатки.
Раскрытие пути контроля ZNF124–MSX2
Следующим вопросом было, какие гены обычно контролирует ZNF124. С помощью биохимических методов, отображающих места связывания белков с ДНК, в сочетании с глобальным анализом РНК из мышиной сетчатки, команда обнаружила, что ZNF124 связывается с геном MSX2 и активирует его. В здоровых клетках ZNF124 прикрепляется к определённой короткой последовательности в регуляторной области «включения» MSX2 и повышает его активность. У мышей без Gm20541 уровень MSX2 падал более чем вдвое. Когда исследователи удалили MSX2 специально в палочках, у этих животных также развивалось истончение слоя фоторецепторов и укорочение внешних сегментов, повторяя дефекты, наблюдавшиеся у мышей с инактивацией аналога ZNF124. Это поместило MSX2 непосредственно ниже ZNF124 в пути, необходимом для выживания фоторецепторов.
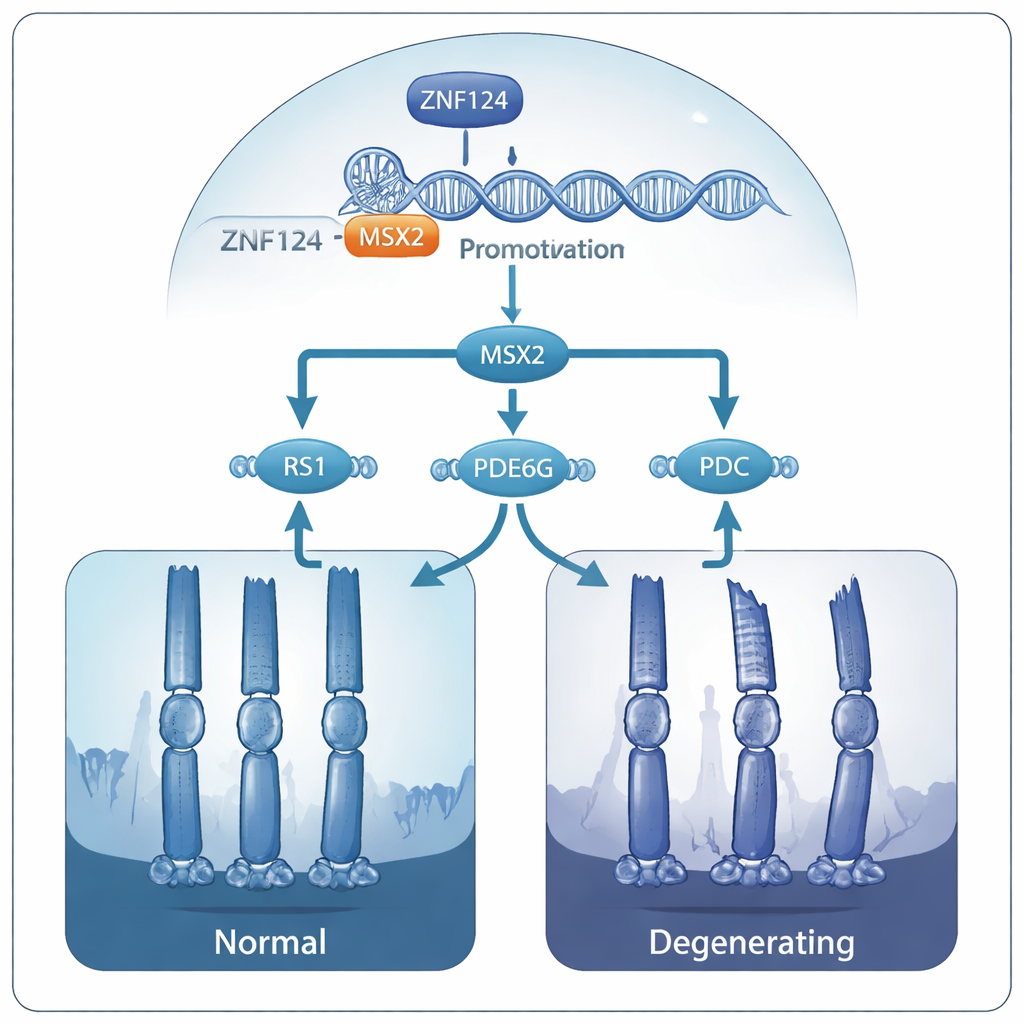
От генетических переключателей к хрупким фоторецепторам
Дальнейший анализ показал, что MSX2, в свою очередь, поддерживает несколько других генов, уже связанных с наследственными заболеваниями сетчатки: RS1, PDE6G и PDC. Эти гены обеспечивают структуру сетчатки и химию визуальной сигнализации. При снижении уровня MSX2 активность всех трёх генов уменьшалась, и их белковые продукты снижались. Авторы предлагают, что у людей с повреждающими мутациями ZNF124 эта вся каскадная цепь ослабляется: ZNF124 больше не может полностью активировать MSX2, MSX2 не поддерживает RS1, PDE6G и PDC, и со временем фоторецепторы теряют структурную целостность и погибают, приводя к прогрессирующей потере зрения.
Что это значит для пациентов и терапий
Для неспециалиста главный вывод заключается в том, что сетчатка зависит от тонко настроенной иерархии генетических переключателей. Эта работа выявляет ZNF124 как новый верхнеуровневый переключатель, отказ которого может вызвать наследственную слепоту через конкретного нижестоящего партнёра MSX2 и его таргетные гены. В клинической практике ZNF124 теперь можно добавить в панели генетического тестирования, что поможет большему числу семей получить точный диагноз. В долгосрочной перспективе терапии, восстанавливающие активность ZNF124, MSX2 или затронутых нижестоящих генов, могут помочь стабилизировать или вернуть светочувствительные клетки, что даёт новую надежду людям с пока не объяснёнными формами ретинита пигментоза.
Цитирование: Yang, Y., Jiang, X., Li, S. et al. Unveiling ZNF124 as a novel determinant in neurodegeneration: orchestration of photoreceptor homeostasis through MSX2 transcriptional regulation. Cell Death Dis 17, 234 (2026). https://doi.org/10.1038/s41419-026-08487-6
Ключевые слова: ретинит пигментоза, фоторецепторы, ZNF124, MSX2, наследственное заболевание сетчатки