Clear Sky Science · ru
Индуцируемая HIF2α лизилоксидаза защищает успешную беременность путем ремоделирования коллагенов на фето-материнском интерфейсе
Почему матка должна подготовиться к новому гостю
Прежде чем беременность сможет установиться, ранний эмбрион обязан совершить нечто поразительное: внедриться в стенку матки и создать систему жизнеобеспечения — плаценту. В этой работе изучается, как ткань матери тихо перестраивается, чтобы принять эмбрион, с акцентом на то, как низкое содержание кислорода и малоизвестный фермент помогают подготовить слизистую оболочку матки. Понимание этой тонко настроенной «хореографии» может прояснить причины ранних неудач беременности и подсказать новые подходы к предотвращению бесплодия и осложнений беременности.
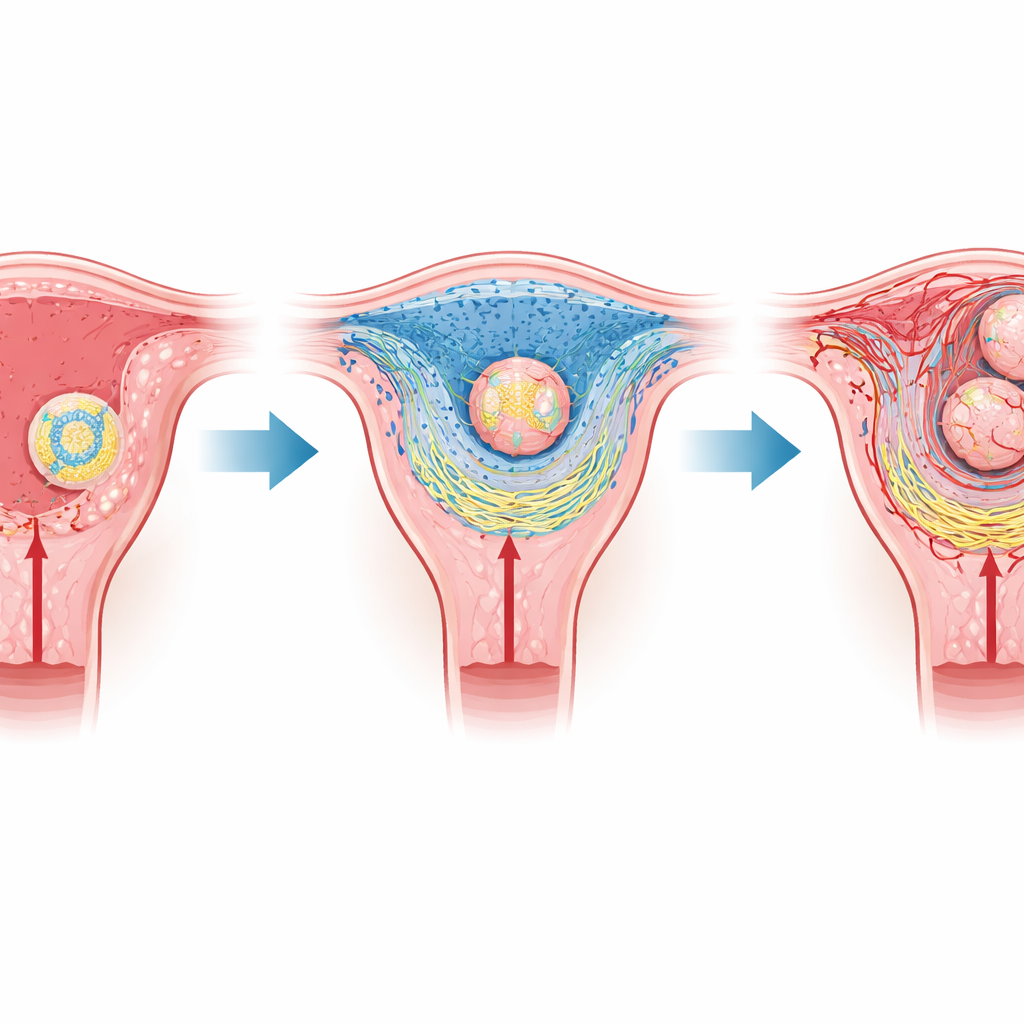
Тонкая встреча матери и эмбриона
У млекопитающих, таких как мыши и люди, ранняя стадия беременности зависит от имплантации, когда эмбрион прикрепляется к слизистой оболочке матки, а затем начинает ее инфильтрировать. Эмбрион окружен оболочкой из специализированных клеток, которые позднее сформируют плаценту, тогда как ткань матери преобразуется в подушкообразный слой, называемый децидуой. Ближе всего к эмбриону располагается тонкая область, известная как первичная децидуальная зона, лишенная кровеносных сосудов и поэтому бедная кислородом. Предыдущие исследования показали, что этот естественно низкий уровень кислорода способствует имплантации, но оставалось неясным, как такое простое физическое условие может перестроить целые ткани.
Низкий уровень кислорода как скрытый переключатель
Авторы использовали мощный метод пространственной транскриптомики, который сопоставляет активность генов непосредственно с участками тканей, чтобы изучить матки мышей в те дни, когда эмбрионы прикрепляются и внедряются. Они сосредоточились на белке HIF2α, который активируется в условиях низкого кислорода и действует как генетический переключатель. У нормальных мышей клетки в первичной децидуальной зоне проявляли высокую активность генов, связанных с гипоксией и построением окружающего каркаса, включая коллагены, формирующие внеклеточный матрикс. Когда HIF2α был удален только в матке, общее распределение типов клеток выглядело удивительно нормально. Но при высоком разрешении сеть коллагенов оказалась дезорганизованной, эпителиальная поверхность не раскрывалась должным образом, и эмбриональные клетки испытывали трудности при проникновении в материнскую ткань.
Фермент, скрепляющий каркас
Глубже в своей работе исследователи выявили ключевого участника, действующего ниже по цепочке от HIF2α: лизилоксидазу, или Lox, фермент, который химически сшивает коллагеновые волокна и помогает укрепить и стабилизировать ткань. В нормальной беременности уровни Lox резко возрастали вокруг эмбрионов как раз тогда, когда они начинали внедряться. В матках без HIF2α экспрессия Lox снижалась, а коллагеновые волокна выглядели фрагментированными вместо плотной сетки. Чтобы прямо проверить роль Lox, исследователи создали мышей, у которых Lox был удален только в матке. Эти самки реже вступали в беременность, несли меньше эмбрионов и часто демонстрировали признаки потери эмбрионов и кровотечений на поздних сроках беременности, хотя первые этапы прикрепления и утолщения ткани первоначально выглядели нормально.
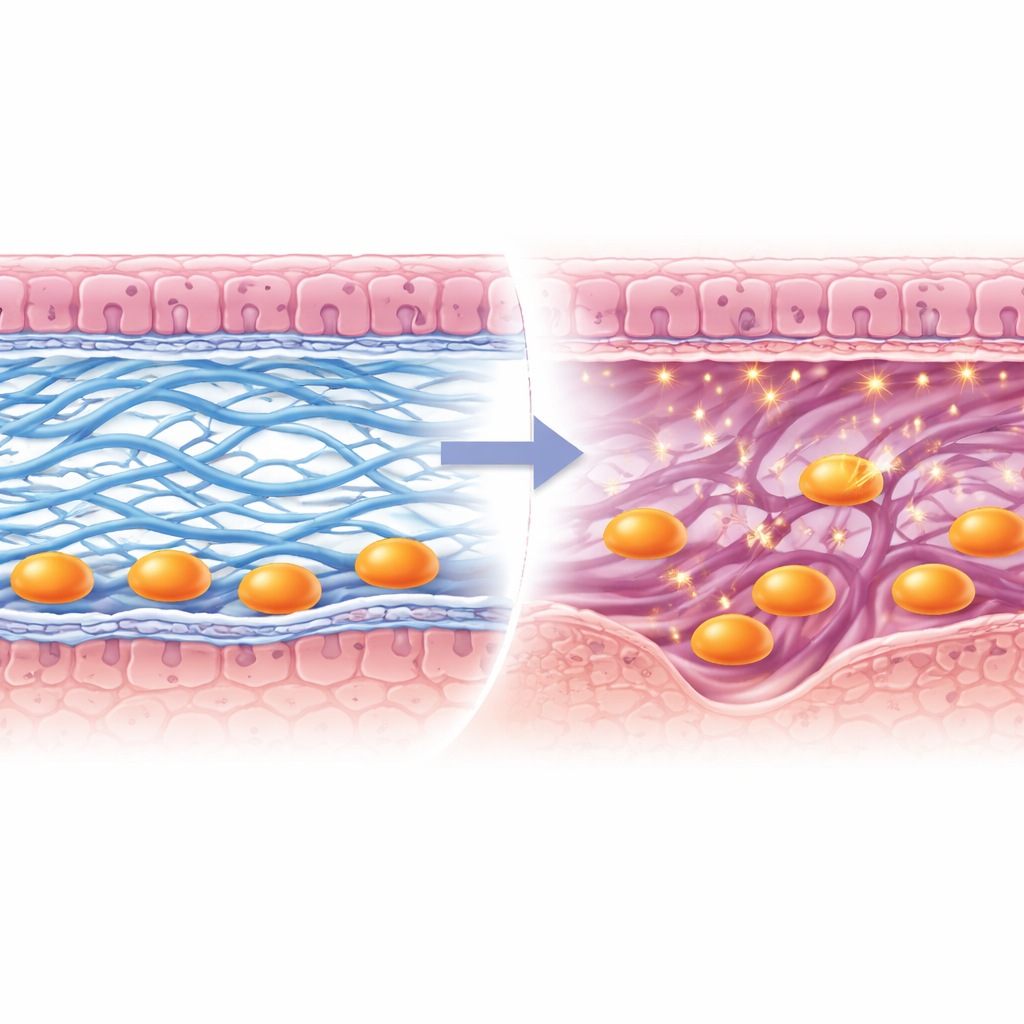
Открывая путь для плаценты
Тщательное визуализирование показало, что именно пошло не так при отсутствии Lox. Тонкая белковая пластинка, называемая базальной мембраной, которая обычно разрушается, чтобы пропустить эмбриональные клетки, оставалась в значительной степени целой. Коллаген I в подлежащей строме не формировал прочных, непрерывных пучков, тогда как коллаген IV в базальной мембране не очищался должным образом вблизи внедряющихся клеток. В результате трофобласты — клетки эмбрионального происхождения, прокладывающие путь и строящие плаценту — оставались запертыми на поверхности вместо того, чтобы продвигаться в материнский слой. Команда также обнаружила, что фермент, расщепляющий коллаген, Mmp9, не активировался в этих трофобластах, что дополнительно мешало их прогрессу. Со временем плацентарные структуры формировались плохо, эмбрионы развивались аномально, и вероятность успешной беременности снижалась.
Что это означает для здоровья беременности
В сумме полученные данные описывают цепочку событий, в которой низкий уровень кислорода в ранней зоне имплантации активирует HIF2α, который, в свою очередь, стимулирует Lox. Lox затем перестраивает и сшивает коллагеновые волокна и способствует разрушению базальной мембраны, а также позволяет таким ферментам, как Mmp9, расчистить путь. Это ремоделирование обеспечивает и структурный каркас, и открытый проход для инвазии трофобластов и строительства плаценты. Для непрофессионального читателя главный вывод в том, что успешная беременность зависит не только от здоровья эмбриона и гормонов, но и от тихой перестройки архитектуры материнской ткани. Нарушения в этой гипоксии–HIF2α–Lox оси могут лежать в основе некоторых случаев необъяснимого бесплодия, выкидышей и расстройств, связанных с недостаточной инвазией плаценты, что может указывать на новые диагностические маркеры и терапевтические мишени для поддержки ранней беременности.
Цитирование: Aikawa, S., Shimizu-Hirota, R., Sakashita, A. et al. HIF2α-induced lysyl oxidase safeguards successful pregnancy by remodelling collagens at the feto-maternal interface. Cell Death Dis 17, 250 (2026). https://doi.org/10.1038/s41419-026-08485-8
Ключевые слова: имплантация эмбриона, внеклеточный матрикс матки, лизилоксидаза, инвазия трофобласта, развитие плаценты