Clear Sky Science · ru
Таргетирование митохондриальной фосфатазы PGAM5 ослабляет ферроптоз и острый панкреатит за счёт повышения экспрессии FSP1, опосредованной NRF2
Почему напряжённые клетки и воспалённая поджелудочная важны
Когда клетки подвергаются чрезмерной нагрузке, они могут умирать так, что это вредит всему организму. Один из таких видов гибели клеток, называемый ферроптозом, запускается ионами железа и неконтролируемыми химическими реакциями, которые «ржавеют» липиды в мембранах клеток. Этот процесс связывают с повреждениями органов, включая болезненное и иногда смертельно опасное состояние — острый панкреатит. Исследование, лежащее в основе этой статьи, выявляет ключевой переключатель в митохондриях — электростанциях клетки — который может усиливать или ослаблять ферроптоз, и показывает, как блокировка этого переключателя защищает поджелудочную железу в мышиной модели.
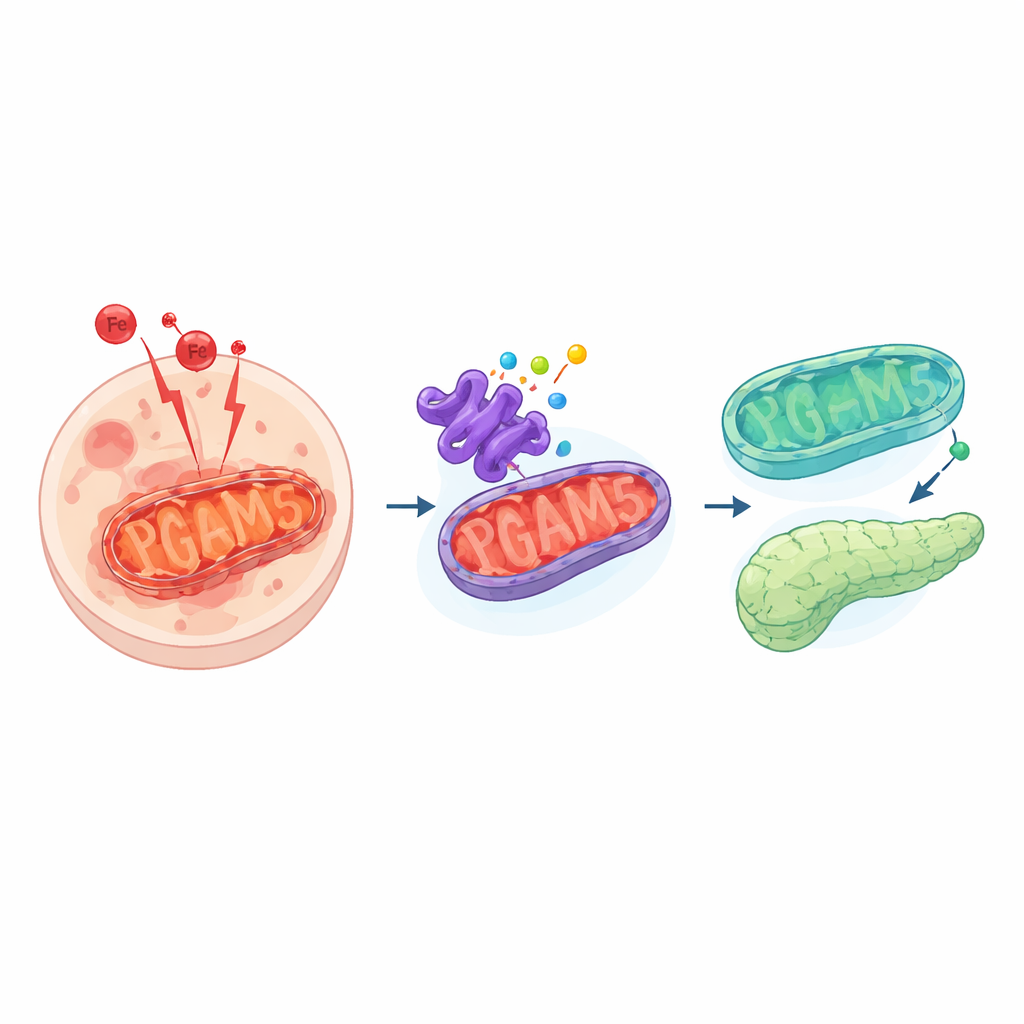
Опасный тип клеточной гибели
Ферроптоз отличается от более привычных форм клеточной гибели, таких как апоптоз. Вместо аккуратного самоуничтожения клетки при ферроптозе переживают бурю реакций, управляемых железом, которые превращают чувствительные липиды мембран в прогоркшие продукты. Это создаёт токсичные побочные продукты и разрывы в мембранах, что в конечном итоге убивает клетку. Обычно клетки сдерживают этот процесс с помощью защитных систем, детоксифицирующих реактивные молекулы. Когда эти системы выходят из строя или перегружены, ферроптоз может распространять повреждения по тканям, вносить вклад в развитие рака и приводить к отказу органов.
Митохондриальный переключатель в прицеле
Исследователи сосредоточились на белке PGAM5, который локализуется на внутренней стороне митохондрий и функционирует как сигнальный узел. PGAM5 участвует в контроле формы митохондрий, реагирует на стресс и влияет на то, как клетки справляются с окислением. Удивительно, но как снижение уровня PGAM5, так и его повышенная экспрессия делали клетки менее уязвимыми к ферроптозу. Химическое ингибирование PGAM5, генетическое подавление экспрессии и моделирование избытка белка ослабляли накопление вредных липидных продуктов и снижали гибель клеток, вызванную веществом-индуктором ферроптоза. Это показало, что система тонко сбалансирована: и дефицит, и избыток PGAM5 переводят клетки в более защищённое состояние.
Включение внутреннего щита
При дальнейшем изучении авторы обнаружили, что влияние PGAM5 реализуется через защитную ось, включающую ещё двух участников: NRF2 и FSP1. NRF2 — мастер-регулятор, который при активации и перемещении в ядро запускает широкий набор антиоксидантных защит. FSP1 — один из его эффекторов, помогающий восстанавливать жирорастворимый антиоксидант и блокировать повреждение липидов на мембране. При изменении уровня PGAM5 клетки увеличивали как транскрипцию, так и содержание белка NRF2, и NRF2 активнее перемещался из цитоплазмы в ядро. Там он увеличивал продукцию FSP1. Блокирование FSP1 или NRF2 устраняло защитный эффект и восстанавливало чувствительность к ферроптозу, что демонстрирует: цепочка PGAM5–NRF2–FSP1 необходима для наблюдаемой устойчивости.
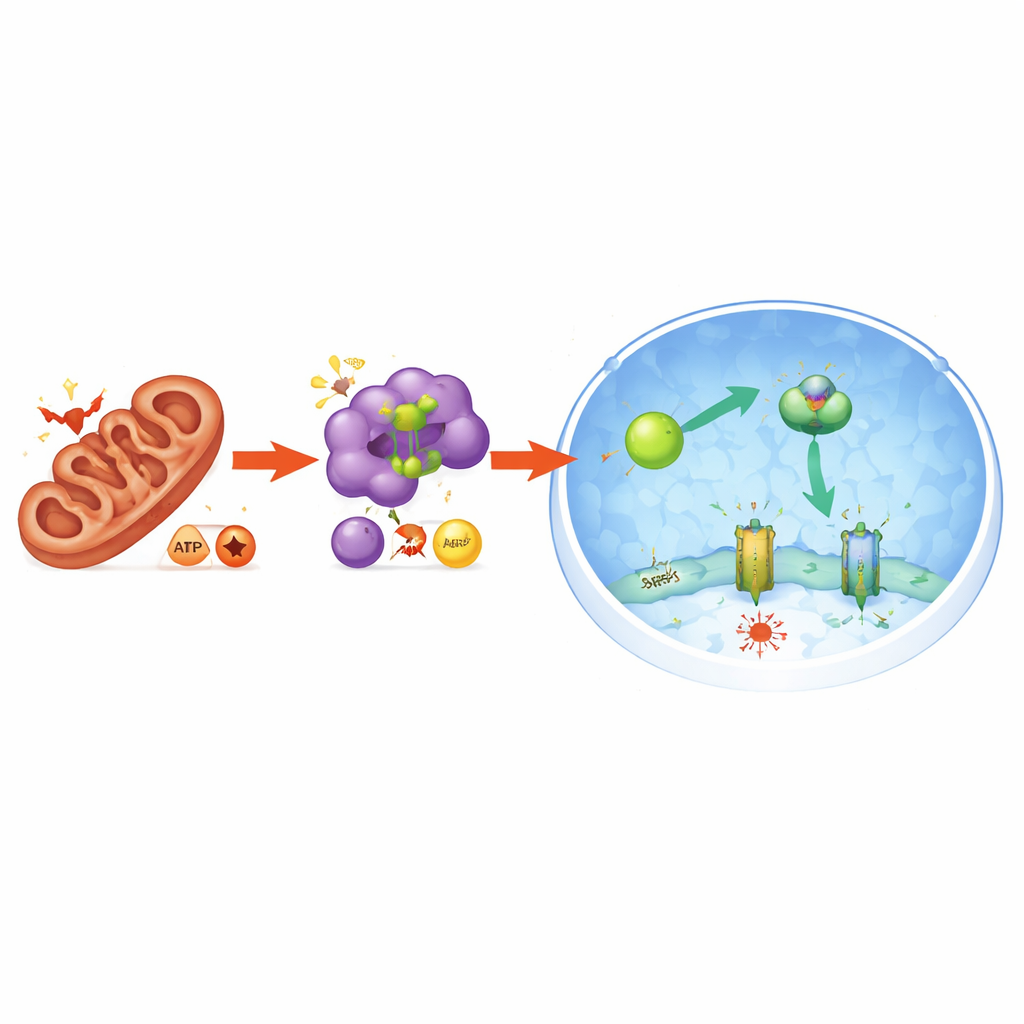
Энергетический стресс как скрытый передатчик
Исследование также показало, как митохондриальный стресс переводится в эту защитную реакцию. Нарушение функции PGAM5 нарушало митохондриальный баланс и изменяло энергетический статус клетки: соотношение низкоэнергетических молекул (AMP и ADP) к высокоэнергетическому ATP повышалось, посылая сигнал об энергетическом стрессе. Это, в свою очередь, активировало энергоощущающий фермент AMPK. Активированный AMPK напрямую модифицировал NRF2 так, что тот легче попадал в ядро и усиливал производство FSP1. При отключении AMPK NRF2 уже не накапливался в ядре, уровень FSP1 падал, и клетки снова становились восприимчивыми к ферроптозу. Таким образом, PGAM5 связывает состояние митохондрий с более широкой энергией — и антиоксидантной — ответной программой, защищающей клетки от железозависимой гибели.
Защита поджелудочной в живом организме
Чтобы проверить значение этого механизма в целом органе, учёные обратились к мышиной модели острого панкреатита, вызванного высокими дозами аминокислоты аргинина. В этой модели поджелудочная демонстрировала обширные повреждения, повышенные уровни ферментов в крови, указывающих на повреждение ткани, и всплеск воспалительных молекул. Маркеры липидной пероксидации — отличительный признак ферроптоза — также резко возросли в поджелудочной. Лечение мышей соединением, ингибирующим PGAM5, смягчало эти симптомы: маркеры повреждения в крови снижались, ткань поджелудочной выглядела более здоровой в микроскопе, а воспалительные сигналы уменьшались. Одновременно маркеры ферроптоза падали, а активность AMPK, уровни NRF2 и FSP1 в поджелудочной возрастали, что соответствовало защитному пути, наблюдаемому в клеточных культурах.
Что это значит для будущих терапий
В совокупности работа выделяет PGAM5 как центральную точку контроля, связывающую митохондриальный стресс, энергетический статус клетки и мощную антиоксидантную программу, блокирующую ферроптоз. При снижении активности PGAM5 активируются AMPK и NRF2, повышается FSP1, и клетки лучше противостоят железозависимому повреждению липидов. У мышей такая стратегия уменьшает повреждение поджелудочной при остром панкреатите. Для неспециалиста это означает, что учёные обнаружили новый внутренний «автомат защиты», который может предотвратить разрушительную форму клеточной гибели. Хотя до клинического применения ещё далеко, таргетирование PGAM5 или его внизпо течений может открыть новые пути лечения состояний, где ферроптоз и митохондриальная дисфункция играют вредную роль.
Цитирование: Ma, S., Qin, J., Luan, J. et al. Targeting mitochondrial phosphatase PGAM5 alleviates ferroptosis and acute pancreatitis by upregulating NRF2-mediated FSP1 expression. Cell Death Dis 17, 252 (2026). https://doi.org/10.1038/s41419-026-08484-9
Ключевые слова: ферроптоз, митохондрии, острый панкреатит, окислительный стресс, клеточная смерть