Clear Sky Science · ru
Малое молекулярное ингибитор белка ARF GTPase 1 ограничивает рост и метастазирование клеток рака печени и толстой кишки
Почему это исследование важно
Рак печени и толстой кишки — одни из самых смертельных опухолей, а существующие методы лечения часто уменьшают опухоли ценой тяжёлых побочных эффектов. В этом исследовании изучается новый тип препарата, который не просто отравляет быстро делящиеся клетки, а проникает внутрь раковых клеток и разъединяет белковый «узел управления», от которого они зависят для роста и распространения. Нацеливаясь на этот узел, экспериментальное соединение стремится замедлить рост опухоли при меньшем вреде для здоровых тканей.
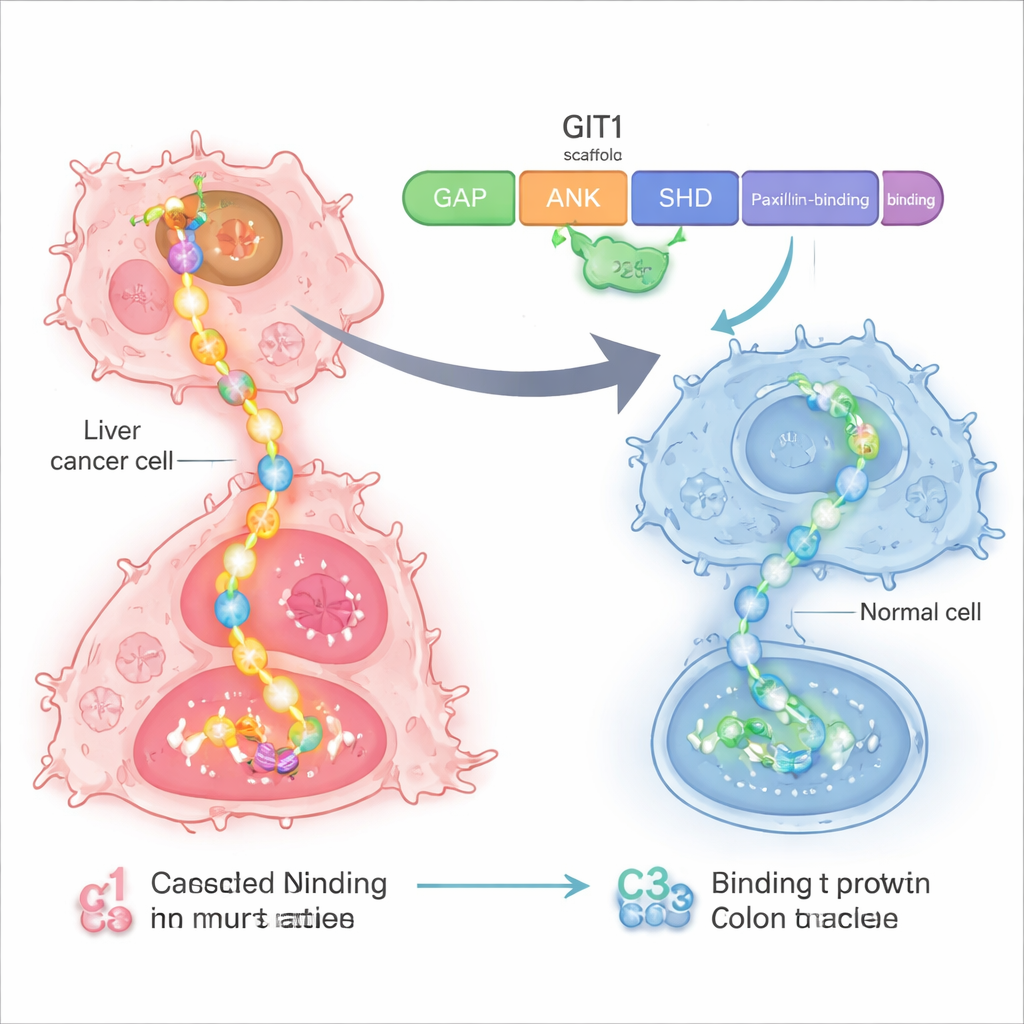
Уязвимый узел управления внутри раковых клеток
Исследователи сосредоточились на белке под названием GIT1, который действует как каркас или распределительная планка внутри клетки. При раке печени и толстой кишки GIT1 и его партнёр MAT2B перепроизводятся. Вместе они собирают несколько компонентов крупного сигнального пути роста, известного как RAS–RAF–MEK–ERK — цепочки сигналов, побуждающей клетки делиться и мигрировать. Ранние работы показали, что при избытке GIT1 и MAT2B опухоли печени и толстой кишки растут быстрее и легче дают метастазы, тогда как при уменьшении этих белков рост рака замедляется. Это сделало каркас GIT1–MAT2B привлекательной мишенью для более точной терапии.
Проектирование малой молекулы без чертежа
Ключевой проблемой было то, что трёхмерная кристаллическая структура GIT1 недоступна, поэтому команда не могла просто «посмотреть» на форму белка. Вместо этого они использовали компьютерное моделирование, чтобы предсказать структуру одной области GIT1, состоящей из анкириновых повторов, расположенной рядом с местами связывания MAT2B и других сигнальных белков. Затем они виртуально просеяли большую библиотеку малых молекул против этой модели, чтобы выяснить, какие из них могли бы связаться с этой областью. Из девяти кандидатов, протестированных в клетках, выделилась одна молекула — соединение 3 (C3). C3 специфически связывался с GIT1, но не с его близким родственником GIT2, и снижал активность сигнала роста ERK в нескольких линиях раковых клеток.
Остановка деления и распространения раковых клеток
При обработке клеток рака печени и толстой кишки C3 замедлял их рост, а при более высоких дозах многие клетки умирали, в то время как незлокачественные печёночные и почечные клетки в основном оставались невредимыми. C3 вызывал остановку клеток на границе фаз G2 и M клеточного цикла — контрольной точки перед митозом и во время него, когда клетка делится на две. Соединение также резко снижало способность раковых клеток образовывать колонии и мигрировать по поверхности чашки — два лабораторных показателя, связанных с регенерацией опухоли и метастазированием. На молекулярном уровне C3 ослаблял взаимодействия между GIT1, MAT2B и сигнальными белками RAF–MEK–ERK, что приводило к снижению активности MEK и ERK и уменьшению уровня циклина D1, драйвера клеточного цикла.
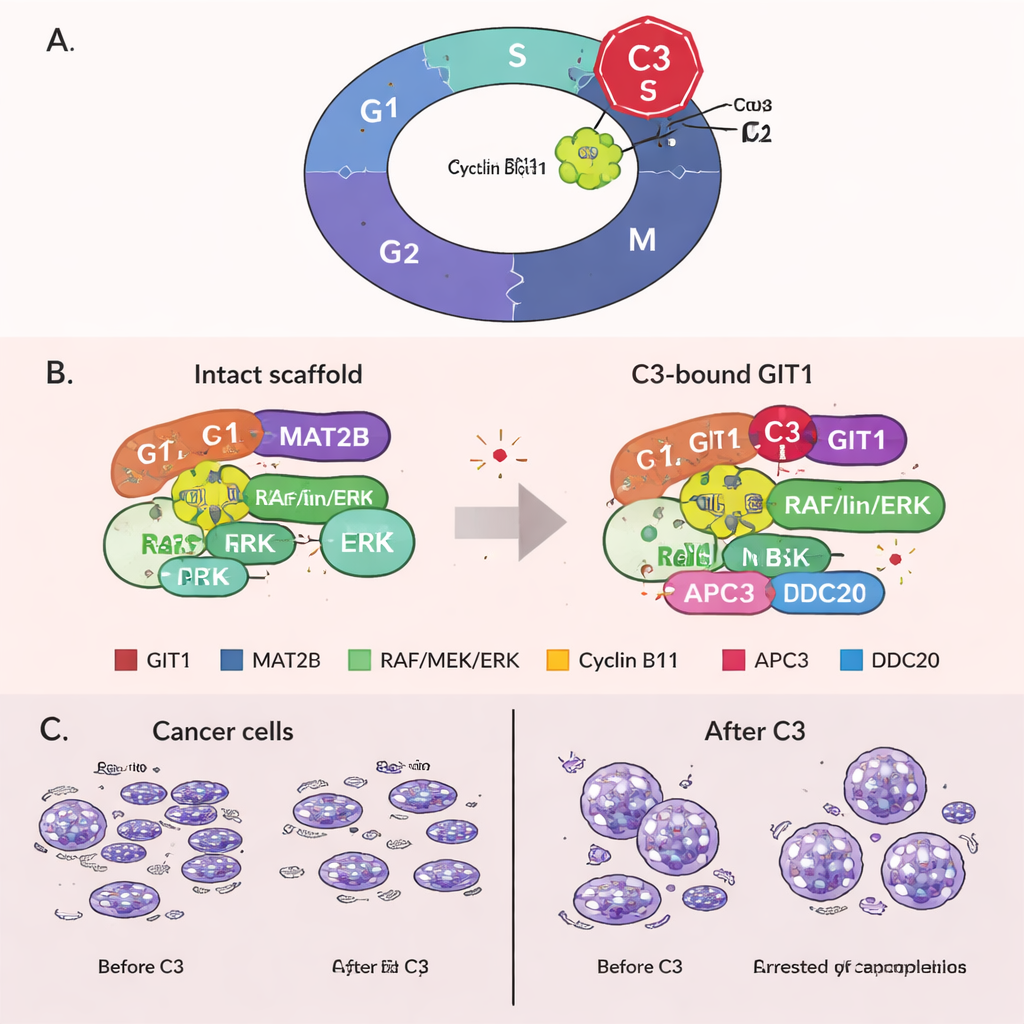
Фиксация клеток в митозе через недавно обнаруженную роль GIT1
Неожиданно команда обнаружила новую функцию GIT1 на заключительных этапах деления клетки. Они выяснили, что GIT1 связывается с циклином B1 — белком, способствующим входу клеток в митоз, — а также с частями белкового комплекса, называемого анафаз-промоутирующим комплексом (APC/C), который обычно помечает циклин B1 для разрушения, чтобы клетки могли выйти из митоза. Лечение C3 усиливало связь между GIT1 и циклином B1, но ослабляло связи между GIT1, циклином B1 и компонентами APC/C. В результате циклин B1 переставал эффективно разрушаться, его уровень оставался высоким, и клетки застревали в митозе. Эта продолжительная остановка известна тем, что запускает клеточную гибель, предоставляя второй путь, с помощью которого C3 может убивать раковые клетки. Важно, что при экспериментальном снижении уровня GIT1 C3 потерял большую часть своей способности повышать уровень циклина B1, блокировать клеточный цикл и подавлять рост, что показывает, что эффекты действительно зависят от GIT1.
Многообещающие результаты на животных моделях
Затем исследователи перешли к мышиным моделям, чтобы проверить, работает ли C3 в живом организме. У иммунокомпетентных мышей с имплантированными колоректальными опухолями инъекции C3 непосредственно в опухоль резко замедляли её рост без очевидной токсичности для основных органов. В двух дополнительных моделях — человеческие клетки рака толстой кишки, растущие в печени иммунодефицитных мышей, и мышиные клетки рака толстой кишки, распространившиеся в печень у иммунокомпетентных мышей — введение C3 внутрибрюшинно снижало опухолевую нагрузку и признаки метастазирования. Анализы крови и исследования тканей показали хорошую переносимость лечения, а фармакокинетические исследования продемонстрировали, что уровни препарата в крови оставались достаточно высокими в течение нескольких часов после дозирования.
Что это может означать для будущих методов лечения рака
Для неспециалиста ключевая мысль в том, что исследователи нашли способ атаковать рак не путём ориентирования на один мутированный фермент, а нарушая много компонентную сборку белков, от которой раковые клетки зависят как для сигналов роста, так и для корректного деления. Их малая молекула C3 специфически связывается с GIT1, перестраивает его сеть партнёров, ослабляет крупный путь роста и запирает раковые клетки в фатальной «пробке» во время митоза. Хотя C3 пока остаётся экспериментальным инструментом, а не лекарством для пациентов, работа демонстрирует, что нацеливание на каркасные белки, такие как GIT1, может открыть новую дорогу в лечении рака печени и толстой кишки с большей точностью и, возможно, с меньшими побочными эффектами.
Цитирование: Peng, H., Chhimwal, J., Fan, W. et al. A small molecule inhibitor of ARF GTPase protein 1 limits liver and colon cancer cell growth and metastasis. Cell Death Dis 17, 238 (2026). https://doi.org/10.1038/s41419-026-08477-8
Ключевые слова: рак печени, рак толстой кишки, таргетная терапия, арест клеточного цикла, каркасный белок