Clear Sky Science · ru
Варианты с потерей функции в HPDL нарушают развитие коры человека через изменения функции митохондрий
Почему крошечные «электростанции» клеток важны для растущего мозга
Большинство людей при мысли о развитии мозга представляет генетику и нейронную проводку. Это исследование показывает, что ещё один, часто недооцениваемый фактор — маленькие электростанции внутри наших клеток, митохондрии — тоже может формировать рост мозга. Изучая редкие детские двигательные расстройства, связанные с геном HPDL, авторы показывают, как дефекты производства энергии могут приводить к уменьшению развивающейся коры — области мозга, важной для движения, мышления и поведения.
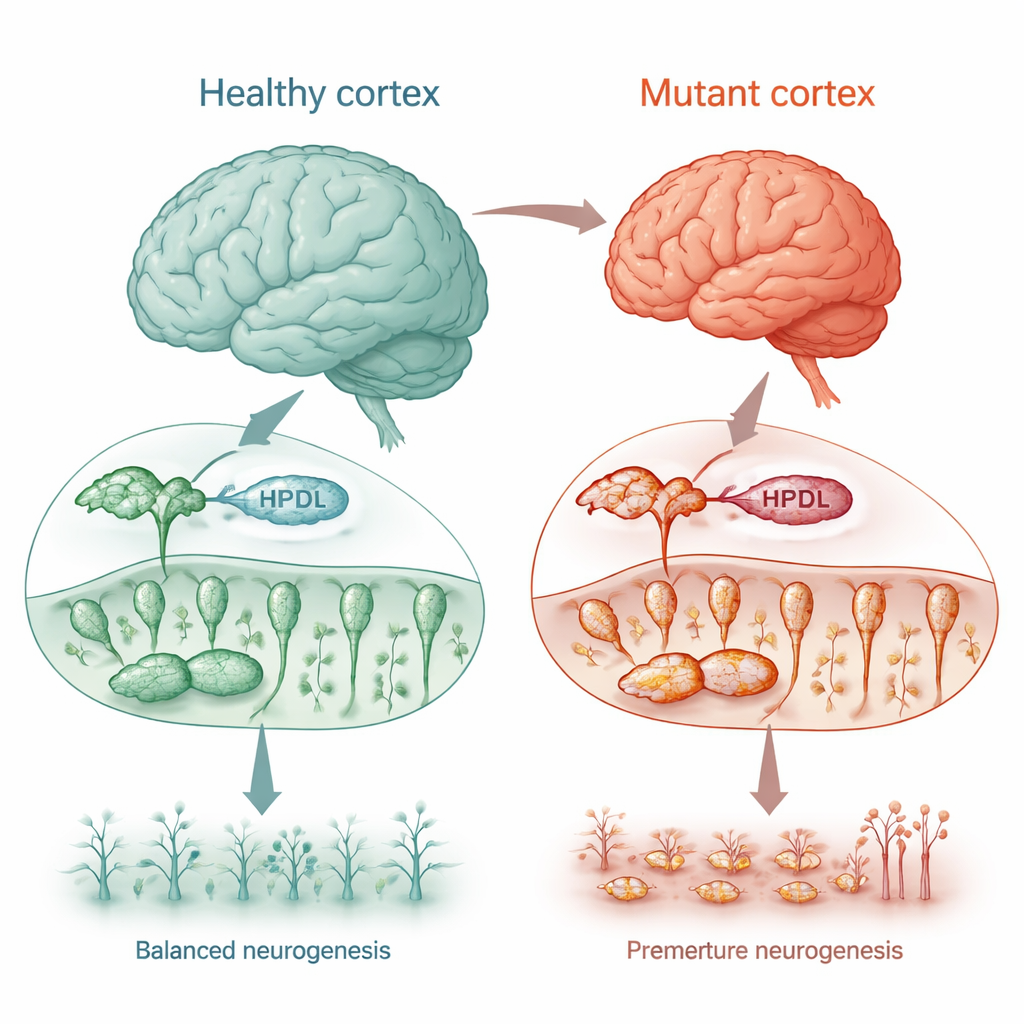
Редкое двигательное расстройство как окно в рост мозга
У некоторых детей с изменениями в гене HPDL развивается наследственная спастическая параплегия — состояние, вызывающее скованность и слабость в ногах, а также судороги, задержку развития и в тяжёлых случаях уменьшенный мозг (микроцефалия). Хотя было известно, что белок HPDL локализуется в митохондриях, его точная роль и причина, по которой его утрата повреждает мозг, оставались неясными. Исследователи использовали несколько моделей человеческих клеток, включая нейропластические клеточные линии и клетки мозга, выращенные из кожных образцов пациентов, чтобы проверить, необходим ли HPDL для нормального развития мозга и здоровья митохондрий.
Что происходит, когда HPDL отключают
Сначала команда выключила HPDL в линии человеческой нейробластомы с помощью редактирования CRISPR. Без HPDL в этих клетках исчез полноразмерный белок и возникли явные митохондриальные нарушения. Крупные комплексы белков дыхательной цепи, которые обычно работают вместе для выработки энергии, были нарушены, а ключевые компоненты, участвующие в использовании кислорода, оказались сокращены. Клетки потребляли меньше кислорода, производили меньше энергосвязанной респирации и генерировали больше реактивных форм кислорода — вредных побочных продуктов, часто называемых «окислительным стрессом». В то же время общее число митохондрий не уменьшилось, а уровни коэнзима Q10, важной молекулы для переноса энергии, были даже выше, что указывает на качественный, а не только количественный дефект функции митохондрий.
Ткань мозга в чашке показывает раннее перепроизводство нейронов
Чтобы увидеть, как утрата HPDL влияет на реальное развитие человеческого мозга, исследователи перепрограммировали кожные клетки четырёх заболевших детей в индуцированные плюрипотентные стволовые клетки, а затем направили их в формирование корковых клеток и трёхмерных «мини-мозгов» (органоидов). Рано на стадии развития, когда большинство клеток ещё должно делиться как нейральные прогениторы, культуры с мутациями HPDL уже содержали больше зрелых нейронов и меньше прогениторов. Профили активности генов подтверждали это: пути, стимулирующие образование нейронов, включались преждевременно, тогда как те, что поддерживают деление клеток, были подавлены. В органоидах этот преждевременный переход от строительных блоков к готовым нейронам привёл к гораздо меньшим структурам, напоминающим мозг, что отзывается микроцефалией у самых тяжёлых детей.
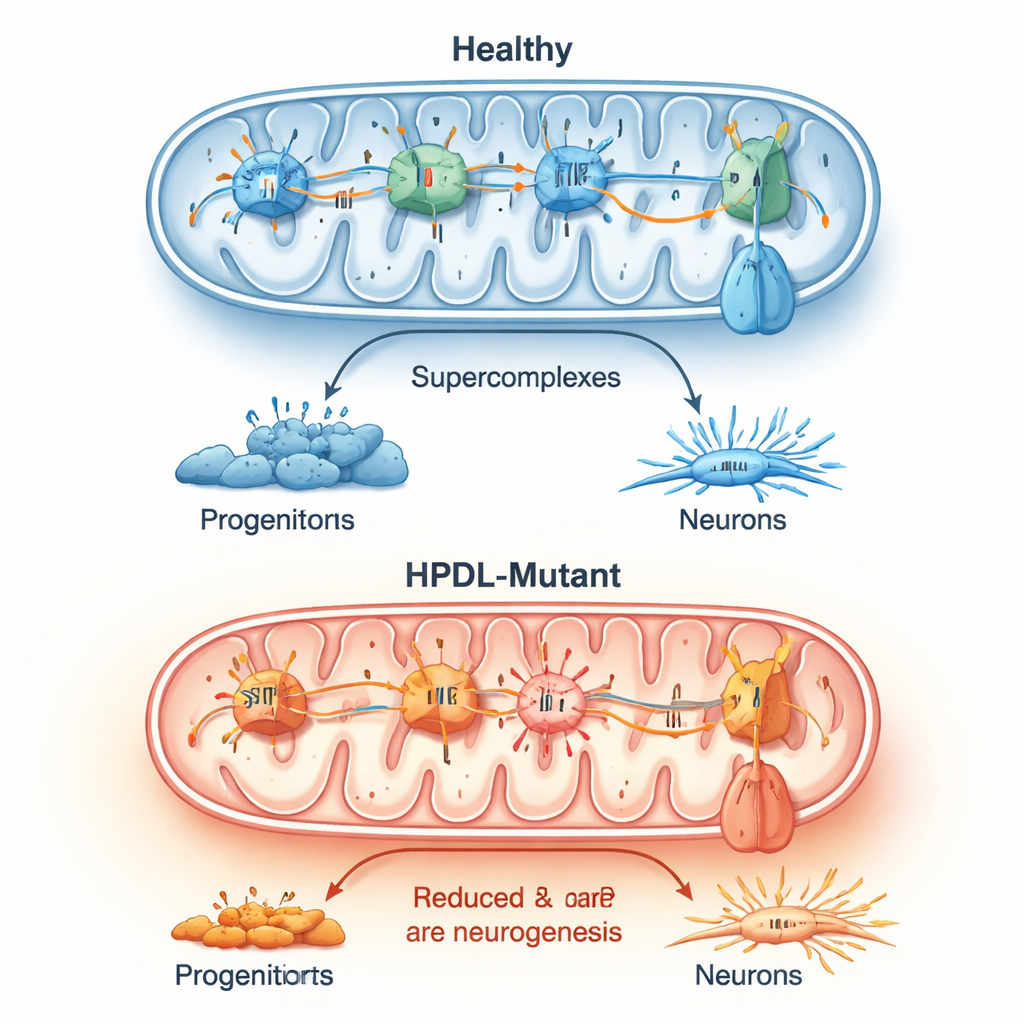
Сломанные «электростанции» и уставшие клетки
Более детальное исследование показало, что клетки мозга с мутациями HPDL имели нарушенное окислительное фосфорилирование — основной способ, которым митохондрии производят энергию. Окрашивание ферментов выявило ослабленную активность одного из ключевых митохондриальных комплексов, а другие меры показали изменённый электрический потенциал на мембране митохондрий. Во многих мутантных клетках критический фермент, обычно синтезирующий АТФ, по-видимому работал в обратном направлении, чтобы поддерживать этот мембранный потенциал, что свидетельствует о глубоком метаболическом стрессе. Во всех линиях пациентов уровни реактивных форм кислорода были постоянно повышены, а нормальные крупные комплексы дыхательной цепи формировались хуже. Эти митохондриальные изменения тесно коррелировали по времени и степени с преждевременным образованием нейронов.
Тестирование способов ослабить стресс
Поскольку, по-видимому, центральную роль играли окислительный стресс и нарушенная химия коэнзима Q10, команда проверила, могут ли методы, нацеленные на эти проблемы, замедлить переход к образованию нейронов. Они подвергли ранние корковые культуры воздействию двух антиоксидантов и 4-гидроксибензоата — малой молекулы, связанной с синтезом коэнзима Q10. В нескольких линиях, полученных от пациентов, эти соединения частично уменьшали преждевременную нейрогенезу, но ответ зависел от конкретной мутации HPDL. Некоторые линии реагировали преимущественно на антиоксиданты, другие — на предшественник коэнзима Q10, а одна линия не реагировала вовсе. Этот мутация-специфичный паттерн указывает на то, что для расстройств, связанных с HPDL, могут понадобиться персонализированные стратегии лечения.
Что это значит для детей и будущих терапий
Проще говоря, это исследование показывает, что HPDL действует как хранитель «строительного материала» мозга на ранних этапах развития. Когда HPDL не работает, митохондрии становятся неэффективными и чрезмерно напряжёнными, что подталкивает прогениторные клетки преждевременно превращаться в нейроны. Резерв делящихся клеток истощается, кора не может достичь полного размера, и схемы проводки изменяются, что способствует двигательным расстройствам и другим симптомам. Частичное восстановление, наблюдавшееся при применении антиоксидантов и соединений, связанных с коэнзимом Q10, намекает на то, что в будущем регулирование клеточного энергетического баланса и окислительного стресса может помочь детям с мутациями HPDL и, возможно, другим пациентам с митохондриальными формами заболеваний мозга.
Цитирование: Baggiani, M., Desbats, M.A., Naef, V. et al. Loss of function variants in HPDL impair human cortical development via alterations of mitochondrial function. Cell Death Dis 17, 237 (2026). https://doi.org/10.1038/s41419-026-08476-9
Ключевые слова: HPDL, митохондрии, развитие коры, микроцефалия, окислительный стресс