Clear Sky Science · ru
RIPK1 регулирует судьбу β-клеток через влияние на экспрессию генов и киназную сигнализацию в мышиной модели самореактивности β-клеток
Почему важно сохранять клетки, вырабатывающие инсулин
Сахарный диабет 1 типа развивается, когда собственная иммунная система организма разрушает инсулинопродуцирующие бета-клетки поджелудочной железы. После их исчезновения людям приходится полагаться на пожизненные инъекции инсулина. В этом исследовании изучается ключевой внутренний «переключатель» в бета-клетках — белок RIPK1, который помогает решать, выживет ли клетка или погибнет во время иммунной атаки. Понимание и контроль этого переключателя могут открыть новые пути для защиты оставшихся бета-клеток и, возможно, замедлить или смягчить течение диабета 1 типа.
Переключатель стресса внутри бета-клеток
В ходе развития диабета 1 типа бета-клетки оказываются в враждебной среде. Иммунные клетки выделяют провоспалительные сигналы — такие как TNFα и IFNγ, — которые тянут бета-клетки к стрессу и гибели. Белок RIPK1 выступает центральным решающим элементом во многих типах клеток, интегрируя эти сигналы и направляя клетки либо к выживанию, либо к различным формам запрограммированной гибели. В этой работе исследователи задали вопрос: играет ли RIPK1 ту же роль в бета-клетках при иммунной атаке и может ли ослабление активности RIPK1 помочь этим клеткам выжить.
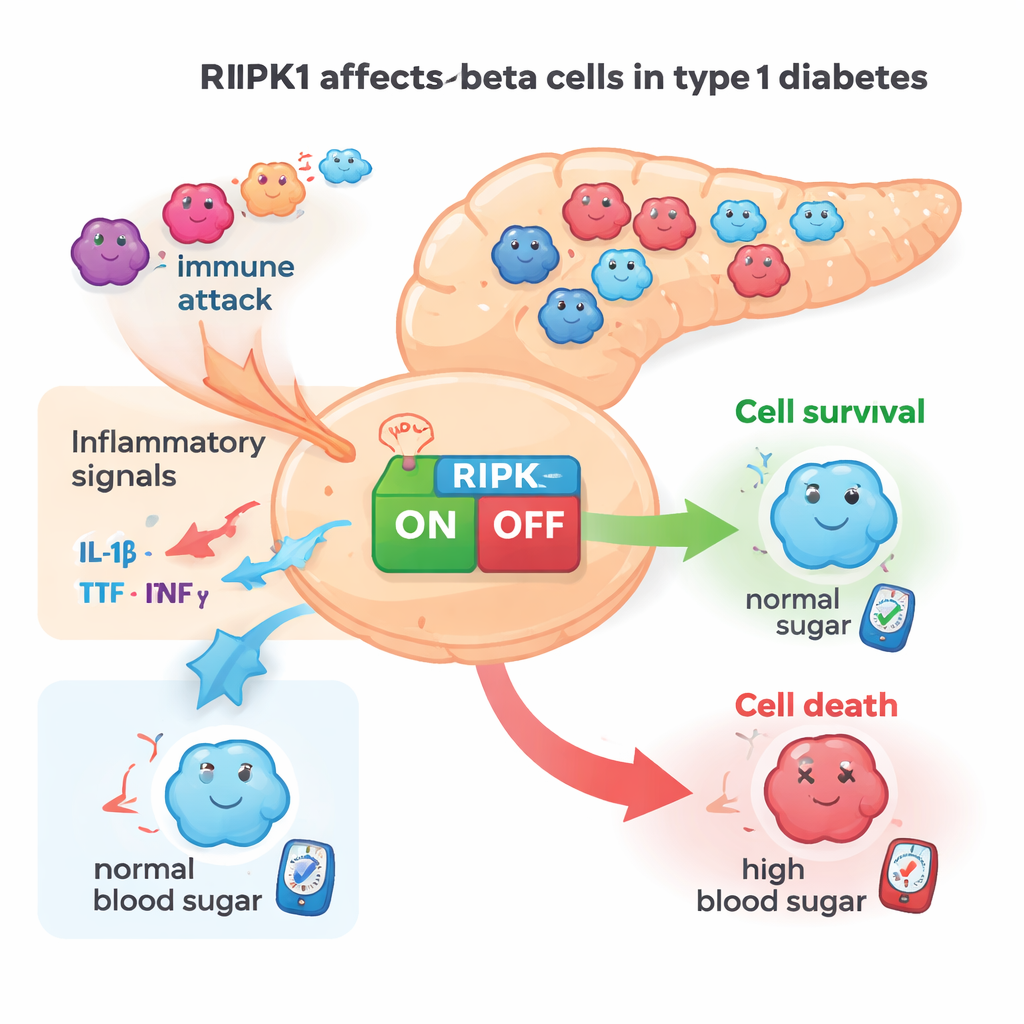
Уровень RIPK1 повышается в клетках, склонных к диабету
Сначала команда искала признаки участия RIPK1 в сахарном диабете 1 типа. Они обнаружили, что провоспалительные сигналы повышают активность RIPK1 в бета-клеточных линиях мышей и в выращенных в лаборатории человеческих бета-клетках. В тканях поджелудочной железы как у мышей, так и у людей RIPK1 ясно присутствовал в инсулинопродуцирующих клетках. Важно, что островки поджелудочной у предрасположенных к диабету NOD-мышей демонстрировали повышенную активность гена Ripk1 по мере старения животных и усиления аутоиммунитета. Данные одиночной клеточной транскриптомики от доноров-людей показали похожую картину: бета-клетки у людей с диабетом 1 типа содержали больше РНК RIPK1, чем у недиабетических доноров. В совокупности эти наблюдения указывают на RIPK1 как на стресс-ассоциированный белок, который становится более активным именно тогда, когда бета-клетки находятся под аутоиммунным давлением.
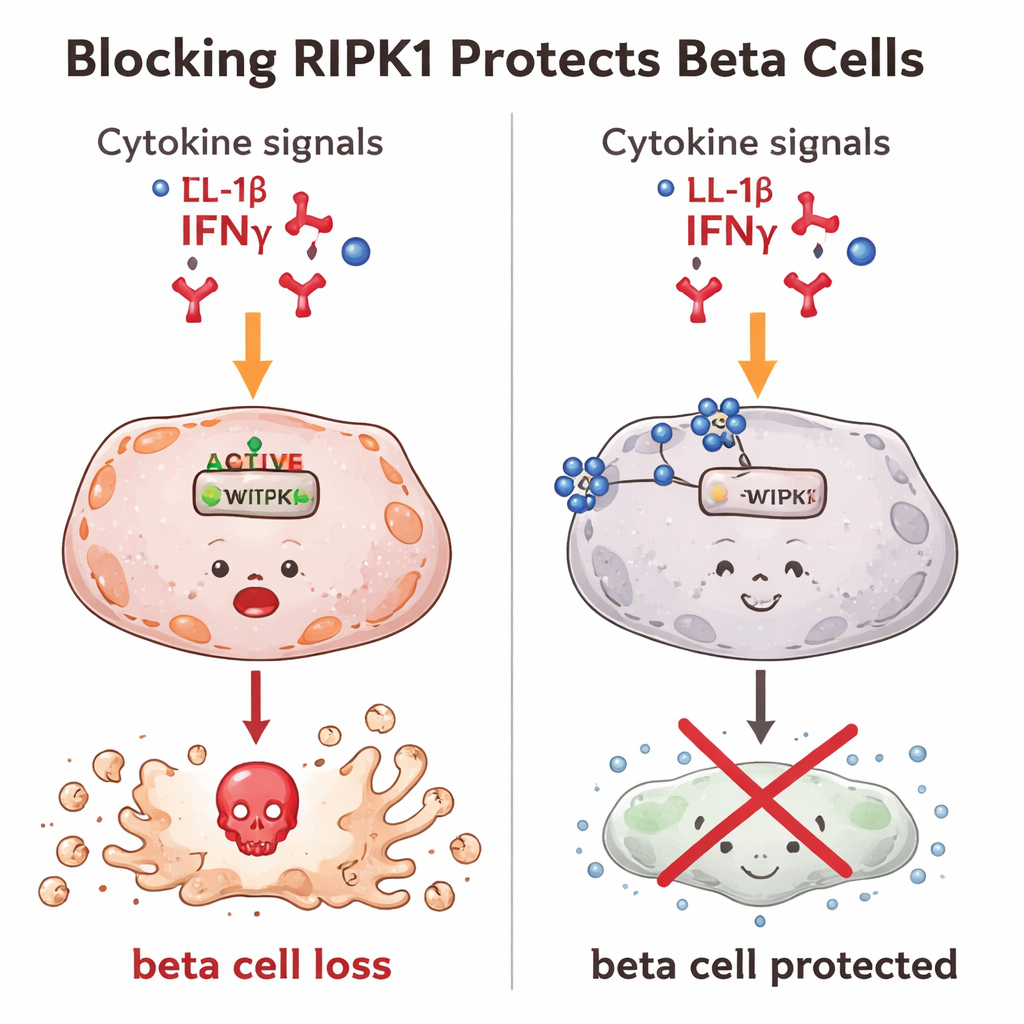
Блокирование RIPK1 помогает бета-клеткам выживать
Далее исследователи проверили, что происходит при блокаде RIPK1. В мышиных бета-клетках, подвергавшихся провоспалительным сигналам, RIPK1 обычно активировался и увеличивал гибель клеток. Когда ученые использовали небольшие молекулы, ингибирующие активность RIPK1 или уменьшающие его количество в клетке, значительно меньше бета-клеток гибло. Затем они применили инструменты редактирования генома, чтобы ослабить ген Ripk1, получив бета-клетки с существенно пониженным уровнем RIPK1. Эти редактированные клетки оказались заметно устойчивыми как к классическим путям «программируемой» гибели, так и к более взрывной, воспалительной форме гибели. Иными словами, снижение RIPK1 сохраняло больше бета-клеток в живых даже при сильных разрушающих сигналах.
Глубокие изменения программ клеток и сигнализации
Защита бета-клеток оказалась не только в блокаде одного пути гибели. С помощью масштабного секвенирования РНК команда обнаружила, что удаление RIPK1 перестраивает многие генетические программы в бета-клетках. Гены, связанные с воспалением и врожденными иммунными ответами, были подавлены, тогда как несколько генов, связанных с идентичностью бета-клетки и синтезом инсулина, были повышены. Одновременно широкое обследование активных ферментов показало, что утрата RIPK1 перенастраивает многочисленные сигнальные пути, включая системы MAPK и JAK, которые передают стрессовые и иммунные сообщения. Эти изменения указывают на то, что RIPK1 влияет не только на то, умрет ли бета-клетка, но и на то, насколько «воспаленной», узнаваемой и функциональной она является во время аутоиммунной атаки.
Сопротивление иммунной атаке в организме
Чтобы проверить значимость этих находок в более реалистичных условиях, исследователи смешали иммунные клетки, вызывающие диабет, из NOD-мышей с нормальными или лишенными RIPK1 бета-клетками. Обе группы бета-клеток по-прежнему могли активировать иммунные клетки, но клетки без RIPK1 уничтожались примерно вдвое реже, чем нормальные. В модели на мышах команда имплантировала в одних и тех же животных как нормальные, так и лишенные RIPK1 бета-клетки и затем вызвала аутоиммунную атаку. Со временем обычные трансплантаты бета-клеток почти исчезли, тогда как трансплантаты без RIPK1 оставались в десятки и более сотен раз ярче в биолюминесцентной визуализации, что указывало на значительно большее число выживших клеток после иммунного натиска.
Что это может означать для людей с диабетом 1 типа
Эта работа показывает, что RIPK1 действует как центральный переключатель стресса, который помогает решать, жить ли клеткам, производящим инсулин, или погибнуть во время аутоиммунных атак. При снижении активности RIPK1 бета-клетки реже гибнут, реже посылают провоспалительные сигналы и с большей вероятностью сохраняют свою идентичность и функцию. Препараты, безопасно нацеленные на RIPK1, уже изучаются при других заболеваниях, поэтому адаптация подобных стратегий для защиты бета-клеток может предложить новый подход к предотвращению или замедлению диабета 1 типа, особенно на ранних стадиях, когда часть бета-клеток еще жива.
Цитирование: Contreras, C.J., Mukherjee, N., Harris-Kawano, A. et al. RIPK1 regulates β-cell fate via actions on gene expression and kinase signaling in a mouse model of β-cell self-reactivity. Cell Death Dis 17, 220 (2026). https://doi.org/10.1038/s41419-026-08471-0
Ключевые слова: сахарный диабет 1 типа, бета-клетки, RIPK1, аутоиммунитет, клеточная гибель