Clear Sky Science · ru
Перенастройка судьбы меланомных клеток: модуляторы TRPM8 индуцируют апоптоз и усиливают цитотоксичность NK-клеток
Почему обращение «холодового датчика» против рака кожи важно
Меланома — опасная форма рака кожи, которая часто научается ускользать как от лекарств, так и от иммунной системы. В этом исследовании изучается неожиданная уязвимость меланомных клеток: белок TRPM8, известный прежде всего как сенсор, позволяющий нервным клеткам ощущать холод или ментол. Авторы показывают, что тщательно разработанные препараты, блокирующие TRPM8, способны подтолкнуть меланомные клетки к самоуничтожению и одновременно сделать их более уязвимыми для атаки со стороны естественных киллеров (NK-клеток). Это двойное действие намекает на новый подход к лечению стойкой, распространённой меланомы.
Скрытый переключатель на меланомных клетках
Анализируя крупные онкологические базы данных и исследуя в лаборатории клетки меланомы, полученные от пациентов, команда обнаружила, что TRPM8 значительно более выражен в метастатической меланоме, чем в нормальной коже, включая здоровые меланоциты и дермальные фибробласты. С помощью микроскопии показали, что TRPM8 локализуется и на поверхности клетки, и на внутренних мембранах, занимая стратегические позиции для влияния на поведение клетки. При обработке панелью новых молекул-таргетов TRPM8 два соединения (обозначенные как 4 и 9) стабильно выделялись: они резко снижали выживаемость меланомных клеток со временем, одновременно оставляя нормальные клетки кожи в основном невредимыми. Генетические тесты подтвердили: при удалении TRPM8 эти препараты теряли свою цитотоксичность, а при повышении экспрессии TRPM8 меланомные клетки становились ещё более чувствительны, что доказывает зависимость эффекта от этого конкретного канала. 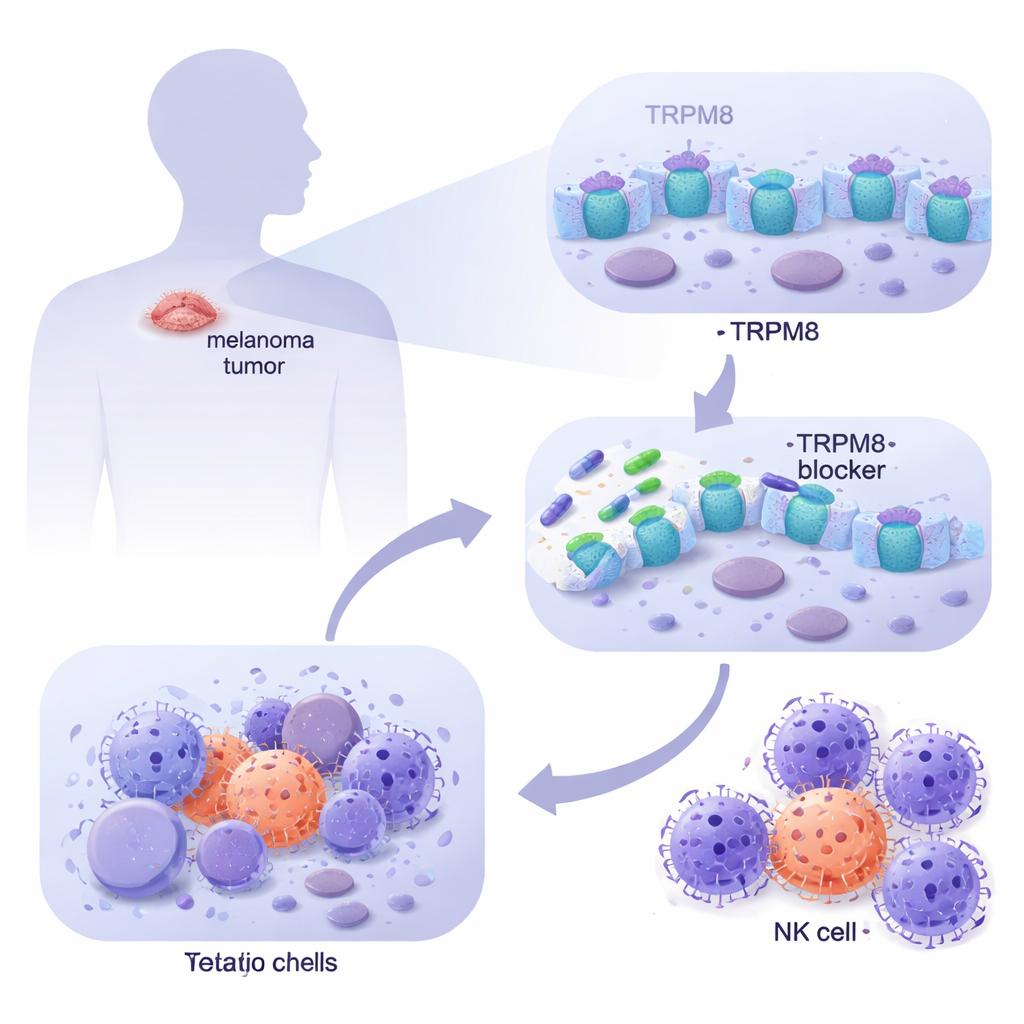
Вынуждение раковых клеток в энергетический кризис
В отличие от классических активаторов TRPM8, таких как ментол, которые вызывают приток кальция в клетки, эти новые блокаторы не вызывали изменений кальция. Вместо этого они запустили волну оксидативного стресса внутри меланомных клеток. Соединения быстро повышали уровень реактивных форм кислорода, особенно в митохондриях, энергетических фабриках клетки. Этот окислительный всплеск приводил к потере мембранного потенциала митохондрий, их фрагментации и утечке цитохрома c — ключевого шага в активации внутриклеточной программы «самоубийства». Антиоксиданты, удалявшие эти реактивные молекулы, в значительной степени спасали клетки, что указывает на то, что нарушение редокс‑баланса не побочный эффект, а движущая сила гибели клеток. В дальнейшем классические маркеры смерти, такие как активация каспазы‑3 и кливаж PARP, подтвердили, что клетки проходят программируемый апоптоз, а не случайное повреждение.
Обезвреживание сигналов выживания и пробуждение сторожа
Окислительный удар вызвал более широкий стресс‑ответ. Препараты активировали ATM — сенсор повреждений ДНК, и приводили к накоплению и активации p53, известного супрессора опухолей, который решает, пытаться ли повреждённой клетке восстановиться или погибнуть. Одновременно соединения ослабляли один из главных путей выживания меланомы: PI3K–AKT. Обычно TRPM8 физически взаимодействует с компонентами PI3K, помогая поддерживать AKT в активной, пролейтинговой форме. После лечения это взаимодействие разрывалось, и активность AKT падала, сдвигая баланс в сторону клеточной гибели. Важно, что эти изменения были выражены в меланомных клетках, но не в незлокачественных, что предполагает терапевтическое окно, при котором опухоль поражается сильно, а здоровая ткань остаётся защищённой.
Делая опухоли заметнее для иммунных «ударных групп»
Опасность меланомы также заключается в её умении ускользать от иммунного надзора. Поэтому исследователи проверили, что происходит с опухолевыми клетками, пережившими низкие дозы блокаторов TRPM8 в течение длительного времени. Они обнаружили, что эти уцелевшие клетки начинают проявлять больше поверхностного маркера ULBP1, который действует как сигнал бедствия, распознаваемый рецепторами NKG2D на NK‑клетках. Другие родственные маркеры не менялись, указывая на селективный эффект. В трёхмерных сфериоидах меланомы, которые лучше имитируют реальные опухоли, предварительная обработка блокаторами TRPM8 не только уменьшала размеры структур и увеличивала гибель клеток, но и значительно повышала их уязвимость к атаке NK‑клеток. При блокировании ULBP1 или NKG2D антителами это дополнительное уничтожение в значительной степени исчезало, что показывает: улучшенная иммунная очистка осуществляется через конкретное взаимодействие между опухолью и NK‑клетками. 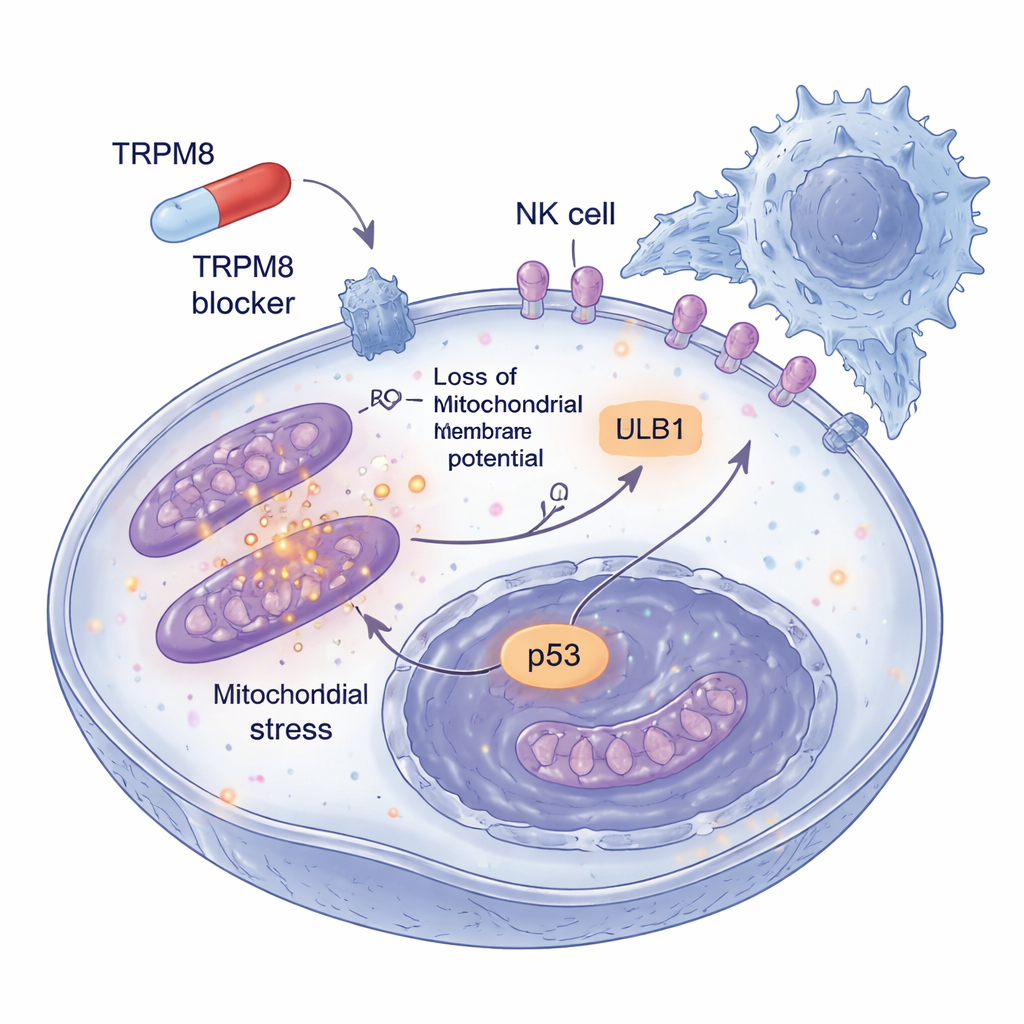
Что это может означать для будущего лечения меланомы
Проще говоря, блокирование «холодового датчика» TRPM8 превращает его в терапевтический рычаг: это вталкивает меланомные клетки в фатальный митохондриальный и ДНК‑кризис и одновременно помечает их для уничтожения NK‑клетками. Поскольку препараты щадят нормальные клетки кожи и не вредят самим NK‑клеткам, они представляют собой перспективную базу для новых методов лечения. Авторы предполагают, что блокаторы TRPM8 могут сочетаться с существующими иммунотерапиями, чтобы атаковать продвинутую, лекарственно‑устойчивую меланому по двум направлениям: непосредственно убивая опухолевые клетки и делая выживших более заметными и уязвимыми для иммунной системы.
Цитирование: Sorrentino, C., Lauretta, C., D’Angiolo, R. et al. Rewiring melanoma cell fate: TRPM8 modulators trigger apoptosis and boost NK cell cytotoxicity. Cell Death Dis 17, 223 (2026). https://doi.org/10.1038/s41419-026-08469-8
Ключевые слова: меланома, TRPM8, митохондрии, окислительный стресс, натуральные киллеры