Clear Sky Science · ru
Лактилирование, индуцирующее TRIM29, вызывает инвазивное поведение и метастазирование в лимфатические узлы при раке желудка через путь Wnt/β-катенин, опосредованный hnRNPA1
Почему это исследование важно
Рак желудка — один из самых смертоносных видов рака в мире главным образом потому, что он рано распространяется в близлежащие лимфатические узлы, что затрудняет излечение хирургическим путем. В этом исследовании показано, как химическая модификация, связанная с метаболизмом опухоли, активирует белок TRIM29, помогая раковым клеткам проникать в окружающие ткани, стимулировать образование новых лимфатических сосудов и сопротивляться химиотерапии. Понимание этой цепочки событий открывает новые пути для замедления или даже блокирования распространения рака желудка.
Опасное сотрудничество в опухолях желудка
Исследователи начали с сопоставления образцов рака желудка с соседней нормальной тканью у 100 пациентов, а также с большими публичными геномными базами данных. Они обнаружили, что TRIM29, белок ранее связанный с регуляцией иммунитета и другими видами рака, постоянно повышен в опухолевых клетках. У пациентов с высоким уровнем TRIM29 в опухолях чаще выявлялись поражения лимфатических узлов и сосудов, а выживаемость в целом была ниже. Эти закономерности указывают на то, что TRIM29 не просто присутствует, но активно участвует в повышении агрессивности рака желудка.
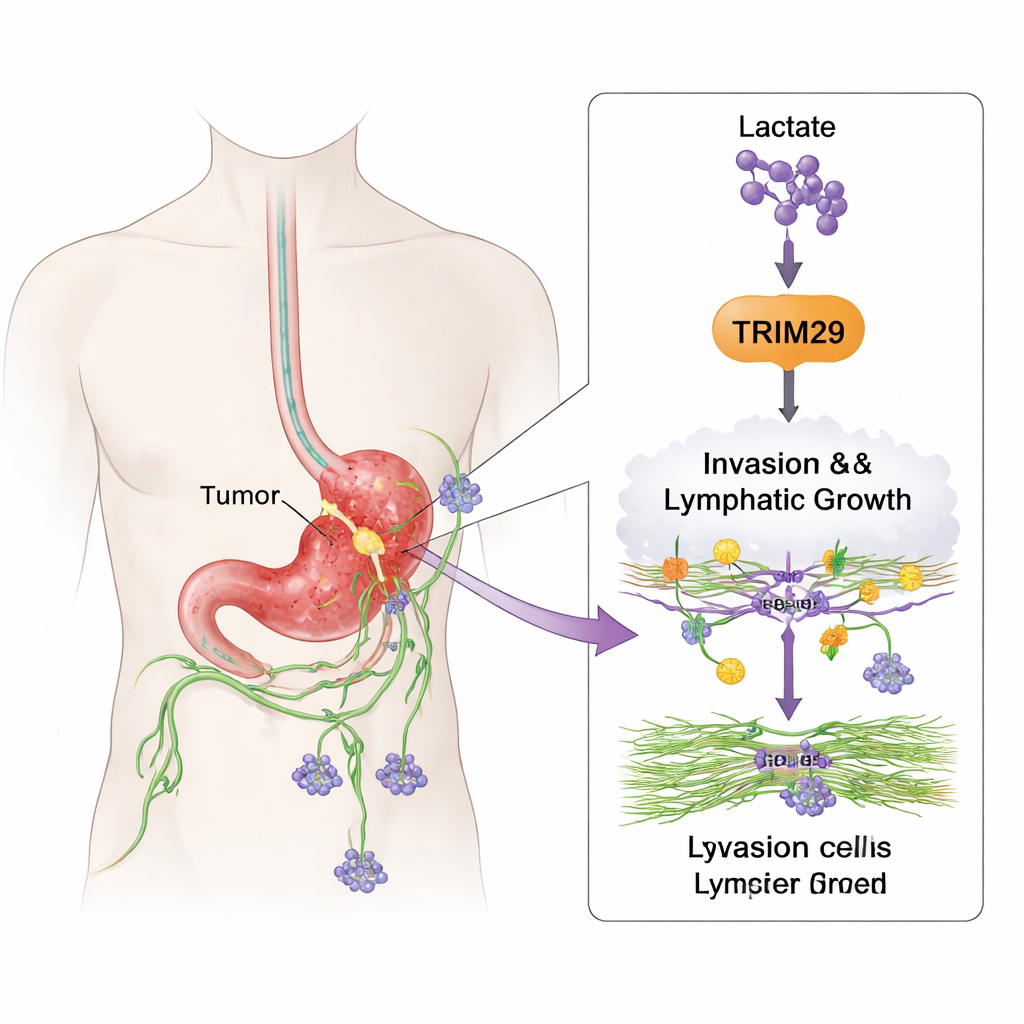
Как раковые клетки учатся путешествовать
Чтобы выяснить функцию TRIM29, команда изменила его уровни в клеточных линиях рака желудка. При снижении TRIM29 клетки заметно теряли подвижность и способность проталкиваться через 3D-гели, имитирующие ткань организма. Повышение уровня TRIM29 давало противоположный эффект, делая клетки более инвазивными. Исследователи также изучали лимфатические эндотелиальные клетки, выстилающие лимфатические сосуды. Клетки рака с высоким содержанием TRIM29 стимулировали эти сосудистые клетки к отрастанию и формированию трубчатых структур — признак лимфангиогенеза. В модельных экспериментах на мышах опухоли с высоким TRIM29 давали больше метастазов в печень и лимфатические узлы, тогда как при подавлении TRIM29 распространение уменьшалось и формировалось меньше лимфатических сосудов.
Молекулярная передача: защита ключевого регулятора
Вглубь механизма учёные обнаружили, что TRIM29 физически связывается с другим белком — hnRNPA1, известным влиянием на процессинг генов и связью с метастазированием. Обычно hnRNPA1 может помечаться для разрушения другим белком‑ферментом ZFP91 через систему утилизации клеточных белков. TRIM29 вмешивается в этот процесс, конкурируя с ZFP91 за связывание с hnRNPA1. При избытке TRIM29 он защищает hnRNPA1 от пометки и распада. В результате hnRNPA1 стабилизируется и накапливается в раковых клетках, что запускает цепь сигналов, завершающуюся активацией пути Wnt/β‑катенин — известного фактора роста и мобильности опухолей. Это, в свою очередь, повышает производство VEGF‑C — молекулы, стимулирующей образование лимфатических сосудов, предоставляя клеткам опухоли больше «дорог» для выхода из ткани.
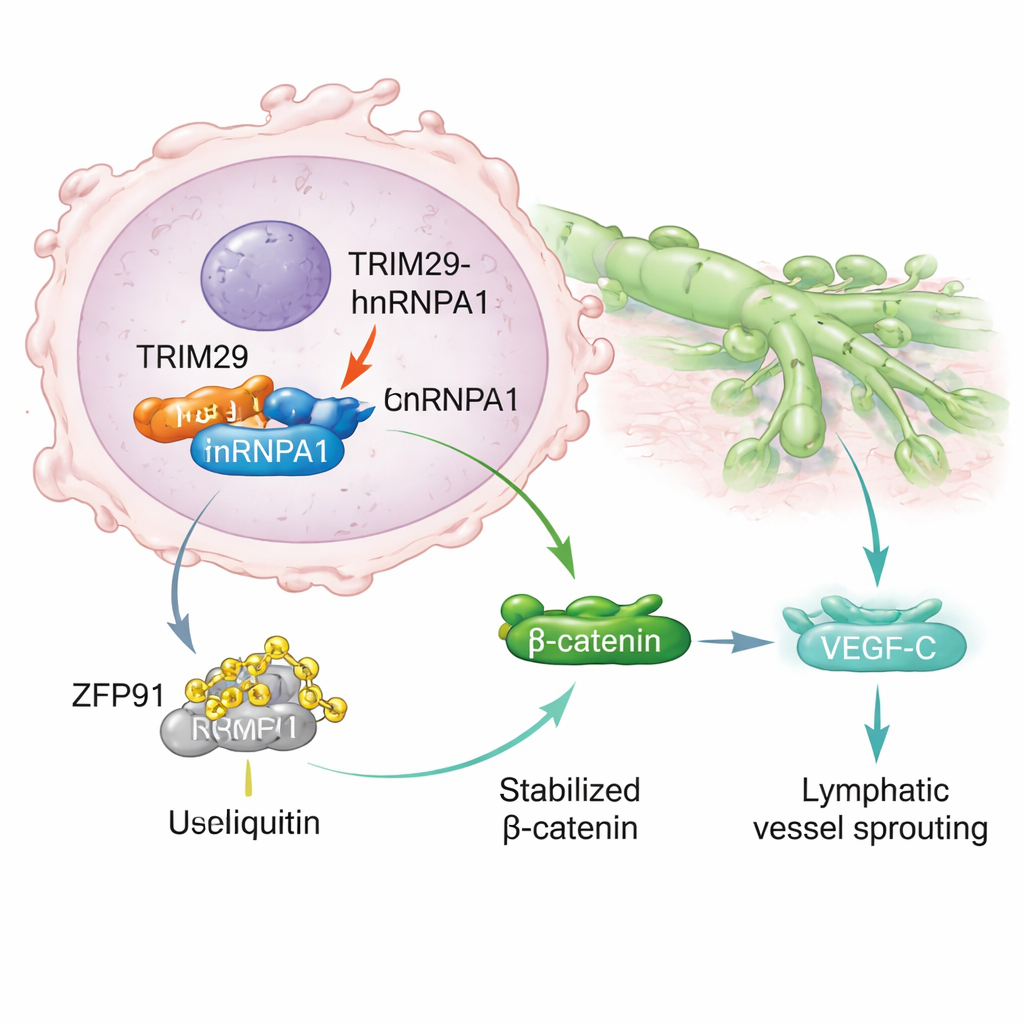
Подпитка рака лактатом
Исследование также связывает инвазивное поведение с метаболической переработкой сахаров в опухоли. Быстро растущие опухоли часто полагаются на метаболизм, который производит большое количество лактата — побочного продукта, который раньше считали лишь отходом. Авторы показывают, что лактат может химически модифицировать гистоны — белки, упаковующие ДНК, в частности в положении H3K9. Это «лактилирование» действует как переключатель для гена TRIM29, усиливая его экспрессию. При снижении производства лактата с помощью метаболических препаратов уровень TRIM29 падал; при увеличении лактата TRIM29 возрастал. Ткани рака желудка у пациентов демонстрировали повышенные уровни лактилирования H3K9, что коррелировало с повышенным TRIM29, большим числом метастазов в лимфатические узлы и худшей выживаемостью. По сути, изменённый метаболизм опухоли помогает задать более агрессивную генетическую программу.
Новые способы усилить химиотерапию
Лимфатические сосуды выполняют не только транспорт раковых клеток — они также могут отводить химиопрепараты из опухолей. Используя трансплантаты опухолей пациентов, выращенные у мышей, исследователи проверили, может ли блокирование TRIM29 и роста лимфатических сосудов улучшить действие 5‑фторурацила (5‑FU), стандартного препарата при раке желудка. Инактивация TRIM29 или блокада лимфангиогенеза по отдельности делала 5‑FU более эффективным в сокращении опухолей и снижении деления клеток. Сочетание обеих стратегий давало наилучший эффект, что указывает на потенциальный путь преодоления некоторой формы лекарственной устойчивости при запущенном заболевании.
Что это значит для пациентов
Это исследование даёт пошаговую картину: опухоли желудка вырабатывают избыток лактата, который включает TRIM29; TRIM29 затем защищает hnRNPA1, стабилизирует сигнальный путь роста и усиливает образование лимфатических сосудов и распространение в лимфатические узлы. Клинически высокий уровень TRIM29 и связанные маркеры лактилирования идентифицируют пациентов с более высоким риском агрессивного течения. В будущем препараты, уменьшающие лактат‑сигнализацию, блокирующие TRIM29 или предотвращающие рост лимфатических сосудов, могут быть комбинированы с существующей химиотерапией, чтобы ограничить распространение рака желудка и повысить эффективность лечения.
Цитирование: Hua, R., Yu, J., Niu, Y. et al. Lactylation-drived TRIM29 induces invasive behavior and lymph node metastasis in gastric cancer via hnRNPA1-mediated Wnt/β-catenin pathway. Cell Death Dis 17, 222 (2026). https://doi.org/10.1038/s41419-026-08468-9
Ключевые слова: метастазирование рака желудка, TRIM29, лактат и лактилирование, лимоангиогенез, путь Wnt бета-катенин