Clear Sky Science · ru
Селенометионин как ингибитор ферроптоза с двойным механизмом действия: поставка селена для биосинтеза GPX4 помимо транссульфурации и тушение ROS за счёт восстановительной способности, независимой от активности GPX4
Почему важно защищать клетки от «ржавления»
Клетки в организме могут погибать по-разному, и один из новейших и наиболее интригующих способов называется ферроптозом — специфическим видом повреждения мембран, напоминающим ржавчину, вызванным железом. Этот процесс уже связан с рядом заболеваний — от поражений почек до нейродегенерации. Микроэлемент селен, знакомый многим из пищевых добавок, играет ключевую роль в предотвращении этого опасного типа гибели клеток. В данном исследовании изучается, как распространённая селенсодержащая аминокислота селенометионин защищает клетки от ферроптоза посредством не одной, а двух различных защитных стратегий.
Новый защитник обнаружен в крупном поиске препаратов
Чтобы найти малые молекулы, способные блокировать ферроптоз, исследователи просканировали тысячи соединений из числа одобренных FDA препаратов и природных продуктов. Они использовали химикат RSL3 для индукции ферроптоза в человеческих раковых клеточных линиях и отслеживали гибель клеток и накопление окисленных липидов в мембранах. Среди всех кандидатов селенометионин выделился как мощный защитник: он снижал повреждение липидов и гибель клеток в разных типах клеток и в двух основных моделях ферроптоза — при прямой ингибиции GPX4 (RSL3) и при дефиците цистина, строительного блока для антиоксиданта глутатиона. Эти результаты показали, что селенометионин является широким и надёжным ингибитором ферроптоза. 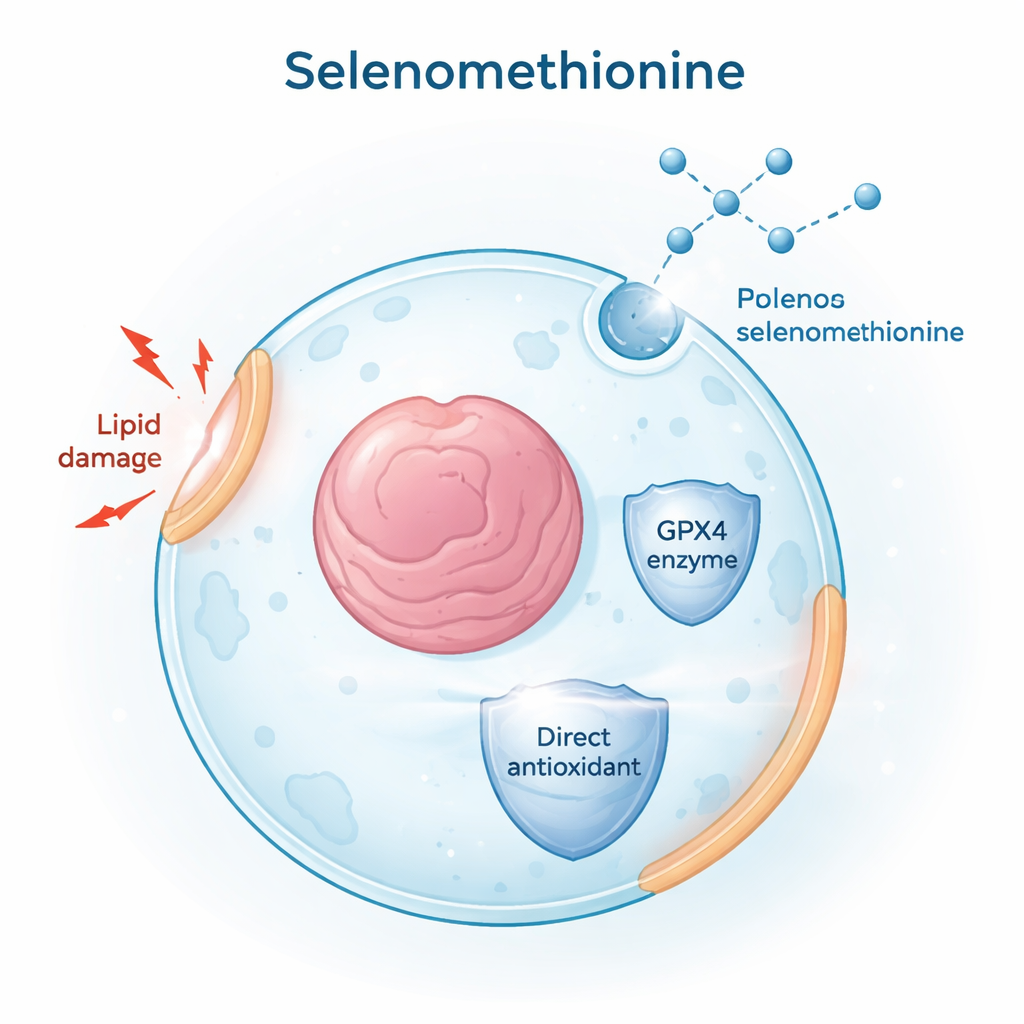
Поставка селена для ключевого защитного фермента
Основной антиферроптозный щит в клетке — фермент GPX4, для функционирования которого необходим селен. Команда поставила цель выяснить, просто ли селенометионин подпитывает этот путь или действует шире. Они отследили, как селен из селенометионина может превращаться в формы, пригодные для включения в GPX4, даже когда обычный путь — транссульфурация — нарушен или заблокирован. С помощью генетического понижения экспрессии и химических ингибиторов ферментов в серо‑селеновых путях они обнаружили, что селенометионин по‑прежнему повышает уровни GPX4 и защищает клетки. Это показало, что клетки могут использовать несколько метаболических маршрутов для извлечения селена из селенометионина и поддерживать синтез GPX4 даже в тканях, где классический путь слабо выражен.
Защита, не зависящая от привычного фермента
Удивительно, но при полном удалении GPX4 из клеток с помощью CRISPR селенометионин продолжал защищать от ферроптоза. Он по‑прежнему снижал повреждение липидов мембран и гибель клеток, что указывает на то, что GPX4 — не единственный фактор. Дополнительные эксперименты дали основания полагать, что часть этой защиты связана с включением селенометионина в вновь синтезируемые белки, но это объясняет лишь часть эффекта. Авторы затем сосредоточились на химической реактивности самого селенометионина. Они обнаружили, что он может напрямую нейтрализовать реактивные формы кислорода (ROS), включая перекись водорода, и превращаться в окислённую форму — сульфоксид. Масс‑спектрометрия подтвердила этот продукт, а введение в клетки уже окислённой формы также снижало ферроптоз, что подразумевает, что клетки могут восстанавливать её обратно в активный селенометионин в рамках редокс‑цикла.
От культуральных экспериментов к защите почек у животных
Чтобы проверить, имеют ли эти механизмы значение в целом организме, команда использовала мышиную модель острого повреждения почек, вызванного противоопухолевым препаратом цисплатином — состояние, в котором участвует ферроптоз. Мыши, получавшие цисплатин, теряли вес, у них увеличивался объём почек, ухудшалась функция почек и повышались маркёры ферроптоза. При лечении селенометионином многие из этих нарушений уменьшались: масса тела восстанавливалась, отёчность почек снижалась, показатели функции почек в крови нормализовались, воспалительные сигналы уменьшились, а химические маркёры липидного повреждения упали. В почечной ткани также отмечали более высокие уровни GPX4 и меньше структурных повреждений. Эти преимущества были сопоставимы с эффектами ферростатина‑1, известного экспериментального ингибитора ферроптоза. 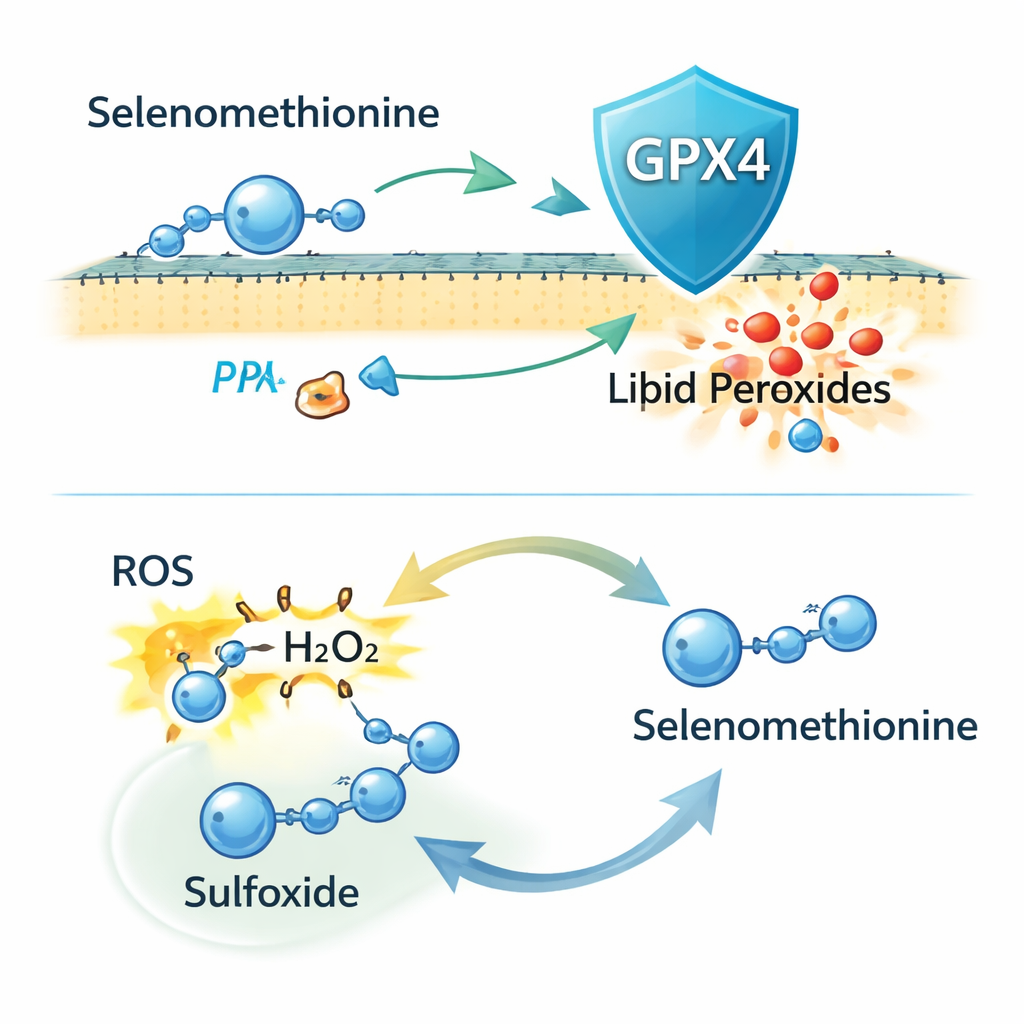
Что это означает для будущих терапий
Проще говоря, работа показывает, что селенометионин действует как двуфункциональный огнетушитель против железозависимого «ржавления» клеточных мембран. С одной стороны, он поставляет селен, позволяя клеткам синтезировать больше фермента GPX4, который действует как внутренняя служба очистки для повреждённых липидов. С другой стороны, сам селенометионин может поглощать вредные окислители и участвовать в цикле восстановления, обеспечивая резервную защиту, независимую от GPX4. В совокупности эти свойства делают селенометионин перспективным кандидатом для профилактики или лечения заболеваний, где ферроптоз играет ключевую роль, например, при повреждении почек, вызванном лекарствами, и, возможно, при других состояниях, связанных с неконтролируемым окислительным стрессом.
Цитирование: Xia, C., Sun, X., Shao, J. et al. Selenomethionine as a dual-mechanism ferroptosis inhibitor: selenium-supply-driven GPX4 biosynthesis beyond transsulfuration and reductive-capacity-mediated ROS scavenging independent of GPX4 activity. Cell Death Dis 17, 224 (2026). https://doi.org/10.1038/s41419-026-08466-x
Ключевые слова: ферроптоз, селен, селенометионин, окислительный стресс, острое повреждение почек