Clear Sky Science · ru
Компонент шаперонина TRiC Cct3 необходим для аксоплазматической транспортировки, миелинизации и донастройки нейромышечных синапсов
Когда проводка нервов нарушается
Наш мозг и тело полагаются на длинные кабелеобразные нервные волокна, которые передают сигналы быстро и надежно. Для этой работы многие нервы покрыты изолирующей миелиновой оболочкой, а их концы должны формировать точные контакты с мышцами. В статье исследуют, что происходит, когда ключевой клеточный «помощник» в сворачивании белков, называемый Cct3, не выполняет свою функцию. На примере данио-рерио и человеческих тканей авторы показывают, как один компонент большой машины-шаперона может нарушить миелин, контакты нерв–мышца и внутреннюю транспортную систему, которая поддерживает нейроны живыми и работоспособными.
Клеточный портной, строящий нервы
Внутри каждой клетки вновь синтезированные белки должны приобретать правильную форму, подобно тому как портной точно подгоняет костюм. Комплекс TRiC, включающий субъединицу Cct3, — один из основных «портных», помогающий сворачивать примерно 10% всех клеточных белков, особенно структурные белки актин и тубулин. Эти строительные блоки формируют внутренний каркас клетки и «рельсы», по которым перемещается жизненно важный груз. У пациентов с дефектными вариантами CCT3 и родственных генов на снимках мозга выявляют уменьшение белого вещества (миелин-обогащённой проводящей ткани) и проблемы в периферических нервах и мышцах. Авторы поставили задачу понять, как потеря Cct3 срывает развитие и функцию нервной системы.
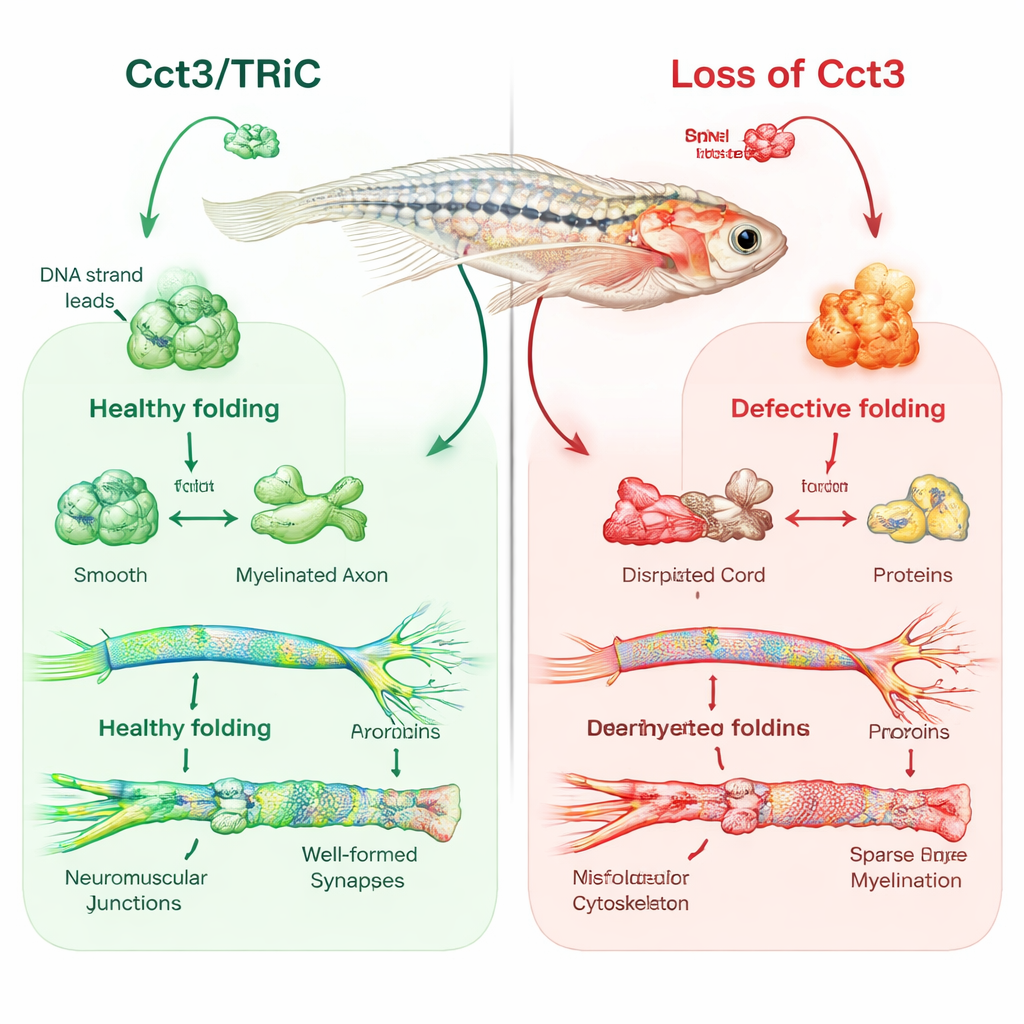
Данио-рерио как окно в мир нервной изоляции
Исследователи использовали редактирование генома CRISPR/Cas9, чтобы получить данио-рерио без функционального cct3. У этих рыбок наблюдали уменьшенные мозг и глаза, скопление жидкости вокруг сердца, слабую реакцию на прикосновение, и они умирали в течение нескольких дней. Когда учёные восстанавливали нормальный cct3, вводя его матричную РНК, многие дефекты корректировались, что подтвердило, что потеря Cct3 является коренной причиной. Сосредоточившись на миелине, они применили флуоресцентные метки и электронную микроскопию, чтобы визуализировать изолирующие слои вокруг нервов. У нормальных рыб клетки, формирующие миелин, в мозге и периферических нервах аккуратно обвивали аксоны многослойными оболочками к четвёртому дню развития. Напротив, у мутантов cct3 число миелинизирующих клеток было значительно меньше, и многие аксональные участки практически не имели нормальной миелиновой оболочки, несмотря на нормальный внешний вид самих аксонов.
Хрупкие поддерживающие клетки и напряжённые нервно‑мышечные связи
Чтобы выяснить, почему миелин отсутствует, авторы изучили шванновские клетки и связанные с ними клетки нервного гребня — поддерживающие клетки, которые обвивают периферические нервы. У нормальных рыб эти клетки вытягивали длинные тонкие отростки и затем упорядочивали свою форму при формировании миелиновых сегментов. У мутантов они округлялись, укорачивали отростки и фрагментировались. Их ядра распадались по типичному паттерну запрограммированной гибели, и появился ключевой маркер гибели (активированный Caspase 3), что указывает на преждевременную гибель многих этих клеток. Тем временем на нейромышечных синапсах, где нервы контактируют с мышцами, схема «горячих точек» рецепторов на мышцах не донастраивалась. Вместо множества маленьких точных кластеров у мутантов были более крупные и редкие участки рецепторов, что перекликалось с упрощённой синаптической структурой, наблюдавшейся у человека с мутацией CCT3.
Разрушенные внутренние «рельсы» и замедленное движение груза
Поскольку TRiC помогает сворачивать актин и тубулин, авторы внимательно изучили внутренний каркас моторных аксонов. Они обнаружили резкое снижение общего уровня тубулина у мутантов и драматическое уменьшение числа нормальных микротрубочек — полых трубочек, служащих транспортными путями — как в центральных, так и в периферических нервах. Химические «метки» на тубулине, важные для стабильных, пригодных для транспорта микротрубочек, также были сильно изменены. С помощью живой визуализации светящихся митохондрий и эндосом внутри моторных аксонов исследователи проследили движение этих грузов. У здоровых рыб органеллы быстро и направленно перемещались вдоль аксона. У мутантов многие органеллы застревали или лишь покачивались взад‑вперёд, что соответствует повреждённым «рельсам» и нарушенному транспорту.
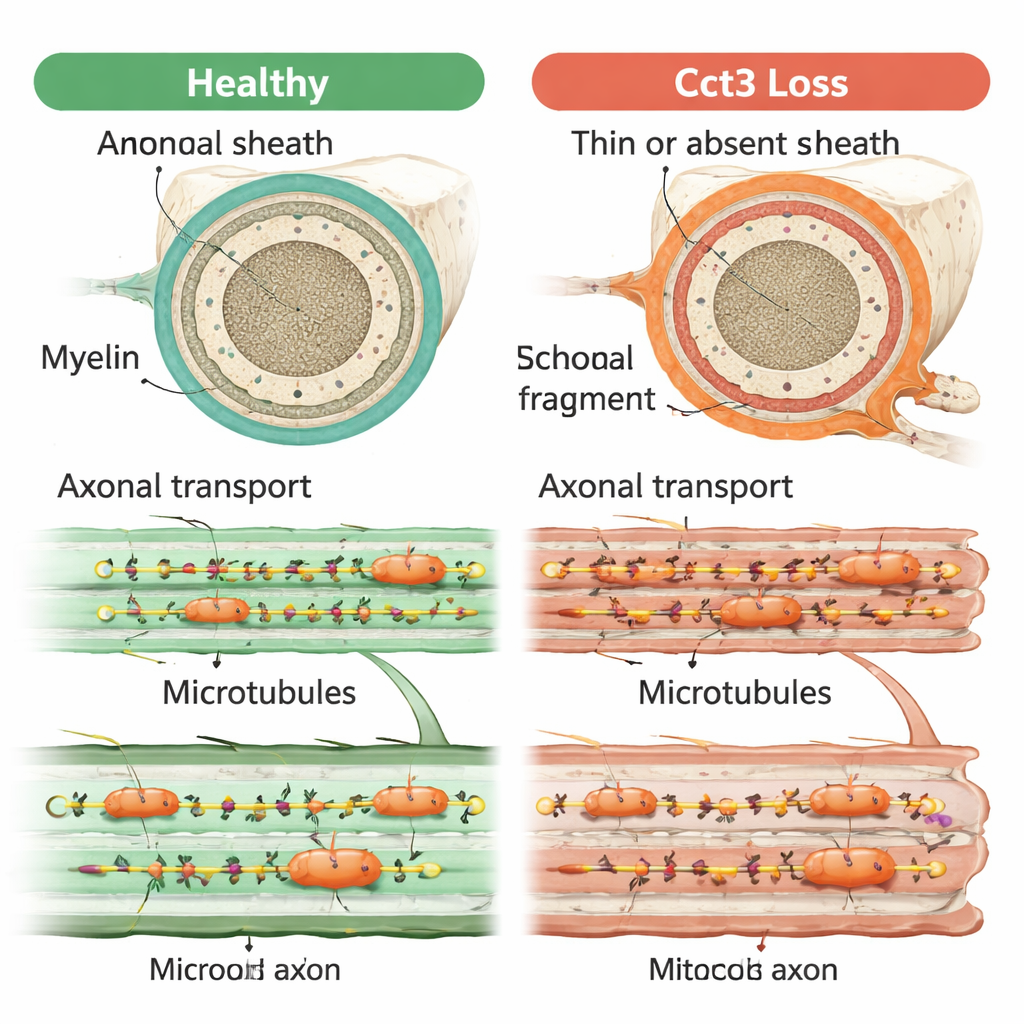
Одна фундаментальная проблема за множеством симптомов
В совокупности результаты показывают, что Cct3 необходим для нескольких взаимосвязанных аспектов здоровья нервов: он поддерживает выживание миелинизирующих поддерживающих клеток, обеспечивает правильное обёртывание миелина и позволяет созревающим нейромышечным синапсам тонко настраиваться. Все эти роли восходят к его функции в сворачивании и поддержании белков, формирующих цитоскелет и микротрубочные «рельсы», используемые для аксоплазматической транспортировки. Когда эти рельсы выходят из строя, ключевые сигналы и вещества не достигают нужных участков вдоль нерва, что, вероятно, подрывает как коммуникацию с миелинизирующими клетками, так и формирование нервно‑мышечных контактов. Эта работа указывает на то, что нарушенная аксоплазматическая транспортировка может быть общей ниточкой, связывающей разнообразные мозговые и нервные нарушения при расстройствах, связанных с TRiC.
Цитирование: Zhang, X., Zajt, K.K., Palaz, T. et al. The chaperonin TRiC component Cct3 is required for axonal transport, myelination, and neuromuscular junction refinement. Cell Death Dis 17, 221 (2026). https://doi.org/10.1038/s41419-026-08465-y
Ключевые слова: миелинизация, аксоплазматическая транспортировка, нейромышечный синапс, молекулярные шапероны, модель на данио-рерио