Clear Sky Science · ru
Сигнализация ацетилирования PDHA1 подавляет купроптоз и ослабляет эффект антиандрогенов при раке предстательной железы
Почему это исследование важно
Рак предстательной железы — одно из самых распространённых онкологических заболеваний у мужчин; многие продвинутые случаи лечат препаратами, блокирующими мужские гормональные сигналы. Ключевой препарат, энзалутамид, часто сначала эффективен, но затем перестаёт помогать по мере развития резистентности опухолей. В этом исследовании раскрывается неожиданный механизм, благодаря которому некоторые опухоли ускользают от действия энзалутамида, и показано, что блокирование одного метаболического пути может вновь сделать опухоли чувствительными, что открывает путь к более длительным и эффективным методам лечения.
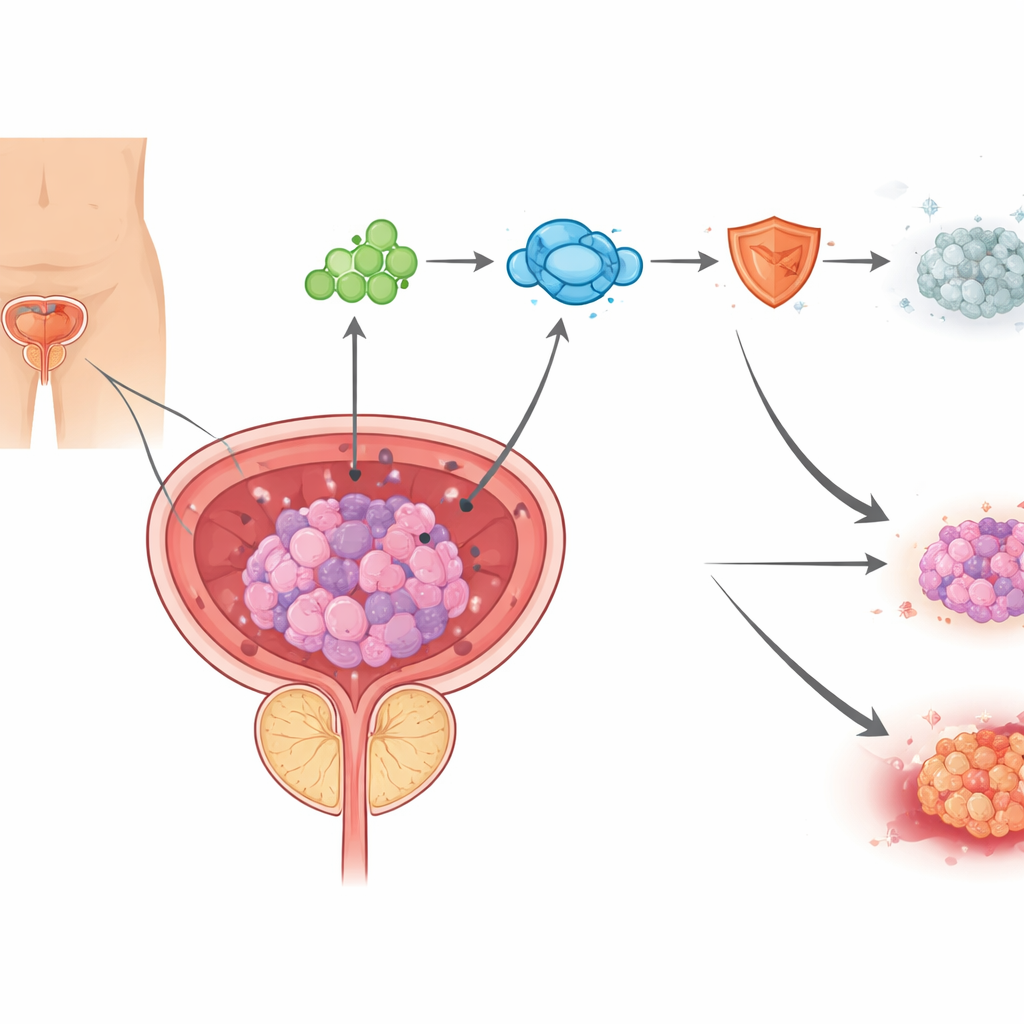
Новый тип гибели клеток, вызванный медью
Клетки могут погибать по разным сценариям, и современная онкология всё чаще пытается вновь включать эти природные программы гибели в опухолевых клетках. Авторы сосредоточились на недавно описанном виде гибели клеток — купроптозе, который запускается при накоплении меди в митохондриях, энергетических станциях клетки. В образцах рака предстательной железы пациентов, лечившихся антиандрогенами, исследователи обнаружили признаки накопления меди и повреждения митохондрий наряду с белковыми изменениями, типичными для купроптоза. В клеточных культурах энзалутамид повышал уровни меди и повреждал митохондрии, а соединение, связывающее медь, в значительной мере спасало клетки, что показывает: часть цитотоксичности энзалутамида связана с индуцированием медью‑опосредованной гибели клеток.
Как опухоли смягчают токсичность меди
Однако не все раковые клетки гибнут. Проанализировав несколько наборов данных по резистентным к энзалутамиду опухолям и сосредоточившись на генах, связанных с купроптозом, авторы выделили один ключевой белок: PDHA1, компонент ферментного комплекса, превращающего продукты расщепления сахаров в ацетил‑CoA — важный клеточный строительный блок. Уровни PDHA1 были выше в резистентных опухолях, это коррелировало с худшим выживанием и более агрессивным течением болезни, и сам энзалутамид повышал экспрессию PDHA1. В экспериментах в культуре клетки, у которых снижали PDHA1, становились значительно чувствительнее как к энзалутамиду, так и к прямому индукторам купроптоза, тогда как повышение PDHA1 делало их более устойчивыми к гибели. В экспериментах на мышах опухоли с пониженным PDHA1 значительно сильнее сокращались под действием энзалутамида, подтверждая, что этот фермент помогает опухолям противостоять терапии в живом организме.
Метаболический и эпигенетический щит против лечения
Далее команда выяснила, как PDHA1 создает этот щит. Поскольку PDHA1 участвует в производстве ацетил‑CoA, они протестировали, не влияет ли он на упаковку и чтение ДНК. При высоком уровне PDHA1 возрастали уровни ацетил‑CoA и ацетильные метки на гистонах, особенно те, что связаны с активной транскрипцией генов. Одним из ключевых «выгодополучателей» оказался SLC7A11 — транспортер, ввозящий цистеин в клетки для синтеза глутатиона, главного антиоксиданта. При повышенном PDHA1 клетки синтезировали больше глутатиона; при снижении PDHA1 уровни цистеина и глутатиона падали. Глутатион, в свою очередь, связывал и нейтрализовал медь, снижая стресс, запускающий купроптоз. Восстановление глутатиона или SLC7A11 отменяло усиление медного стресса, наблюдаемое при блокаде PDHA1, показывая, что цепочка PDHA1–ацетил‑CoA–гистоны–SLC7A11–глутатион позволяет опухолевым клеткам «вычищать» медь и избегать гибели.
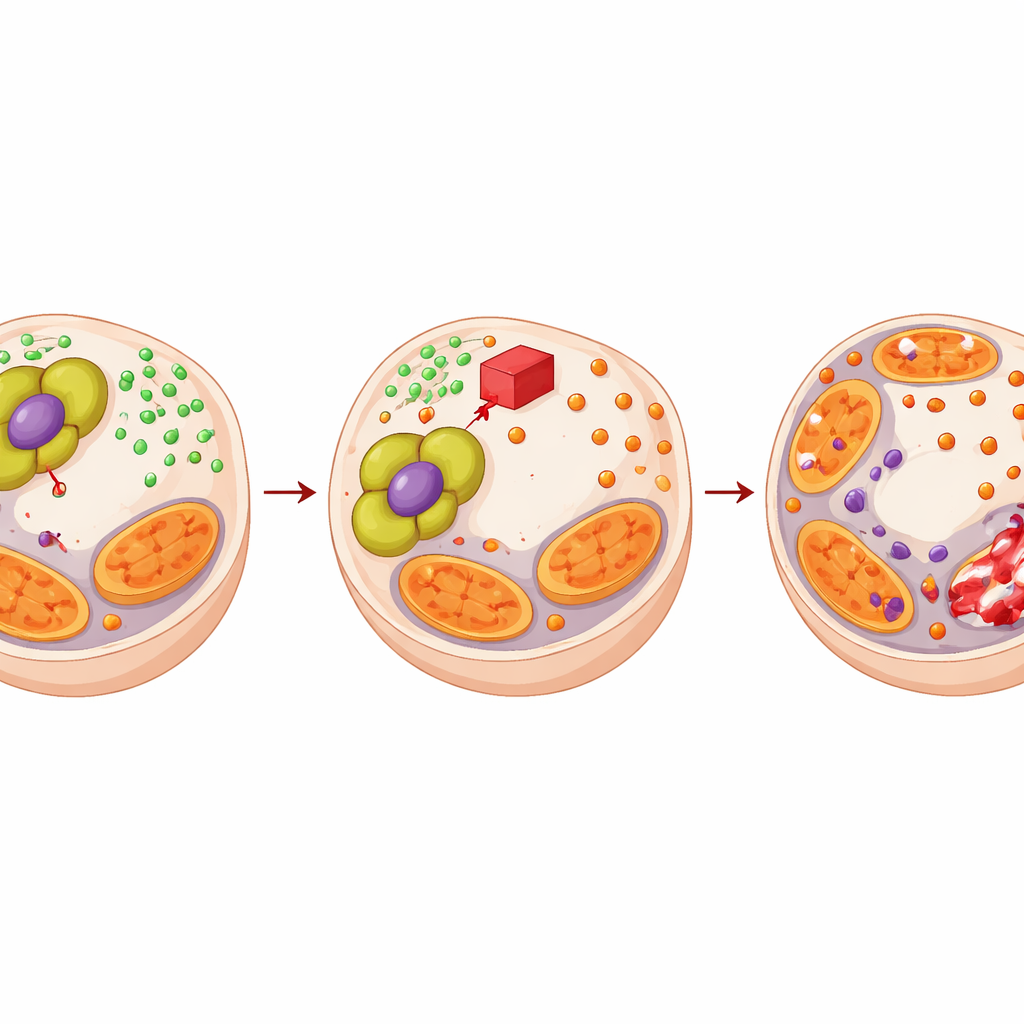
Преобразование уязвимости в терапевтическую стратегию
Поскольку PDHA1 помогает опухолям противостоять энзалутамиду, укрепляя систему буферизации меди, авторы проверили, не может ли препарат, нацеленный на PDHA1, изменить ситуацию. Они использовали CPI‑613 — соединение, нарушающее работу того же метаболического комплекса. CPI‑613 сам по себе усиливал медный стресс и повреждал митохондриальные белки в клетках рака предстательной железы, при этом не повреждая нормальные клетки предстательной железы. В комбинации с энзалутамидом CPI‑613 подавлял рост раковых клеток гораздо сильнее, чем любое из средств по‑отдельности; математический анализ подтвердил истинный синергизм. В моделях опухолей на мышах и при трансплантатах от пациентов пара препаратов давала меньшие опухоли, больше мёртвых участков ткани, меньше делящихся клеток и более выраженные сигнатуры медью‑опосредованной гибели клеток.
Что это значит для пациентов
В совокупности результаты показывают: некоторые опухоли предстательной железы уходят от действия энзалутамида, перестраивая метаболизм так, чтобы увеличивать производство ацетил‑CoA, переписывать активность генов и повышать уровень глутатиона, который нейтрализует токсичную медь и блокирует купроптоз. При ингибировании PDHA1 этот защитный контур можно разрушить, позволив медью‑опосредованной гибели клеток идти своим путем и восстанавливая эффективность гормон‑блокирующей терапии. Хотя необходимы клинические испытания, работа указывает на конкретную, проверяемую стратегию: сочетание энзалутамида с препаратами, нацеленными на PDHA1, такими как CPI‑613, чтобы преодолеть резистентность при продвинутом, трудноподдающемся лечению раке предстательной железы.
Цитирование: Zhuang, R., Zhou, Q., Cheng, B. et al. PDHA1–acetylation signaling suppresses cuproptosis to attenuate anti-androgen effect in prostate cancer. Cell Death Dis 17, 243 (2026). https://doi.org/10.1038/s41419-026-08462-1
Ключевые слова: рак предстательной железы, резистентность к лекарствам, медью‑индуцированная гибель клеток, метабилизм рака, эпигенетическая регуляция