Clear Sky Science · ru
Сигнализация IRE1 в эндотелии поддерживает целостность гематоэнцефалического барьера и ограничивает нейровоспаление после травмы головы
Почему важно защищать «внутреннюю стенку» мозга
После удара по голове первоначальное повреждение — лишь часть картины. В последующие часы и дни мозг запускает мощную стрессовую и иммунную реакцию, которая может незаметно расширять зону поражения. В этом исследовании изучают, как небольшая система распознавания стресса внутри клеток, выстилающих сосуды мозга, помогает сохранять «внутреннюю стенку» мозга — гематоэнцефалический барьер — герметичной и спокойной после черепно-мозговой травмы. Понимание этой скрытой защиты может указать путь к новым лечениям, уменьшающим длительную инвалидизацию после травм головы.
Стражи мозга под давлением
Мозг опирается на специализированный барьер, образованный эндотелиальными клетками, которые выстилают просвет сосудов и строго контролируют, что может переходить из крови в ткань мозга. Черепно-мозговая травма (ЧМТ) может нарушить этот барьер, позволив воспалительным молекулам и иммунным клеткам проникнуть внутрь и усугубить повреждение. Внутри эндотелиальных клеток действует система контроля качества — ответ на накопление белков в незавёрнутом виде (unfolded protein response), помогающая клеткам справляться со стрессом в органелле, называемой эндоплазматическим ретикулумом. Один из ключевых компонентов этой системы, IRE1, служит датчиком и регулятором при клеточном напряжении. Авторы задали вопрос: помогает ли этот эндотелиальный сенсор защищать барьер после ЧМТ или, наоборот, усугубляет ситуацию?
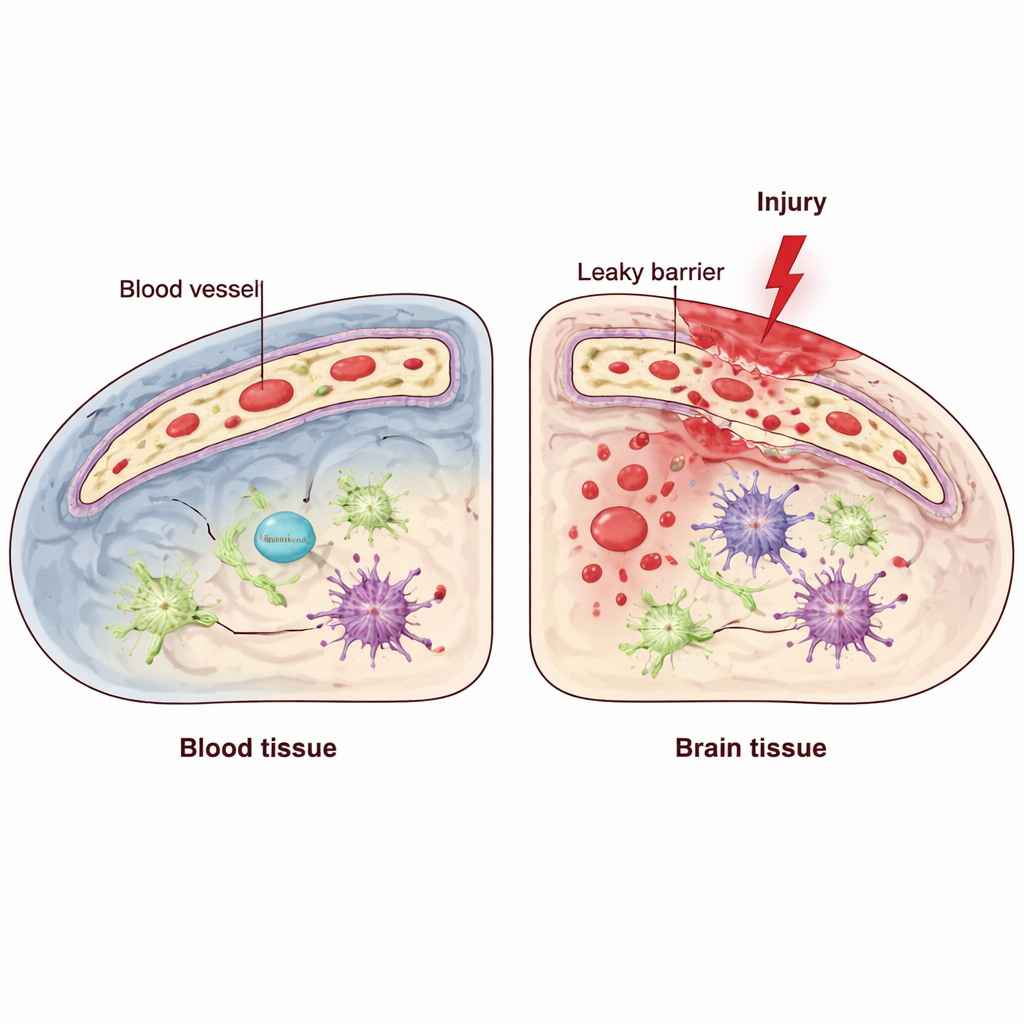
Выключение клеточного датчика в сосудистых клетках
Чтобы выяснить это, исследователи использовали генетически модифицированных мышей, у которых IRE1 можно было выборочно отключать только в эндотелиальных клетках. Затем они моделировали контролируемое повреждение в моторной коре, имитируя аспекты человеческой ЧМТ, и сравнивали этих животных с нормальными сиблингами. Оценивали движение с помощью заданий на равновесие и точную постановку лап, а также исследовали ткань мозга с помощью высокоразрешающей микроскопии и молекулярных методов. У нормальных мышей активность IRE1 в клетках сосудов рядом с повреждением повышалась вскоре после травмы, что говорит о том, что эндотелий быстро чувствует и реагирует на стресс. В отсутствие IRE1 именно в этих клетках животные показывали худшие результаты в моторных тестах, что указывает на менее успешное функциональное восстановление.
Протекающие сосуды, больше иммунных клеток и гибнущие нейроны
Далее исследователи оценили, насколько сохраняется гематоэнцефалический барьер. В норме крупные сывороточные белки, такие как антитела, остаются внутри сосудов. После ЧМТ в зоне очага ожидается некоторая утечка, но у мышей без эндотелиального IRE1 наблюдалось значительно более широкое просачивание этих белков в мозг. Микроскопия показала снижение уровня важного контактного белка VE‑cadherin, который герметизирует прилегающие эндотелиальные клетки, в повреждённой области при отсутствии IRE1, хотя общее количество сосудов выглядело схожим. Эта проницаемость сопровождалась притоком иммунных клеток в область вокруг очага и повышением уровней провоспалительных сигналов. В тех же зонах нейроны чаще демонстрировали признаки дегенерации и программируемой гибели, а зона повреждённой ткани вокруг ядра травмы была заметно больше.
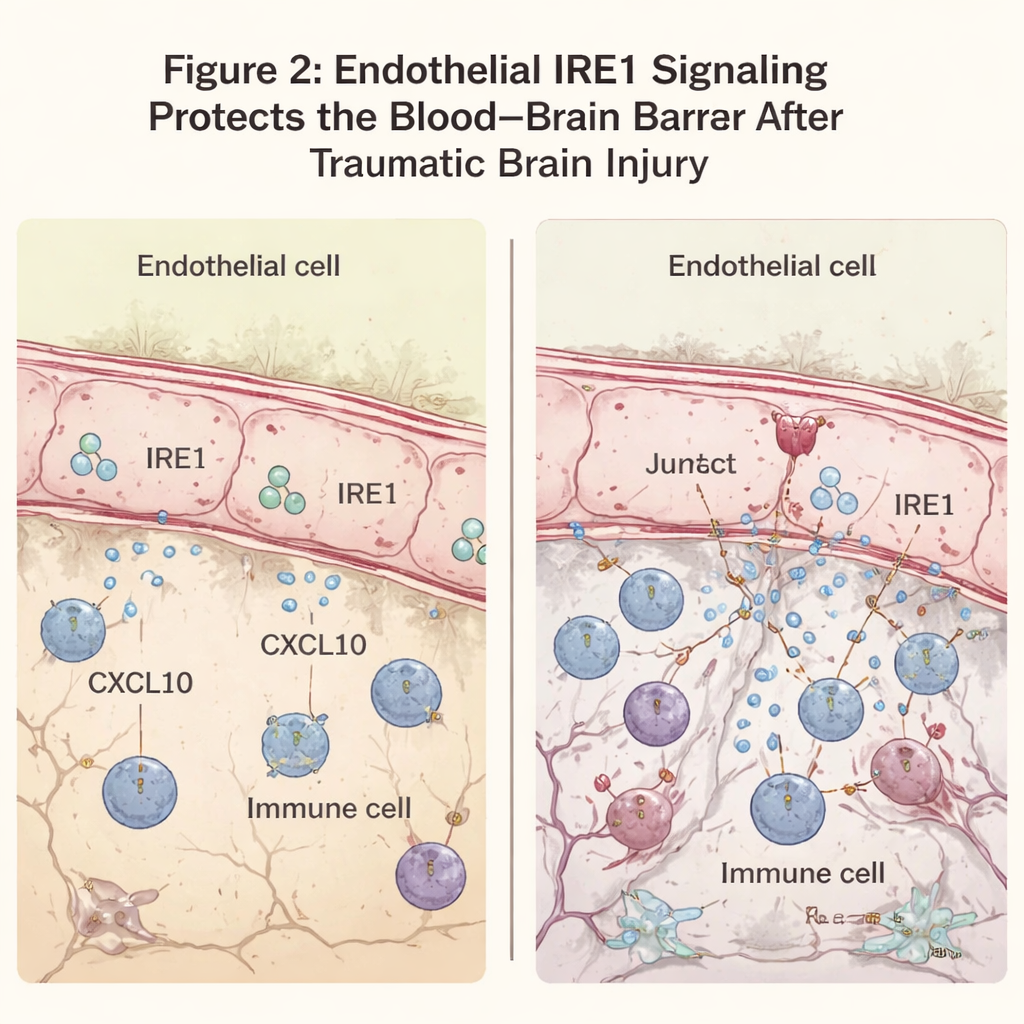
Препарат против стресса усмиряет вспышку сигналов
Чтобы понять молекулярные механизмы, команда проанализировала, какие гены активируются после травмы. У мышей без эндотелиального IRE1 существенно усиливалась экспрессия генов, связанных с антивирусным и воспалительным ответом. Особенно выделялся CXCL10 — хемокин, своего рода молекулярная вспышка, привлекающая иммунные клетки и потенциально ослабляющая барьер. CXCL10 был особенно повышен в эндотелиальных клетках рядом с очагом при отсутствии IRE1. В культуре мозговых эндотелиальных клеток при воздействии провоспалительного стимула снижение стресса эндоплазматического ретикулума с помощью препарата TUDCA снижало и активность IRE1, и продукцию CXCL10. При введении травмированным мышам TUDCA уменьшал уровни CXCL10 и маркеров иммунных клеток в повреждённой коре и улучшал моторные показатели, что наводит на мысль: подавление этого стрессового пути может ослабить вторичное повреждение.
Что это значит для людей с травмами головы
Проще говоря, работа показывает: сенсор стресса IRE1 в клетках, выстилающих сосуды мозга, действует как страж после черепно-мозговой травмы. Когда он присутствует и функционирует, он помогает сохранять гематоэнцефалический барьер плотным, уменьшает выброс химических сигналов, привлекающих иммунные клетки, и ограничивает распространение воспаления и гибель нейронов вокруг очага. При его выключении барьер становится более проницаемым, иммунные клетки проникают в мозг, и повреждений становится больше. Поскольку клетки сосудов относительно доступны для действующих через кровоток препаратов, нацеливание на их стрессовые ответы — с помощью соединений вроде TUDCA или более точных будущих терапий — может стать практической стратегией для уменьшения долгосрочного вреда после травм головы.
Цитирование: Fan, Q., Takarada-Iemata, M., Tanaka, T. et al. Endothelial IRE1 signaling maintains blood–brain barrier integrity and limits neuroinflammation after traumatic brain injury. Cell Death Dis 17, 210 (2026). https://doi.org/10.1038/s41419-026-08461-2
Ключевые слова: черепно-мозговая травма, гематоэнцефалический барьер, эндотелиальные клетки, нейровоспаление, клеточный стресс