Clear Sky Science · ru
CD36 повышает чувствительность клеток тройного негативного рака молочной железы к палмитат-индуцируемому ферроптозу
Почему жир вокруг опухолей может быть и другом, и врагом
Опухоли молочной железы развиваются в ткани, естественно богатой жиром, и известно, что раковые клетки «подкармливаются» близлежащими жирными кислотами. Это исследование выявляет неожиданный поворот: при определённых условиях один из наиболее распространённых жиров в организме — пальмитиновая кислота — может на самом деле способствовать уничтожению особенно агрессивной формы рака молочной железы, запускаючи специфический тип клеточной гибели. Понимание того, как это происходит, может указать путь к новым методам лечения для пациентов, у которых сейчас мало опций.
Трудно поддающийся лечению рак молочной железы под микроскопом
Тройной негативный рак молочной железы (TNBC) лишён рецепторов гормонов и факторов роста, на которые нацелены многие современные препараты, что делает его одним из самых трудноизлечимых типов рака молочной железы. Эти опухоли находятся в тесном контакте с адипоцитами, которые выделяют большие количества жирных кислот, включая насыщенную пальмитиновую кислоту. Исследователи хотели выяснить, действительно ли пальмитиновая кислота просто подпитывает рост опухоли, или она также может создавать уязвимость, которую можно использовать для уничтожения раковых клеток.
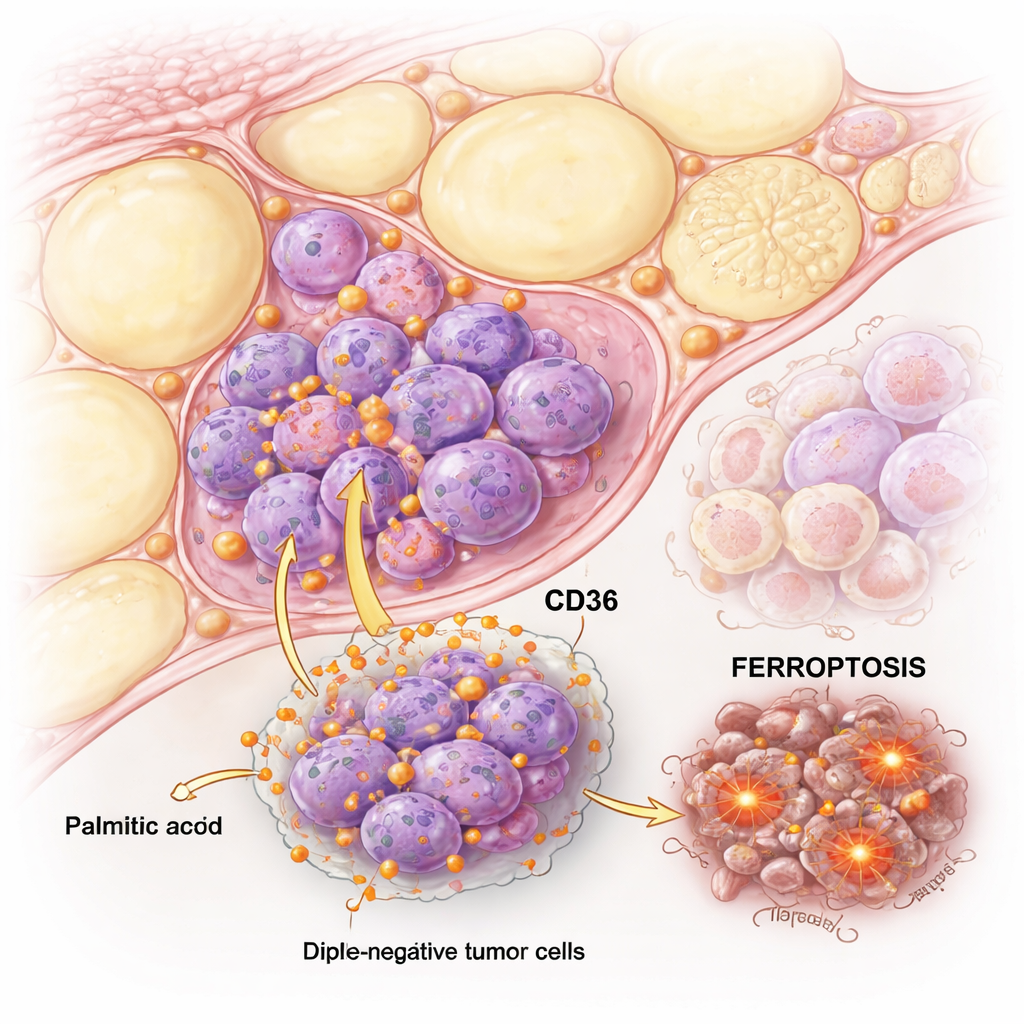
Когда пальмитиновая кислота доводит раковые клетки до предела
Команда сравнила клетки TNBC с гормон-чувствительными «люминальными» клетками рака молочной железы и подвергла их воздействию возрастающих доз пальмитиновой кислоты. Оба типа клеток могли пострадать от высоких доз, но TNBC-клетки оказались значительно более чувствительны. Детальные тесты показали, что в люминальных клетках пальмитиновая кислота в основном вызывала классическую апоптозную гибель — аккуратную форму смерти клетки. В клетках TNBC, однако, пальмитиновая кислота запускала и апоптоз, и другой, менее знакомый путь — ферроптоз, который зависит от железа и разрушения липидов клеточных мембран.
Жировой «дверной проём» под названием CD36
Чтобы понять, почему TNBC-клетки реагировали так иначе, исследователи сосредоточились на CD36 — белке на поверхности клетки, выполняющем роль дверного проёма для длинноцепочечных жирных кислот. В TNBC-клетках естественным образом было заметно гораздо больше CD36, чем в люминальных клетках, и воздействие пальмитиновой кислоты ещё больше повышало уровень CD36. Это означало, что TNBC-клетки вбирали больше пальмитиновой кислоты, накапливали повреждённые липиды, производили больше реактивных форм кислорода в митохондриях и накапливали больше свободного железа внутри клетки — все ключевые признаки ферроптоза. Когда CD36 блокировали с помощью препарата или снижали генетическими методами, индуцируемый пальмитиновой кислотой ферроптоз резко уменьшался.
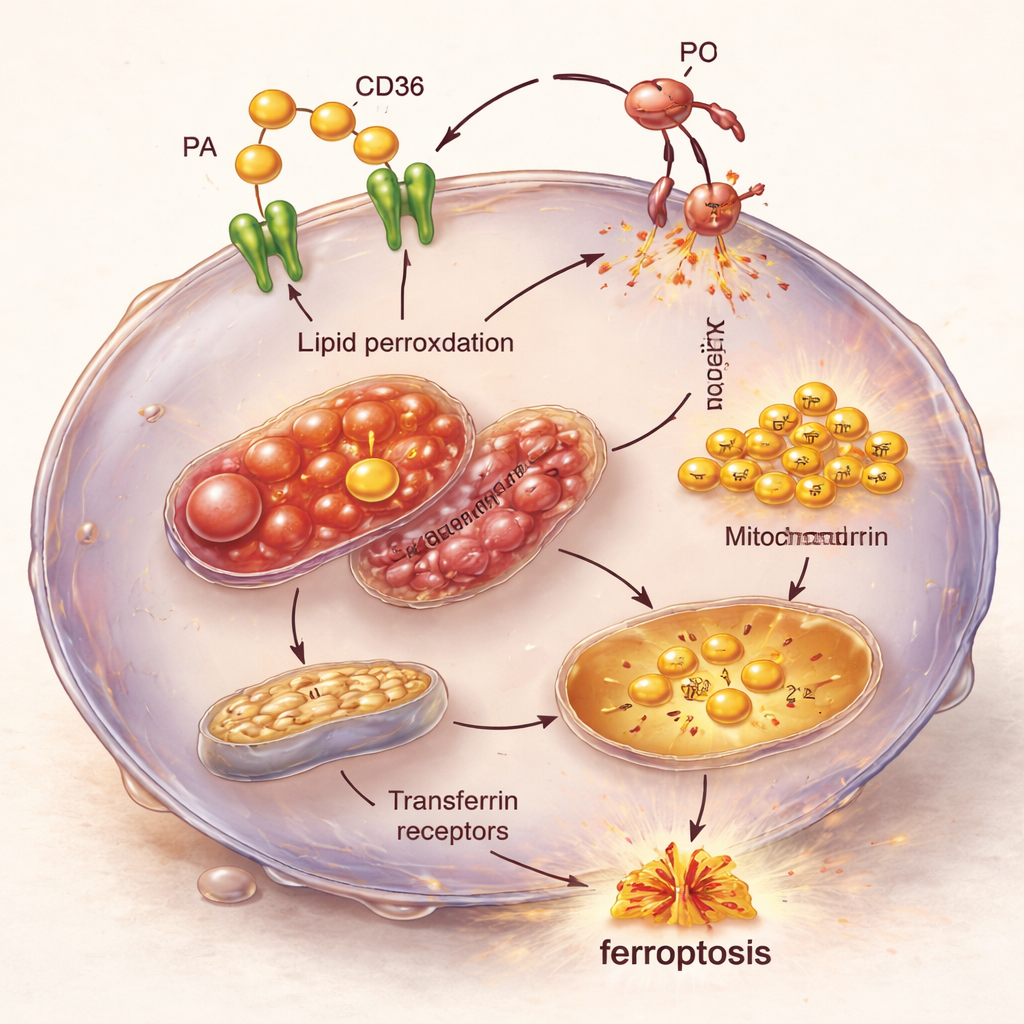
Взгляд на цепную реакцию внутри клетки
Микроскопия и анализ активности генов показали внутреннюю цепную реакцию, лежащую в основе этой уязвимости. TNBC-клетки, перегруженные пальмитиновой кислотой и CD36, демонстрировали распухшие, структурно повреждённые митохондрии и повышенные уровни железа, доставляемого через трансферриновые рецепторы. Одновременно включались гены, способствующие ферроптозу, в то время как гены, которые обычно защищают от этого типа клеточной гибели, были понижены. В результате возникал идеальный шторм: поступление избытка жира, больше доступного железа для поддержания реакций и ослабленные защитные механизмы против повреждения липидов — все это вместе толкало TNBC-клетки к ферроптозу.
Какие пациенты могут выиграть больше всего?
Рак не является однородным, даже среди TNBC. Используя образцы опухолей, выращенные в мышах, и большие базы данных пациентов, авторы обнаружили, что CD36 особенно высок в одном подтипе TNBC, называемом люминально-андрогенно-рецепторным (LAR), который ранее уже отмечался как более чувствительный к ферроптозу. Другие подтипы TNBC с высоким поглощением железа также, как правило, демонстрировали более высокий уровень CD36. Эта картина указывает на то, что CD36 может служить маркером для идентификации пациентов, чьи опухоли естественно подготовлены для терапии, основанной на ферроптозе.
Превращая обычный жир в терапевтического союзника
Проще говоря, эта работа показывает, что распространённый диетический и тканевой жир — пальмитиновая кислота — может способствовать гибели определённых клеток тройного негативного рака молочной железы, когда они экспрессируют высокий уровень транспортёра жиров CD36. Провоцируя перегрузку липидами, накопление железа и повреждение клеточных мембран, CD36 делает эти раковые клетки более склонными к ферроптозу — разрушительной участи, от которой они не в состоянии спастись. Если будущие методы лечения смогут безопасно усилить этот путь — или сочетать его с препаратами, дополнительно ослабляющими защиту клеток — клиницисты смогут превратить метаболическую уязвимость в новый, более точный способ атаки некоторых из самых агрессивных опухолей молочной железы.
Цитирование: Closset, L., Foy, JP., Louadj, L. et al. CD36 enhances sensitivity of triple negative breast cancer cells to palmitate-induced ferroptosis. Cell Death Dis 17, 219 (2026). https://doi.org/10.1038/s41419-026-08460-3
Ключевые слова: тройной негативный рак молочной железы, ферроптоз, CD36, пальмитиновая кислота, метаболизм опухоли