Clear Sky Science · ru
Дебикувитинирование гексокиназы 2, опосредованное USP30, контролирует метаболическую судьбу глюкозы и прогрессирование опухоли
Как раковые клетки перенастраивают использование сахара
Раковые клетки известны своим «сладким аппетитом»: они используют сахар необычными способами, чтобы подпитывать быстрое деление. В этом исследовании обнаружен новый переключатель — белок USP30, который помогает опухолевым клеткам решать, как расходовать глюкозу. Тонко регулируя другой белок, гексокиназу 2 (HK2), USP30 может сдвигать клетки в сторону интенсифицированного сжигания сахаров и ускоренного роста, что указывает на новую потенциальную мишень для противораковой терапии. 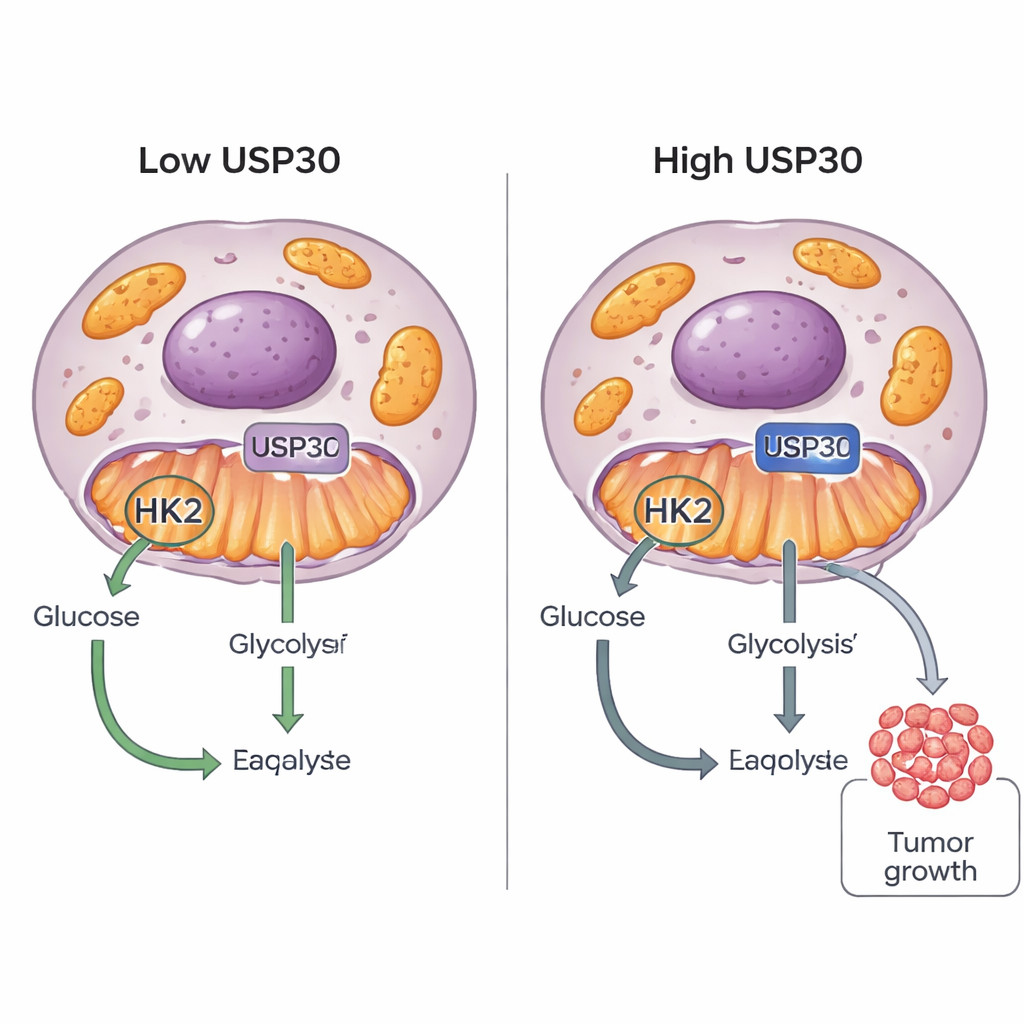
Сахароохотничий образ жизни внутри опухолей
Большинство здоровых клеток извлекают энергию из питательных веществ эффективно, но многие раковые клетки отдают предпочтение быстрому и менее бережливому пути — аэробному гликолизу, известному также как эффект Варбурга. Они поглощают большие количества глюкозы и быстро превращают её в лактат, даже при наличии кислорода. Такая стратегия даёт не только энергию: она обеспечивает строительные блоки для ДНК, липидов и белков, помогает опухолям выживать при стрессе и может ослаблять иммунный ответ. На входе в этот путь стоит гексокиназа — фермент, который помечает поступающую глюкозу фосфатной группой, придавая ей обязательный статус для дальнейшего распада и синтетической активности.
Митохондриальный фермент выходит на авансцену
USP30 — это фермент, расположенный на наружной поверхности митохондрий, энергетических станций клетки. Он принадлежит к семейству дебикувитиназ, которые снимают крошечные белковые метки — убиквитин — с других белков, часто изменяя их стабильность, локализацию или активность. Ранее USP30 был известен по ролям в нервных клетках и в контроле качества митохондрий, но его влияние на рак оставалось неясным. Анализ больших баз данных по раковым генам показал, что опухоли с повышенным уровнем USP30 склонны демонстрировать усиленные сигнатуры сжигания глюкозы и ослабленные сигнатуры распознавания жиров, что наводит на мысль: USP30 может помогать онкозависимым клеткам переключаться на сахарозависимый образ жизни.
Связь USP30 с «вратарями» клеточного обмена сахара
Чтобы проверить эту связь, исследователи понижали или удаляли USP30 в нескольких линиях раковых клеток и измеряли их энергетическую переработку. С помощью приборов, отслеживавших в реальном времени выработку кислоты и потребление кислорода, они обнаружили, что потеря USP30 резко снижает как гликолиз, так и митохондриальное дыхание. Производство лактата и потребление глюкозы упали, что свидетельствует о замедлении «сахарного двигателя» клеток. Серия экспериментов с масс-спектрометрией затем показала, что USP30 физически взаимодействует с несколькими ферментами, связанными с обменом глюкозы, прежде всего с гексокиназами HK1 и HK2. Последующие тесты продемонстрировали, что это взаимодействие зависит от каталитической активности USP30 и происходит напрямую, а не через промежуточные партнёры.
Точная молекулярная ручка на гексокиназе 2
Углублённое изучение выявило, что USP30 удаляет специфические типы убиквитиновых цепочек — так называемые атипичные звенья — с HK1 и HK2. Для HK2 это редактирование происходит в одной ключевой аминокислоте — лизине 144 (K144). При мутации K144, при которой лизин теряет способность нести убиквитин, HK2 становится более стабильной, сильнее связывается с каналоподобным белком VDAC1 на митохондриях и демонстрирует повышенную ферментативную активность. Клетки, запрограммированные нести эту K144-мутацию, направляли больше HK2 к митохондриям, сильнее сжигали глюкозу, выделяли больше лактата и демонстрировали более быстрый рост и подвижность в культурах. У мышей опухоли, выращенные из клеток с мутантной HK2 K144, росли крупнее и быстрее, чем опухоли с нормальной HK2, что подчёркивает значимость этого крошечного молекулярного переключателя. 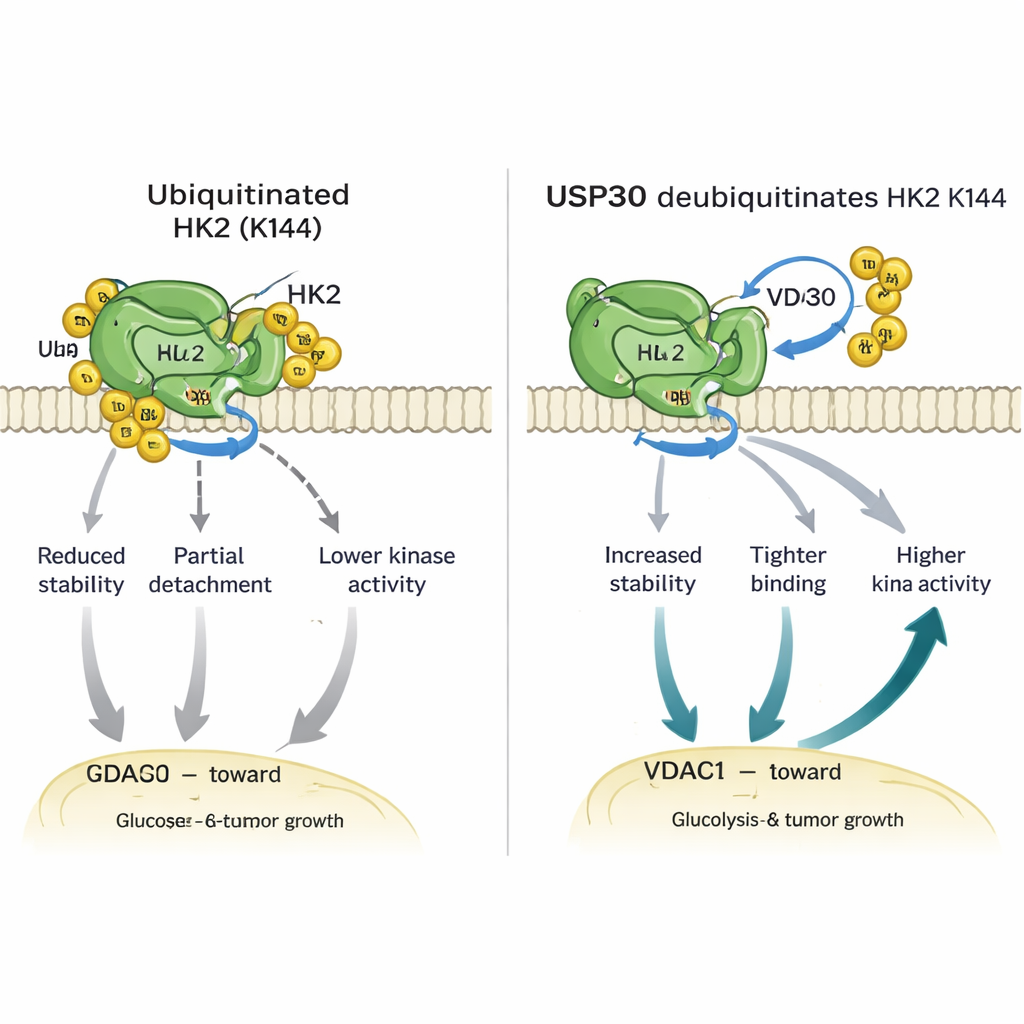
Превращение метаболического переключателя в преимущество роста
Эти результаты выстраивают ясную цепочку событий: USP30 связывается с HK2, снимает убиквитиновые метки с K144 и тем самым удерживает HK2 в активном состоянии и прикреплённой к митохондриям. Это усиливает гликолиз, питает деление и миграцию опухолевых клеток и в конечном счёте ускоряет рост опухоли. При отсутствии или неактивности USP30 HK2 становится менее стабильной и эффективной, и раковые клетки теряют часть своего метаболического преимущества. Проще говоря, USP30 действует как механик, который поддерживает «сахарный двигатель» раковой клетки в настроенном и закреплённом состоянии — уберите механика, и двигатель начинает захлёбываться.
Что это значит для будущего лечения рака
Для неспециалиста главный вывод в том, что раковые клетки зависят от тонкой настройки того, как они «сжигают» сахар, и USP30 — недавно обнаруженная ручка на этой панели управления. Стабилизируя HK2 в одной конкретной точке, USP30 помогает опухолям поддерживать глюкозоохотливый метаболизм и расти агрессивнее. Препараты, блокирующие USP30 или разрушающие его связь с HK2 на лизине 144, могли бы ослабить опухоли, «истощая» их сахарный двигатель, при этом не обязательно нанося такой же ущерб нормальным клеткам. Эта работа добавляет важный кусок в головоломку того, как рак перенастраивает метаболизм, и предлагает перспективный новый подход для таргетной терапии.
Цитирование: Haowei, Z., Li, X., Liao, W. et al. USP30-mediated Deubiquitination of Hexokinase 2 controls the metabolic fate of glucose and tumor progression. Cell Death Dis 17, 225 (2026). https://doi.org/10.1038/s41419-026-08459-w
Ключевые слова: метаболизм рака, гликолиз, гексокиназа 2, USP30, эффект Варбурга